范特霍夫等温方程推导过程
粉丝111获赞656
相关视频
 05:12
05:12 28:26查看AI文稿AI文稿
28:26查看AI文稿AI文稿高考化学反应原理的真题中,越来越多的题目以阿伦尼乌斯公式以及范特霍夫方程为背景出题。范特霍夫方程同学们可能会感觉陌生一些,这节课带同学们学习范特霍夫方程在高考中的应用。 范特霍夫方程描述的是化学平衡长数和 t 分之一,这个 t 就是温度啊,和 t 分之一的关系。他的图像和阿伦尼乌斯公式描述的图像非常的相像,那如果阿伦尼乌斯公式没有什么基础的同学,可以去看一下咱们的 一轮课程,就在一站的收藏夹一轮的课程,一轮课程里对阿伦尼乌斯公式有非常详细的讲解,阿伦尼乌斯公式看清楚,描述的是速率长数和替分之一的关系。 范特霍夫是化学平衡长数和 t 分之一的关系。速率长数和化学平衡长数是不同的。 阿伦尼乌斯公式里面有个重要的结论啊,你看这就是速率长数了,和替分之一的关系。注意好阿伦尼乌斯公式的相关结论。烙印速率长数和替分之一的图像中,那这个直线他的斜率如果越大,对应的反应活化能越高。 那比如说一二三这三条线谁的斜率最大呢?很明显,三的话斜率最大吗?所以他的活化能是最高的。这个在考试中经常会考到, 范特或副方程也有类似的结论。首先认识一下这个方程, k c, 他指的是标准平衡常数,这个东西叫做标准摩尔函变,那实际 上高中是不学他们的,展现到高考上的话,其实这个 k c 塔你就直接看成平衡常数也行。实际上在高考题中,比如说二一年考出来的全国卷高考题里面,纵坐标他并没有写什么 loin k c 塔,他就直接写的是 loin k, 直接写成了化学平衡常数啊。所以说这玩意你就看成化学平衡常数,然后标准摩尔含变的话,就直接看成正常的含变就行了,就直接就写成德特 h 即可。 那至于后边这部分的话,跟同学没什么关系啊, r 是一个常数, r 分之这个玩意咱们就直接看成 x 即可啊,直接就看成一个 x 即可啊,就跟咱们没有什么太大的关系。前面的这个 r 也是一个常数,所以范特护肤方程咱们直接可以看成这种 十字,那在高考出题里面,他出现的也是这种十字啊,都是烙印 k 等于 r 分之负,德特 h 乘以 t 分之一加 x。 那注意好,范特霍夫方程研究的是 k 和 t 分之一的关系,纵坐标是烙印 k 横坐标, 这是横坐标啊,是 t 分之一,那也就是说又变成了 y 等于 k s 加 b 的一个形式,对吧?那这玩意儿负的二分之 that h 是不是就是斜率? 直线的斜率这个玩意它就是洁具啊,洁具的话咱们不考,所以你主要要记清楚,化学平衡常数和 t 分之一的图像中,负的 r 分之的 th 就是直线的斜率。那我们来看 一下具体的应用。烙印平衡长数和 t 分之一的图像是一条直线,相信这种图像同学们已经见了很多次了,见过的同学可以在弹幕上打个一, 非常的常靠。那首先由于刚才已经给同学们说了,这种图像它的斜率就是负的, that h 除以 r, 那考试中经常就是问你,比如说给你这两条线,问你这两个线所对应的反应是吸热还是放热?那普通的做法同学们肯定也都知道啊,就比如说,你看,随着横坐标的增大, 横坐标的增大,其实就是温度的降低,随着温度的降低,这两条线他的 k 是不是也在降低,说明降低温度平衡,逆向移动,那降低温度向放热方向移动,逆向放热,正向是不是吸热?哎,就能推出来这两 两个反应啊,他肯定都是吸热反应, ok 吧?啊?这两个反应肯定就是吸热反应。由于斜率是负的, r 分之的 th, 所以对于吸热反应而言,这个斜率他是不是小于零啊? 对吧?这个玩意斜率是不是小于零?得特 h 是大于零的,而这个长数也是大于零的,那前面加个负号就是小于零的,所以吸热反应斜率它是小于零的,那对于放热反应而言,得特 h 如果小于零了, 那这里小于零,而是大于零的,前面再加个负号,是不是就斜率就大于零了?所以对于吸热反应而言,斜率它是负的。对于放热反应而言,斜率是正的。所以首先我们可以通过 这些线的斜率快速判断这个反应到底是吸热还是放热,那口诀的话就是正放复吸 斜率,如果是正的反应,就是放热斜率,如果是负的,比如这两个斜率是负的,那他就是吸热反应。那当然普通的判断方法也是可以的。你如果不想记那么多,你看 随着横坐标的增大, t 分之一增大,实际上温度是不是在减小?随着温度的减小,平衡长数是不是越来越小了?说明降温平衡逆向移动,逆向放热,正向吸热,是不是也能判断出来得到一尺大于零?但是有时候你针对这种图像记一下这个结论,可以极大地缩短你的做题时间。 那除了这点,就是你根据斜率可以判断西放热以外,我们还能判断西放热也就是这个寒 变的大小。那一般来说是判断含变绝对值的大小啊,因为有些反应的话,它是吸热的,德特 h 是大于零的,有些反应的话,它是放热的,德特 h 是小于零的。咱们判断的是德特 h 绝对值的大小。 那判断的时候怎么看呢?那你想一想,负的二分之得特 h, 这是斜率啊,你给斜率加一个绝对值是啥?是不是二分之得特 h? 那同学们思考一个问题, r 分之 that h 如果越大的话, 就是斜率的绝对值,越大的话,那对应这个 that h 的绝对值是不是一定也越大?我再说一遍啊,这是个简单的数学问题。首先斜率是这玩意儿,你给斜率 加一个绝对值,是不是相当于就是给上边的这个 that h 加了个绝对值?这个负号是不是就不用管了?因为 r 一定是个正数,对吧?所以斜率的绝对值就等于他。那你想一想,斜率越大的话,对应的 that h 的绝对值是不是一定越大? 所以这个结论也需要记住啊,就是斜率越大,代表含变的绝对值越大。那我们来看一下这两条线,你能分辨的出来哪一个反应含变更大一点吗? 如果没有给你标,那也可以轻松的找出来。由于这条线斜率更大,所以它含变的绝对值更大,又由于正放负息斜率是负的, 所以它是一个吸热反应,对吧?正放复吸斜律为负, 那就是吸热反应。吸热反应的话,含变本来就是大于零的,对吧?那这条线含变的绝对是更大。由于含变本来就是大于零的,那 that h 本来就是大于零的嘛?那就证明这条线的 that h 是不是也就越大一点? ok 啊!首先记清楚这几个结论,咱们先来实战几道经典的模拟题, 接着再来做高考真题啊。比如说恒温恒融的条件下,像密闭容器充入一定量的 x, 发生两个反应,让你画一下这个能量图,看一下能量图和这个曲线最接近的是谁,能不能快速做出来呢?可以暂停一下,同学们自己做一下啊。实际上,根据咱们讲的结论, 那既然它是烙印平衡常数和 t 分之一图像的关系,根据正放复析图像斜率,它都是负的,所以 这两个反应都是吸热反应,对不对?那这两个反应都是吸热反应的话,这两个反应的能量来看, x 能量是不是小于 y, y 的能量是不是小于 z? 那你来看一下,符合能量关系的是不是只有 a, x 能量是不是小于 y, y 的能量是不是小于 z? ok 吧,直接选出 a 选项,那有些同学可能又会有疑问,这道题是正好只有 a 选项满足了, x 到 y, y 到 z 全是吸热反应,那如果人家这个题还有一个图也是这两个反应都是吸热的过程呢?到底选谁? 比如说再给同学们出一道题来看, x 到 y, y 到 z 是不是也是吸热反应呢?这两个图 如果对比的话,哪个正确呢?其实还是可以看因为斜率,反应二的斜率是不是更大一点,所以反应二德特 h 的绝对值更大一点,对吧?所以反应二的德特 h 绝对值大于反应一的德特 h 绝对值。那我们来看一下, 来看这个图,反应一得特 h 的绝对值是不这么多?反应二得特 h 的绝对值是不这么多。那这个图的话,反应一得特 h 绝对值是不大于反应二的,就这个得特 h, 其实就两个物质的能量差吗? 是不是?那你说反应一的绝对值是不是就 x 到 y 的能量差,对吧?就这一段,很明显,这个图的话,反应一 that h 的绝对值是不是要更大一点?但是图像中 展现出来的是反应二的 that h 的绝对值要更大,那你来看这个图,这是反应一 that h 绝对值,对吧? 这是反应二 that h 绝对值很明显,反应二 that h 绝对值数更大一点,因此 a 选项正确。 再来看一道题,反应一二三给你,然后给的是烙印平衡长数和 t 分之一的图像,问你反应二对应的直线应该是谁?反应二来看是一个吸热反应啊,对吧?就不用再分析了,或者你喜欢什么,随着横坐标的增大,温度在减小, k 怎么怎么变? 那你最后可以拿这种分析的过程是不是给自己考试题做一个验算,对吧?那如果说直接碰到了这种模型的话,那咱们就直接套结论了,正放负 息,根据正放复息,由于反应二 that h 是正的, 它是一个吸热的反应,对吧?那它的斜率就是负的,来看一下 a 和 b 谁斜率是负的,是不是 b, 直接写 b 是不是就行了? 正放负吸,这个指的是放热,这个指的是吸热啊,正负指的是斜率,那反应二的话,它是一个吸热的过程,那斜率就是负的吧?这种图对吧?直接写 b 即可。接着让你绘制反应三的图像。 反应三首先是不是得算一下 deta h? 那咱们来看一下计算过程啊。首先根据 get 定律,一减二可以得到反应三,反应三呢? deta h 是负的,八十九,反应三也是放热反应,根据正放 负西放热反应,它的斜率是不是应该为正直?哎,所以它的斜率要画的话肯定是正的,那画的时候就存在一个问题,它的斜率到底是比 a 这条线大,还是要比 a 这条线小呢?那这道模考题考出来的时候也是连考题啊,很多同学可能就蒙了, 其实直接套咱们讲的结论,也不用说是像标准答案那么复杂的证明过程,对吧?咱们直接套结论,斜率越大, that h 的绝对值是不是越大?由于你注意好, that h 三的绝对值是八十九, 是这样吧。那你 a 这条线的话,对应的是反应一,反应一的绝对值是四十九,得特 h 绝对值是四十九,那所以反应一得特 h 的绝对值小于反应三得特 h 的绝对值,绝对值越大,斜率越大嘛。所以说反应三的斜率是不是肯定得大一点?图像是不是应该这样画? ok 吧,同学们,图像应该这样画,那标准答案的证明的话,其实就是利用 get 定律之间的加减去证明的,还是比较费时间的,对吧?也是可以证的啊。嗯,但是如果说你直接知道结论的话,那相当于这这道题的话,那可能就是个 十秒钟,是不是就写完了,会给你节省很多时间啊,毕竟这也是热门题型。好,那咱们再来看一道非常经典的联考题, 好多同学都被这个题恶心过。首先啊,给你三个反应,又给你了函数关系,那你看这个函数关系是不是长得很像,是不是就是范特霍夫方程的变形? long k 等于 t 分之一个数值,再加 x, 这个是洁具。那 这个玩意是谁呢?是斜率啊,对不对?画烙印 k 和 t 分之一的图像,那这个三四五一九就是斜率,斜率是咋表示的来着?负的二分之得特 h, 所以这个玩意是负的二分之得特 h 一, 这个玩意儿是负的二分之得特 h 二,这个玩意儿是负的二分之得特 h 三, ok 吧,哎,这样子咱们就知道了,其实这三个数值啊,和 that h 是有关系的,那 r 是个常数啊,对吧?你是不是可以根据这三个数值直接去求出啊? that h 一, that h 二, that h 三,谁大谁小, 是这样吧,同学们,而且你还可以看出来 dot h 一, dot h 二, dot h 三的正负,那同学们来 说,这三个反应是放着还是吸着反应啊?由于 r 是一个正的常数,对吧?那你说负的 r 分之得特 h 一得特二 h 二得特 h 三都是大于零的,那得特 h 是不是必然是小于零的,才能保证这三个东西它是一个正的。常数 是这样的吧,因为比如说三四一五九,它是负的,二分之 deta h 一这个玩意是正的,前面是负的,那这个玩意必须是不是也是负的,整体才能是正的, 对吧?因为三四一五九是个正值啊,所以咱们可以快速的看出来, that h 一, that h 二, that h 三都是小于零的,那反应的活化能呢?就是你用活化能算 that h, 那就 that h 等于正反应活化能,减逆反应活化能, 这是热化学部分的一个小结论,对吧? deh 等于正反应活化能,减逆反应活化能。那现在注意好, deh 都是小于零的呀,正反应活化能是不是肯定要小于逆反应活化能? 是这样吧,这是第一问啊。第二问, that h 二比 that h 三的数值范围是多少?让你选这个东西啊,很多同学的话,考场上确实选不出来,同学们也可以暂停一下,自己尝试着看能不能做出来。 我估计很多同学还是做不出来的啊,因为标准答案的话,他给的过程啊,你看,让你算的是德特 h 二,德特 h 三,对吧?哎,你要把这个德特 h 一和德特 h 二、德特 h 三联系起来,根据德特 h 一效于零,然后再推出德特 h x, 得到 h 三之间的一个关系。这个很多同学是想不到的,但是如果你听了咱们的课会范特祸福方程,那你想一想吧,这个三四一五九一五三七二 二四七六五都是啥?都是负的 r 分之德特 h。 好吧,那现在问你,德特 h 二和德特 h 三笔直的范围,这玩意就是负的 r 分之德特 h 二,这玩意是负的 r 分之德特 h 三。那同学们想一想, r 是一个常数,你直接一五 三七二除以二四七六五是不是就等于负,而负而全约掉就等于 that h 二除以 that h 三。所以现在人家不管是很多高考题还是模考题,他都是用范特护肤方成为背景给你出题的。用普通的方法当然能做,但是想起来就比较麻烦。如果说你知道 到了高考人家出题的背景,那相当就是降维打击吗?这题就非常的好做了。好,那你看这个值很明显是大于零小于二的呀,是不是同学们答案是不是直接选择 c 选项? 范特护肤方程的第一种应用就是去判断一下反应的西方热以及含变绝对值的大小。那在高考中,还有平时的模考中,还有另一种平衡的证明题也要用到范特护肤方程,这种题可能很多同学很头疼, 给你一个图,多个反应对吧?给你一个图,然后又给你一个方程式,让你求出这个方程式的平衡长数表达式以后,让你去证明这个反应到底是吸热还是放热。全国卷这个题当年的话,反正很多同学感觉比较难啊。 给的这个标准答案的话,很多同学反馈说是不知道人家为什么会想到这里,对吧?各种算什么? log k p 二, 嗯,第一个温度的 log kpr, 第二个温度的 log kpr, 然后不停的去比,不容易想到,对吧?但是如果你知道范特护肤方程,你其实就已经知道了,人家到底让你怎么答题,你往里面套就可以了。 首先介绍一下范特霍夫方程的变形,其实就是把一个反应不同温度的两个范特霍夫方程写出来,写出来以后做一个笔直,就可以得到这么一个式子,那当然这个式子里的这种玩意咱们都不用管,对吧?所以咱们直接写出高考中 那可能用到的,你就把什么标准平衡常数直接写成跨越平衡常数就行了,这玩意就写成含面就可以了,对吧?那就得到 loin k 二 除以 k 一等于二分之负, that h 乘以 t 二分之一,减 t 一分之一。 有个细节需要注意,两个范特霍霍方程你应该带入的是同一个反应在两种温度下的罕变,对吧?那做笔直以后,这里最后写的这玩意其实叫做平均标准摩尔函, 叫平均标准摩尔。汗,那咱们高考里面的话,大家就把这个玩意你也不用管,就直接写成 dh 就行了,那这个 dh 你也不用管数值,你就只用管正负就行了,好吧,只用管正负就行了,那一个反应他到底是吸热反应还是放热反应?这玩意是固定的呀,对吧? 你就算在不同温度下带入范特霍夫方程,那你该是吸热反应的永远是吸热反应,该是放热,永远是放热,是这样吧,哎,咱们就只用灌 德特 h 的正负即可。数值管都不用管,那你一开始这个反应是个吸热反应,你就算带了两个不同温度下的范特或负方程进去,那你这个德特 h 就这里最终是不是还是大于零呢?这个东西咱们在这里只用管正负, 好吧?哎,只用管正负,这个是不就是常数?这是两种温度的平衡常数,这是两种不同的温度, ok 吧?那利用这个方程啊,其实可以去判断反应的西方热。 比如说知道某一个反应在 t 一 t 二温度下,化学平衡常数分别是 k 一和 k 二,而是一个常数啊,直接可以推断函变的正负。 比如我知道了 k 一大于 k 二, t 一大于 t 二,那么 k 二除以 k 一,它是不是就是小于一的? 那烙印以后是不是小于零?这个玩意小于零,那这个玩意小于零以后,说明后边这部分小于零,后边这部分小于零。来看一下,由于 t 一大于 t 二,所以 t 二分之一减 t 一分之一大于零,这部分 大于零的,但是这部分是小于零的,是不是可以推出来反应的得 th 必然要大于零,对吧?这个东西啊,其实就给你一个启示, 对于一个反应而言,你只要找准了两个温度以及他们对应的平衡场数,那就可以快速的推出这个反应到底是吸热反应还是放热反应,那当然平时的话,同学们做题也是这个思路,对吧?哎,问一个反应吸放热,那你就先找 两个温度,然后比一下这两个温度平衡常数谁大谁小是不判断西方热,但是到了高考里,人家给你包装一下, 大部分同学就看不出来了,比如说来看一下这个高考真题,全国卷了啊,很多同学可能做过。首先第一个问你,这个玩意 反应分解为一氧化氮和氯气, dh 大于零还是小于零呢?嗯,首先来看一下这个对应的 k p 二斜率是不负的, 正放复吸,对吧?斜率是负的,所以它肯定是吸热,吸热的话的 h 大于零就不用再想了。但是有些同学就是喜欢想啊,就是要看一下随着横坐标的增大可以怎么变,然后慢慢去分析的话,也可以啊,随你变都行的。 反应这个它的 k 等于什么呢?那你注意好,这个反应它其实就是反应一加上反应二是不就可以了,所以这个反应它等于反应加反应二,那它的平衡常数 就等于 k p 一乘以 k p 二,这是最基础的平衡的结论。好吧,接着问你该反应的 that h 大于零还是小于零呢?那这个标准答案的话,就这个样子,很多同学 看了以后就感觉很无语,对吧?啊?当然你数学好的话,细细分析确实能分析的通,但是想把它总结成一个模板,碰到这种题然后就这样做的话,感觉有一点困难,那咱们就可以用范特或负方程,然后给同学们把这个模型总结出来, 你看到了烙印 k 和 t 分之一的图像,让你判断一个反应的西放热,你得想一想范特回复方程,你就相当于把它总结成一种模型,这个做题就很好做了,因为烙印 k 二除以 k 一等于这么一个式子,对吧?那咱们可以由这个式子直接得到罕变的正 负,所以对反应直接开始读图,反应二的话, k 等于 k p 一乘以 k p 二嘛,对吧?当横坐标取二点二的时候,就取个大概就行了。取二点二的时候, k p 一和 k p 二 数值大概就是十的负一点二和十的负二点六,取个大概就行了,好吧,那算出来 k 一是不是就等于十的负三点八?那横坐标等于二点四的时候,咱们再代入一下 大概就行了,好吧,横坐标二点四的时候, k p 一可以读出来大概是十的负零点七, k p 二读个大概啊,大概就是一个十的负三点三,那 k 二是不是也能算出来是十的负四,对吧?这个东西啊,其实就相当于是给同学们一个模型, 并不是说本身有多难,因为你这个标准答案写的我觉得确实有点离谱,不太好,没有必要,对吧?那咱们通过这个模型给同学们总结一下,碰到了烙印 k 和 t 分之一的图像,你就是去找两个温度,就是去算两个温度对应的平衡长数,直接去比得特 h, 好吧。 所以 k 二就直接等于十的负四,来对比一下, t 一 是十的负三点八, t 二是十的负四,那 t 一和 t 二相比呢? t 一的数值是不是小于 t 二?二点二小于二点四吗? 对吧?但是这玩意是 t 分之一的数值好吧,也就是 t 一分之一等于二点二,怕有些同学数学不太好写详细一点, t 二分之一等于二点四,所以 t 一是不是大于 t 二, 这总没问题吧?好,所以 t 一大于 t 二,而且 k 一大于 k 二,那这时候其实不用范特或夫,同学们是不是都能证明了,由于 t 一大于 t 二,就是 t 二到 t 一升温, 升温平衡长数增大,所以反应为吸热反应,或者就说降低温度,平衡长处减小,那降温平衡逆向移动吧,逆向放热,正向吸热都行,是不能推出来这个反应,肯定是吸热的 啊,很多同学的话,可能就是按照大多数地方,教父啊给的答案是这个东西,你如果按这个答案去理解这个题的话,我觉得这个可能下次碰到一个 差不多相同的题,你可能自己又蒙了,对吧?唠个来唠个去,弄来弄去很麻烦,没有必要,对吧?同学们,以后碰到了这种题,那咱 咱们就去想一想犯错后果方程,想一想最基础的,其实你就是确定两个温度,确定两个平衡场数,是不是就能得到最终的结果。那高考的话,人家画图都是比较标准的啊,就算没有这个横纵坐标 对吧?你自己差不多列个数据也是完全 ok 的,对不对?你用尺子呀,尺子量一下呗,尺子量多少数值就是多少,高考人家做图很标准的,所以说这个 k 你是肯定可以算出来了,比如说就是没有这些数据,对吧?那温度大小你起码知道吗?你就拿尺子量, 你挑两个温度,这两个地方尺子量出来纵坐标乘一下,这两个地方量出来纵坐标是多少?转化成 k 乘一下是不都可以啊?完全 ok 啊,同学们。所以以后碰到这种平衡的证明题,我相信你肯定就会做了, 你看一下咱们数学的答案啊,和这种答案哪一种好呢?很明显是后者,相信你用这种方法去思考这种题的话,你是可以学会这种题的, 对吧?啊?也就是说,其实拿这个模型啊,就给同学们说了,这种证明题你就找两个温度,找两个 k 就比就行了,本质还是这样子啊,那具体如果没有中坐标的话,就直接直接拿尺子量就可以,那当然咱们也可以带到范特护肤方程里去验证一下。你看 浪引 k 二比 k 一, k 二的话,它是小于 k 一的十的负四和十的负三点八吗? k 二小于 k 一,所以这样一除的话,这个东西小于一浪引后是不是小于零?这个玩意小于零就说明 右边这个整体也是小于零的。好,接着代入 t 二分之一和 t 一分之一, t 二分之一和 t 一分之一,咱们 分别选的是二点二和二点四,对吧? t 二分之一数值是二点四, t 一分之一是二点二啊,直接代入。有些同学啊,你们一定要仔细一点,别带个二点四分之一和二点二分之一。好家伙,你看清楚,人家这个 t 分之一的数值就是二点二和二点四,所以 t 二是二点四, t 一分之一是二点二,那这样一减的话,这个东西大于零,而是长数大于零的,那 that h 是不是只能大于零? 这就是奋斗护肤方程在高考以及模考中的应用。第一个结论,同学们要记清楚 lionk 和 t 分之一的图像, 你是可以直接通过斜率读出这个反应到底是吸热还是放热反应,同时读出它含变的绝对值,到底谁大谁小都是根据斜率看的。第二种 情况的话,就这种现在比较流行的平衡证明题,对吧?啊?这个很多地方反正这种题出来以后给的答案全是这个样子,没有必要对吧?你就想一想,如果能记住这个方程的话,记一下,那记不住的话你就清楚记清楚啊, 咱们不管碰到哪种题,永远回归到最基础的,别搞什么 log 这种花里胡哨的啊,你自己考场上也想不来,你就记清楚,咱们就挑两个点,找出这两个点的温度, 对吧?再算出这个两个点对应的平衡长数,然后比大小就行了。那这一说如果没有纵坐标的话,你就可以直接说,比如说 t 的时候,由图中可知 啊, k 一大于 k 二,对吧?就可以了啊,就可以了。那你知道了温度,知道了 k 之间的大小,那最终反应的席放热是不是就出来了? ok 啊。
213化学超人本人账号 01:41查看AI文稿AI文稿
01:41查看AI文稿AI文稿每天一分钟,连着带你过基础!今天我们讲物理化学化学平衡这一章的范特霍夫等文。方程与反应方向的判断和各种因素对平衡的影响。 哈喽哈喽哈喽,我是眼哥。今天我们讲化学平衡的最后两个考点。首先是范特或夫等位方程与反应方向的判断。 对于范特和夫等位方程与反应方向的判断,我们用德塔尔 g m 等于德塔尔 g m, c 塔加上 r t, l, n, q p 来进行判断。当 casit 等于 q p 时,德塔 r g m 等于零反应达平衡。当 casit 大于 q p 时,德塔 r g m 小于零,反应向右进行。当 casit 小于 q p 时,德塔 r g m 大于零,反应向左进行。 其中 qp 为标准增压商。范特霍夫定温方程对理想气体、真实气体或对有纯液体、纯柱体参与的反应以及真实液态混合物、真实溶液中的反应都是适用的。但是注意在上述 不同场合下臭屁像的差异就 ok 了。然后是各种因素对平衡的影响,你只需要记住恋哥总结的这几句话就可以了。一、温度对平衡的影响吸热反应升温反应正向移动。放热反应、降温反应正向移动。 二、压力对平衡的影响压力增加,反映像气体分子数减少的方向移动。压力减小,反映像气体分子数增加的方向移动。三、惰性气体的影响横溶条件下加入惰性气体反应不移动。横压条件下加入惰性气体反映像气体分子数增加的方向移动。 ok 了! 化学平衡这一章实际上不难,很多同学是被书上的这种符号吓到了,实际上跟着脸哥学下来,是不是觉得这一章也不过如此?哈哈哈哈,如果想更加系统的学习专业课,记得私信我哦! 海盗化学跟脸哥上来小 case 持续关注我,我会在下一期视频给大家讲解更多专业海盗化学相关专业的考研干货,记得点赞加关注哦!
70脸哥考研 00:30
00:30 01:48查看AI文稿AI文稿
01:48查看AI文稿AI文稿每天一分钟,免费带你若基础,今天我们讲物理、化学、范特霍夫等量方程和标准平常常数的计算。 哈喽哈喽哈喽,我是点歌,这个系列好久没有争亲了,今天正式回归。今天我们先讲范特霍夫等亚方程。对于范特霍夫等亚方程,主要是用来描述平常常数有温度的关系。对于范特霍夫等亚方程,它主要有三种不同形式,分别是威分式、积分式和不定积分式。其中最重要的就是积分式一定要把它背下来,考试基本上都是考积分式。 然后是标准平常常数的计算。对于标准平常常数的计算,我们是基于 datalgmclt 等于副的 lgmkc, 他只要求出的 datalgmct 就可以求出 that。 而多套 rgmcat 也是化学平衡和热血平衡的桥梁。多套二 gmcat, 我们可以用热力学的方式求出,然后把它的值带到多套二 gmcat 等于 的 rtlkct 中,就可以求出 kct 的值。对于 dataargmcta, 我们也可以用 datalsmcta 和 datasmcta 来进行计算。如果我们要求的不是二百九十八点一五看一下的 datas 和 datas, 那么我们就要通过基尔护肤定律 来求出当前温度的 dotas 和 dotas, 然后因为 dota g 等于 dotas 减去 t 的 dotas, 那么我们就可以求出当前温度的 doctorgmctt, 然后把 doctor rgmcit 代入 doctrlgmcit 等于富的 ict, 从而求出 cat。 在这里你一定要区分吉尔护肤定律和范特霍夫等亚方程,这两个在叫法上非常容易弄混。这两个考点书上讲的非常复杂,但是根本没有必要按书上的来,只要把脸上说的这几个中式记住就 ok 啦! nice 如果想增加系统的学习专业课,记得私信我哦!海南化学跟缅哥上班小 case 持续关注我,我会在下一次视频里为大家讲解更多专用海南化学乡村专业的考研干货,记得点赞加关注哦!
51脸哥考研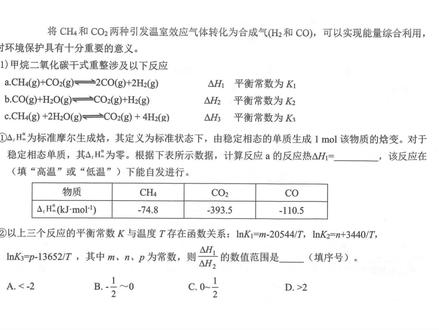 16:49查看AI文稿AI文稿
16:49查看AI文稿AI文稿将甲烷和二氧化碳两种引发温室效应的气体转化为合成器天气和一氧化碳可以实现能量的综合利用,对环境的保护有非常重要的意义。 甲完二氧化碳干式重整设计,以下反应又告诉你了。标准摩尔生成函就定义是由稳定向太的单质生成一抹,而该物质的含变,这是标准摩尔生成函。 对于稳定的单只向太,他的标准摩尔生成还为零,就比如说这里的氢气,他本来就是单只了,那他的标准摩尔生成函就是零, 那一氧化碳的标准摩尔生成函就是稳定的单制,比如说碳单制扔成一模二,一氧化碳的一个含变啊,那就叫做一氧化碳的标准摩尔生成函。 根据下表中的数据计算反应 a 的反应热 at h e 等于多少, 那大家可以从盖斯定律的角度,然后去思考计算得分 h 一啊。也可以直接就是把这种标准摩尔生成函,你就直接可以看作这几个物质具有的能量,然后用生成物能量减反应物能量,然后去算就行。 这个算下结果都是一样的啊,没有什么区别。那比如咱们就直接来计算一下吧,你看 甲完标准摩尔生根还是负的七十四点八,二氧化碳是负三九三点五, 一氧化碳是负一零点五,经济是零,那咱们直接 二乘以负一一零点五就生成。无能量减去反应无能量减反应能,无能量的话相当于加七十四点八,再加上一个三九三点五,又得到最终的答案,这个答案的话就等于正的 二百四十七点三啊,所以特特约吃一等于正的二百四十七点三千娇美摩尔。 以上三个反应的平衡常数 k 和 t 存在函数关系啊,给你了烙印 k 一,烙印 k 二,烙印 k 三的一个关系, 其中 m n p 为长数。问你得退 h 一,不得退 h 二,数值范围是什么?那拿到这个题啊,可能可能懵了, 这个公式的话,其实是大学里面的一个公式啊,你如果说没有学过这个方程的话,你也不会用它,你也不会用它,但是咱们可以用高中的方法把它轻松的解决掉。那大家看, 问你的是德特 h 一和德特 a 二之间的关系,但是给你的是 k 一, k 二 k 三给你了 k, 你能知道什么呢?同学们,我们来想,在你升高温度的时候,烙印 k 一怎么变? 升高温度这个值是不是在减小,这个是减小呢? m 这个长数减去的数值,他在变小,那整体浪一 k, 这个数值是不是在变大?这个数学问大家应该都没问题啊,应该都没问题吧,这个其实就相当于初中数学了啊。这个温度升高, 负的二零五四四除以 t 这一部分是不是减小? m 减去一个减小的数,他的数值是不是在增大,对吧?烙印 k 就在增大,所以说升高温度 k 一增大,升温可以增大,升温为正向进行,因此 na h 一可以判断出来是吸热反应啊,你可以通过这个方程来判断吸放热。 同理,德特 h 二的话,升温升温,你会发现这个值在减小,但是你此时烙印 k 二等于 n 加上一个减小的数,那这个烙印 k 二是不是也在减小? k 二就在减小,对于升温, k 二减小,升温,第二个方式是逆向移动, k 二减小 正为逆向移动,逆向行者正向放着,得退一尺二,就小于零。实际上你发现,就前面的这个号啊,如果是负号,那得退一尺大于零,如果是正号,他得退一尺小于零。比如说这个 在分析面,这个温度升高,那这个值就减小, p 减去一个,减小的值呢?整体就增大。所以升温配三增大,升温平衡正向进行,向吸热方向进行,那它 h 三大于零。 我们再来看一下,你判断出来德特 h 一,德特 h 二得,这是 h 三以后。那么这个德特 h 一比德特 h 二应该怎么去计算呢? 怎么样找到 ththth 的关系?同学们,盖茨定律,好吧,哎,所以说考来考去其实还是落脚在最基础的地方,你的基础只要扎实啊,这个题其实不是什么特别难的事情。好,那我们发现 thth 一 和得退一尺二,得退一尺三之间的关系,这是一个假弯。好,那就一倍的得退一尺一,加上 要有两个水,那加上二倍的 th h 二,那你有没有发现正好等于 thth 三啊?找到这个关系以后啊,那 thth 一是不是可以求出等于二等于这个 thth 三减去二倍的 thth 三, 好带入德特 h 三,德特 h 一啊,等于德特 h 三减去二倍的德特意叉,再除以德特意叉把带入这个式子啊,问你这个,那就等于德特 h 三 除以得退一叉二减去一个二,得退一尺三,除以得退一尺二,得退一尺三大于零,得退一叉二小于零。所以说这个除完以后,这个值是小于零的, 那前面这个数小于零,再加上负二,是不是比负二要更小了?因此这个值小于二也就选出来了, ok 吧。啊,那这个的话,其实也是后续大家考试的 一个方向,很有可能会出现了啊,很有可能会出现 甲烷的水蒸气重整,涉及以下反应,在一密闭容器中通入一模甲丸和三模水蒸气,发生甲丸的水蒸气重整反应,压强为 p 零。铅帕分别在加氧化钙和不加氧化钙的时候,平衡体系中清气的物质的量随温度变化,如图一所示, 温度低于七百度,加入氧化钙可以提高混合器清气的含量。为什么?那当平衡了以后,对吧?质量反应平衡以后,你加入氧化钙,氢气能增多,为啥呢?氧化钙可以反映二氧化碳啊,对吧?哎,原因是氧化钙反应 二氧化碳,是反应二 平衡 正向移动 啊,是反应二平衡正向移动,清气增多, 五百度的时候反应相同的时间。注意好,这里是在一定时间内去测转化率了,如图二所示,你看,随着压强的增大,如果平衡了以后啊,你不断的增加压强,平衡了以后,你加压反应是不会 逆向移动,让甲烷的转化率减小,对吧?但是一开始的时候,你压强增大,他的转化率不停在增大,为啥呢? 因为一开始的时候,你的压强比较小,他的反应速率比较慢,在你给的这一定时间内,相同时间内啊,在你给的这 一定时间内,他没有达到平衡,那么那当到 f 点以后,那就你的压强也就比较合适了,这时候 在你所给的时间内恰好达到了平衡。达到平衡以后,你继续加压,那继续加压,反应速率是不继续增大,反正你肯定是能达到平衡,对吧?后边你当然更能达到平衡了,因为你的速度更快了。那你继续加压的话,平衡是不是逆向移动,他的转化率就开始不停的下降? ok, 那问你易点和 g 点的一个浓度大小关系啊?题目没有考你这个分析,但是就给大家说一下,易点和 g 点甲完的转化率一样,那甲完最终剩余的物质的量肯定也是一样的,但是 怎么增大压强呢?如何加压呢?哎,咱们加压如果影响平衡移动,那是不是就缩小容器体积啊?对吧?那是改变容器体积了啊。 所以说你在加压的过程中,缩小容器体积,那物质量一样,压强越大,你怎么让它压强大呢?是不是就缩小容器体积?因为你没有额外冲入什么反应物,反应物是恒定的,对吧?所以你缩小容器体积,体积小了,物质的量一点,这点一样,但这点体积更小,浓度就会更大。 此温度下,反应二的分压平衡常数 tp 为多少?这又是一个多重平衡?那其实 都是送分了啊,咱们可以列两次三段式解决,那解决的时候先做第一个反应的,再做第二个反应的。来,我们来看一下 一猫甲丸和三猫水一三零零,对吧?假设甲丸反应 xx, 那就反应 x, 这反应三 x, 这剩余一减 x, 这剩余三减 x, 这剩余 x, 这剩余三 x, 这是第一个放中式。第二个就是一氧化碳和水 生成二氧化碳和氢气,那这种气咱们做的时候写出第一个反应方程式,它的三段式以后,然后第二个反应是在第一个反应的基础上继续进行, 此时那一氧化碳有多少呢?一氧化碳是不是就他的量?咱们第一次算一下,一氧化碳是不是 x, 水的话是不是剩下三减 x, 第一个反应没有生成二氧化碳,第一个反应生成氢气是三 x, 这是第一个反应啊。 结束以后我给的一个一氧化碳、水和清气的量,咱们假设反应了完, 嗯,一氧化碳反应的完好,那时候得到,这是 x 减完,这是三减 x 减完,这是完,这是三 x 加完,那就得到了个误式的一个最终的量 啊。由于人家告诉你了,这个转化率 p 零啊,压强 p 零,转化率是百分之六十, 对吧?啊,那所以这个题可能还要更简单一点啊,这个如果告诉你转化率是百分之六十的话,那甲完是不是就反应了零点六,那这个 x 就是零点六啊,那咱们可以直接带入吧。 如果题目复杂一点的话,就是咱们刚才这种写法啊,人家可能会给你一些数据,你再去解除 xy, 但这个题他 x 直接给你了,就比较简单,零点六,零点六, 零点六,一点八,这剩余的是零点四,二点四,零点六,一点八, 一氧化碳的话,第一次是零点六,水的话是二点四,二氧化碳是零。第一个反应一个反应没生成二氧化碳啊,氢气是一点八, 假设这个反应是歪,那一氧化碳是零点六减歪, 水是二点四,减完二氧化碳剩余白硬气是一点八,加完题目这又告诉你了,最终清气五百度,清气物质的量是二点一。 题目告诉你了,五百度的时候天气是二点一。呃,一点八,加崴,等二点一,崴是不算出来,等于零点三,直接带入崴, 零点三,零点三,零点三,零点三。那这个最后的结果,一氧化碳剩余零点三,对,剩余二点一,二氧化碳是零点三,氢气是二点一。好,我们要算二反应的一个分压平衡常数,对吧?那一氧化碳最重的量,那就是 零点三,接着是水最终剩余的量,二点 二氧化碳最终剩余的量, 第一个反应没生成,第二按宽带,第二个反应中是不是就是零点三,然后接着清气的话,最终的量 啊?通过刚才烈士兴起,最终是不是也是二点一? ok, 接着咱们去把这个分压平衡常数算出来就可以啊, 因为他是前后你发现没?反应二是前后计量数相等的一个反应。在这顺便,呃,大家如果单纯的去算分压平衡常数,是不是得算量分数?比如说一氧化碳等物质的量,零点三,除以总物质的量,是他们各自的量分数,对吧?各比如说二,一氧化碳量,分数乘一个 p 零, 这算下是一氧化碳的一个分压啊,那计算的时候那就是清晰的一个量分数, 或者你用依塔来表示也行,都行啊。轻气的一个量分数有二点一,除以总的物质的量能以 p 零,这是轻气的分压再乘以二氧化碳的量,分数再乘一个 p 零,二氧化碳的分压再除以 一氧化碳的量,分数乘以总压,这是一氧化碳分压,再除以水的一个量分数再乘一个皮零,这水的分压是算最终结果。呃,这个大家喜欢这样 就这样算,那顺便给大家说一个小结论啊,就是如果反应前后剂量数相等的时候啊,对于反应前后气体剂量数相等的反应,他的分压平衡常数啊,直接就等于 用物质的量去列。这个平衡常数表达式什么意思啊?就是 k 直接等于星期物质的量数二点一,直接等于二点一,乘以二氧化碳的量零点三,除以一氧化碳的量零点三, 再除以水的物质量二点一。最后答案等于一,可以直接算出答案。这是一个小推论啊,那大家也可以自己去验证一下,可以让你把这个十字一摆 也能看得出来啊。这个十字一百 p 零是不是约没了,对吧?那物质的量分数等于他们各自的物质的量除以总的物质的量,那总的物质的量一样是不是也可以约掉?其实这个 ap 就等 物质的量啊,就生成物物质的量的密次方,所以反应物物质的量的密次方。 甲烷蒸汽重整工业,嗯,面临着大量的碳排放,然后让你写这个电机发生的电机方式,那这个给的比较简单,进去的是甲烷 啊,同时氧离子也参与了反应, 生成物给你的是清气二氧化碳,这生成物反应我都给你了,这没啥难度啊。 好,咱们来看一下甲完的碳,这个是负四, 清元素的话是正一啊,甲完碳是肤色,清元素是正一。好,那在这咱们看一下并价碳后边 这次变到了二氧化碳的正四,碳数升八轻,正一变成了零价的轻,每一个轻降一,那有四个轻,是不是降四?所以一个甲完总共会升四,一个甲完总共升四架,是不是就会失去四个电子 啊?失去四个电子,那失去四个电子以后,左右如果要电荷守恒,右边你生成二氧化碳和氢气是零电荷,你如果要求电荷守恒, 左边是不是得有四个负电盒?中和你失去的四个正电盒,对吧?哎,中和你失失去四个电子以后所带的四个正电盒,所以这个氧离子的话就是二 啊,氧离子就是二,那接着的话,这个方程式就好像就已经平了啊,两个氢气对吧?氢气前面也是二 啊,就是假弯。 首先判断出来他是不是总共升了四架,失去四个垫子, 接着要生成后边的二氧化碳和氢气,要电荷守恒,那不能带电,你是不是得加上四个负电荷?题目也给你说了,用氧离子补电荷,接着生成二氧化碳,如何两个氢气 两分到手啊?有这个平衡的题,这个平衡题唯一一个难一点点呢,就是这个。 这个很多同学可能没见过啊,所以说你不能单纯的只做高考真题,每年他的高考真题都会有一些比较新的东西出现,那如果说你没有见过,那说实在的,指望你上考场上直接想出来,那基本上很难很难了。 所以说大家平时也是要比较好的,这种联考的题啊,一定要好好做一下。
28化学超人本人账号 03:03
03:03 28:26查看AI文稿AI文稿
28:26查看AI文稿AI文稿高考化学反应原理的真题中,越来越多的题目以阿伦尼乌斯公式以及范特霍夫方程为背景出题。范特霍夫方程同学们可能会感觉陌生一些,这节课带同学们学习范特霍夫方程在高考中的应用。 范特霍夫方程描述的是化学平衡长数和 t 分之一,这个 t 就是温度啊,和 t 分之一的关系。他的图像和阿伦尼乌斯公式描述的图像非常的相像,那如果阿伦尼乌斯公式没有什么基础的同学,可以去看一下咱们的 一轮课程,就在一站的收藏夹一轮的课程,一轮课程里对阿伦尼乌斯公式有非常详细的讲解,阿伦尼乌斯公式看清楚,描述的是速率长数和替分之一的关系。 范特霍夫是化学平衡长数和 t 分之一的关系。速率长数和化学平衡长数是不同的。 阿伦尼乌斯公式里面有个重要的结论啊,你看这就是速率长数了,和替分之一的关系。注意好阿伦尼乌斯公式的相关结论。烙印速率长数和替分之一的图像中,那这个直线他的斜率如果越大,对应的反应活化能越高。 那比如说一二三这三条线谁的斜率最大呢?很明显,三的话斜率最大吗?所以他的活化能是最高的。这个在考试中经常会考到, 范特或副方程也有类似的结论。首先认识一下这个方程, k c, 他指的是标准平衡常数,这个东西叫做标准摩尔函变,那实际 上高中是不学他们的,展现到高考上的话,其实这个 k c 塔你就直接看成平衡常数也行。实际上在高考题中,比如说二一年考出来的全国卷高考题里面,纵坐标他并没有写什么 loin k c 塔,他就直接写的是 loin k, 直接写成了化学平衡常数啊。所以说这玩意你就看成化学平衡常数,然后标准摩尔含变的话,就直接看成正常的含变就行了,就直接就写成德特 h 即可。 那至于后边这部分的话,跟同学没什么关系啊, r 是一个常数, r 分之这个玩意咱们就直接看成 x 即可啊,直接就看成一个 x 即可啊,就跟咱们没有什么太大的关系。前面的这个 r 也是一个常数,所以范特护肤方程咱们直接可以看成这种 十字,那在高考出题里面,他出现的也是这种十字啊,都是烙印 k 等于 r 分之负,德特 h 乘以 t 分之一加 x。 那注意好,范特霍夫方程研究的是 k 和 t 分之一的关系,纵坐标是烙印 k 横坐标, 这是横坐标啊,是 t 分之一,那也就是说又变成了 y 等于 k s 加 b 的一个形式,对吧?那这玩意儿负的二分之 that h 是不是就是斜率? 直线的斜率这个玩意它就是洁具啊,洁具的话咱们不考,所以你主要要记清楚,化学平衡常数和 t 分之一的图像中,负的 r 分之的 th 就是直线的斜率。那我们来看 一下具体的应用。烙印平衡长数和 t 分之一的图像是一条直线,相信这种图像同学们已经见了很多次了,见过的同学可以在弹幕上打个一, 非常的常靠。那首先由于刚才已经给同学们说了,这种图像它的斜率就是负的, that h 除以 r, 那考试中经常就是问你,比如说给你这两条线,问你这两个线所对应的反应是吸热还是放热?那普通的做法同学们肯定也都知道啊,就比如说,你看,随着横坐标的增大, 横坐标的增大,其实就是温度的降低,随着温度的降低,这两条线他的 k 是不是也在降低,说明降低温度平衡,逆向移动,那降低温度向放热方向移动,逆向放热,正向是不是吸热?哎,就能推出来这两 两个反应啊,他肯定都是吸热反应, ok 吧?啊?这两个反应肯定就是吸热反应。由于斜率是负的, r 分之的 th, 所以对于吸热反应而言,这个斜率他是不是小于零啊? 对吧?这个玩意斜率是不是小于零?得特 h 是大于零的,而这个长数也是大于零的,那前面加个负号就是小于零的,所以吸热反应斜率它是小于零的,那对于放热反应而言,得特 h 如果小于零了, 那这里小于零,而是大于零的,前面再加个负号,是不是就斜率就大于零了?所以对于吸热反应而言,斜率它是负的。对于放热反应而言,斜率是正的。所以首先我们可以通过 这些线的斜率快速判断这个反应到底是吸热还是放热,那口诀的话就是正放复吸 斜率,如果是正的反应,就是放热斜率,如果是负的,比如这两个斜率是负的,那他就是吸热反应。那当然普通的判断方法也是可以的。你如果不想记那么多,你看 随着横坐标的增大, t 分之一增大,实际上温度是不是在减小?随着温度的减小,平衡长数是不是越来越小了?说明降温平衡逆向移动,逆向放热,正向吸热,是不是也能判断出来得到一尺大于零?但是有时候你针对这种图像记一下这个结论,可以极大地缩短你的做题时间。 那除了这点,就是你根据斜率可以判断西放热以外,我们还能判断西放热也就是这个寒 变的大小。那一般来说是判断含变绝对值的大小啊,因为有些反应的话,它是吸热的,德特 h 是大于零的,有些反应的话,它是放热的,德特 h 是小于零的。咱们判断的是德特 h 绝对值的大小。 那判断的时候怎么看呢?那你想一想,负的二分之得特 h, 这是斜率啊,你给斜率加一个绝对值是啥?是不是二分之得特 h? 那同学们思考一个问题, r 分之 that h 如果越大的话, 就是斜率的绝对值,越大的话,那对应这个 that h 的绝对值是不是一定也越大?我再说一遍啊,这是个简单的数学问题。首先斜率是这玩意儿,你给斜率 加一个绝对值,是不是相当于就是给上边的这个 that h 加了个绝对值?这个负号是不是就不用管了?因为 r 一定是个正数,对吧?所以斜率的绝对值就等于他。那你想一想,斜率越大的话,对应的 that h 的绝对值是不是一定越大? 所以这个结论也需要记住啊,就是斜率越大,代表含变的绝对值越大。那我们来看一下这两条线,你能分辨的出来哪一个反应含变更大一点吗? 如果没有给你标,那也可以轻松的找出来。由于这条线斜率更大,所以它含变的绝对值更大,又由于正放负息斜率是负的, 所以它是一个吸热反应,对吧?正放复吸斜律为负, 那就是吸热反应。吸热反应的话,含变本来就是大于零的,对吧?那这条线含变的绝对是更大。由于含变本来就是大于零的,那 that h 本来就是大于零的嘛?那就证明这条线的 that h 是不是也就越大一点? ok 啊!首先记清楚这几个结论,咱们先来实战几道经典的模拟题, 接着再来做高考真题啊。比如说恒温恒融的条件下,像密闭容器充入一定量的 x, 发生两个反应,让你画一下这个能量图,看一下能量图和这个曲线最接近的是谁,能不能快速做出来呢?可以暂停一下,同学们自己做一下啊。实际上,根据咱们讲的结论, 那既然它是烙印平衡常数和 t 分之一图像的关系,根据正放复析图像斜律,它都是负的,所以 这两个反应都是吸热反应,对不对?那这两个反应都是吸热反应的话,这两个反应的能量来看, x 能量是不是小于 y, y 的能量是不是小于 z? 那你来看一下,符合能量关系的是不是只有 a, x 能量是不是小于 y, y 的能量是不是小于 z? ok 吧,直接选出 a 选项,那有些同学可能又会有疑问,这道题是正好只有 a 选项满足了, x 到 y, y 到 z 全是吸热反应,那如果人家这个题还有一个图也是这两个反应都是吸热的过程呢?到底选谁? 比如说再给同学们出一道题来看, x 到 y, y 到 z 是不是也是吸热反应呢?这两个图 如果对比的话,哪个正确呢?其实还是可以看因为斜率,反应二的斜率是不是更大一点,所以反应二德特 h 的绝对值更大一点,对吧?所以反应二的德特 h 绝对值大于反应一的德特 h 绝对值。那我们来看一下, 来看这个图,反应一得特 h 的绝对值是不这么多?反应二得特 h 的绝对值是不这么多。那这个图的话,反应一得特 h 绝对值是不大于反应二的,就这个得特 h, 其实就两个物质的能量差吗? 是不是?那你说反应一的绝对值是不是就 x 到 y 的能量差,对吧?就这一段,很明显,这个图的话,反应一 that h 的绝对值是不是要更大一点?但是图像中 展现出来的是反应二的 that h 的绝对值要更大,那你来看这个图,这是反应一 that h 绝对值,对吧? 这是反应二 that h 绝对值很明显,反应二 that h 绝对值数更大一点,因此 a 选项正确。 再来看一道题,反应一二三给你,然后给的是烙印平衡长数和 t 分之一的图像,问你反应二对应的直线应该是谁?反应二来看是一个吸热反应啊,对吧?就不用再分析了,或者你喜欢什么,随着横坐标的增大,温度在减小, k 怎么怎么变? 那你最后可以拿这种分析的过程是不是给自己考试题做一个验算,对吧?那如果说直接碰到了这种模型的话,那咱们就直接套结论了,正放负 息,根据正放复息,由于反应二 that h 是正的, 它是一个吸热的反应,对吧?那它的斜率就是负的,来看一下 a 和 b 谁斜率是负的,是不是 b, 直接写 b 是不是就行了? 正放负吸,这个指的是放热,这个指的是吸热啊,正负指的是斜率,那反应二的话,它是一个吸热的过程,那斜率就是负的吧?这种图对吧?直接写 b 即可。接着让你绘制反应三的图像。 反应三首先是不是得算一下 deta h? 那咱们来看一下计算过程啊。首先根据 get 定律,一减二可以得到反应三,反应三呢? deta h 是负的,八十九,反应三也是放热反应,根据正放 负西放热反应,它的斜率是不是应该为正直?哎,所以它的斜率要画的话肯定是正的,那画的时候就存在一个问题,它的斜率到底是比 a 这条线大,还是要比 a 这条线小呢?那这道模考题考出来的时候也是连考题啊,很多同学可能就蒙了, 其实直接套咱们讲的结论,也不用说是像标准答案那么复杂的证明过程,对吧?咱们直接套结论,斜率越大, that h 的绝对值是不是越大?由于你注意好, that h 三的绝对值是八十九, 是这样吧。那你 a 这条线的话,对应的是反应一,反应一的绝对值是四十九,得特 h 绝对值是四十九,那所以反应一得特 h 的绝对值小于反应三得特 h 的绝对值,绝对值越大,斜率越大嘛。所以说反应三的斜率是不是肯定得大一点?图像是不是应该这样画? ok 吧,同学们,图像应该这样画,那标准答案的证明的话,其实就是利用 get 定律之间的加减去证明的,还是比较费时间的,对吧?也是可以证的啊。嗯,但是如果说你直接知道结论的话,那相当于这这道题的话,那可能就是个 十秒钟,是不是就写完了,会给你节省很多时间啊,毕竟这也是热门题型。好,那咱们再来看一道非常经典的联考题, 好多同学都被这个题恶心过。首先啊,给你三个反应,又给你了函数关系,那你看这个函数关系是不是长得很像,是不是就是范特霍夫方程的变形? long k 等于 t 分之一个数值,再加 x, 这个是洁具。那 这个玩意是谁呢?是斜率啊,对不对?画烙印 k 和 t 分之一的图像,那这个三四五一九就是斜率,斜率是咋表示的来着?负的二分之得特 h, 所以这个玩意是负的二分之得特 h 一, 这个玩意儿是负的二分之得特 h 二,这个玩意儿是负的二分之得特 h 三, ok 吧,哎,这样子咱们就知道了,其实这三个数值啊,和 that h 是有关系的,那 r 是个常数啊,对吧?你是不是可以根据这三个数值直接去求出啊? that h 一, that h 二, that h 三,谁大谁小, 是这样吧,同学们,而且你还可以看出来 dot h 一, dot h 二, dot h 三的正负,那同学们来 说,这三个反应是放着还是吸着反应啊?由于 r 是一个正的常数,对吧?那你说负的 r 分之得特 h 一得特二 h 二得特 h 三都是大于零的,那得特 h 是不是必然是小于零的,才能保证这三个东西它是一个正的。常数 是这样的吧,因为比如说三四一五九,它是负的,二分之 deta h 一这个玩意是正的,前面是负的,那这个玩意必须是不是也是负的,整体才能是正的, 对吧?因为三四一五九是个正值啊,所以咱们可以快速的看出来, that h 一, that h 二, that h 三都是小于零的,那反应的活化能呢?就是你用活化能算 that h, 那就 that h 等于正反应活化能,减逆反应活化能, 这是热化学部分的一个小结论,对吧? deh 等于正反应活化能,减逆反应活化能。那现在注意好, deh 都是小于零的呀,正反应活化能是不是肯定要小于逆反应活化能? 是这样吧,这是第一问啊。第二问, that h 二比 that h 三的数值范围是多少?让你选这个东西啊,很多同学的话,考场上确实选不出来,同学们也可以暂停一下,自己尝试着看能不能做出来。 我估计很多同学还是做不出来的啊,因为标准答案的话,他给的过程啊,你看,让你算的是德特 h 二,德特 h 三,对吧?哎,你要把这个德特 h 一和德特 h 二、德特 h 三联系起来,根据德特 h 一效于零,然后再推出德特 h x, 得到 h 三之间的一个关系。这个很多同学是想不到的,但是如果你听了咱们的课会范特祸福方程,那你想一想吧,这个三四一五九一五三七二 二四七六五都是啥?都是负的 r 分之德特 h。 好吧,那现在问你,德特 h 二和德特 h 三笔直的范围,这玩意就是负的 r 分之德特 h 二,这玩意是负的 r 分之德特 h 三。那同学们想一想, r 是一个常数,你直接一五 三七二除以二四七六五是不是就等于负,而负而全约掉就等于 that h 二除以 that h 三。所以现在人家不管是很多高考题还是模考题,他都是用范特护肤方成为背景给你出题的。用普通的方法当然能做,但是想起来就比较麻烦。如果说你知道 到了高考人家出题的背景,那相当就是降维打击吗?这题就非常的好做了。好,那你看这个值很明显是大于零小于二的呀,是不是同学们答案是不是直接选择 c 选项? 范特护肤方程的第一种应用就是去判断一下反应的西方热以及含变绝对值的大小。那在高考中,还有平时的模考中,还有另一种平衡的证明题也要用到范特护肤方程,这种题可能很多同学很头疼, 给你一个图,多个反应对吧?给你一个图,然后又给你一个方程式,让你求出这个方程式的平衡长数表达式以后,让你去证明这个反应到底是吸热还是放热。全国卷这个题当年的话,反正很多同学感觉比较难啊。 给的这个标准答案的话,很多同学反馈说是不知道人家为什么会想到这里,对吧?各种算什么? log k p 二, 嗯,第一个温度的 log kpr, 第二个温度的 log kpr, 然后不停的去比,不容易想到,对吧?但是如果你知道范特护肤方程,你其实就已经知道了,人家到底让你怎么答题,你往里面套就可以了。 首先介绍一下范特霍夫方程的变形,其实就是把一个反应不同温度的两个范特霍夫方程写出来,写出来以后做一个笔直,就可以得到这么一个式子,那当然这个式子里的这种玩意咱们都不用管,对吧?所以咱们直接写出高考中 那可能用到的,你就把什么标准平衡常数直接写成跨越平衡常数就行了,这玩意就写成含面就可以了,对吧?那就得到 loin k 二 除以 k 一等于二分之负, that h 乘以 t 二分之一,减 t 一分之一。 有个细节需要注意,两个范特霍霍方程你应该带入的是同一个反应在两种温度下的罕变,对吧?那做笔直以后,这里最后写的这玩意其实叫做平均标准摩尔函, 叫平均标准摩尔。汗,那咱们高考里面的话,大家就把这个玩意你也不用管,就直接写成 dh 就行了,那这个 dh 你也不用管数值,你就只用管正负就行了,好吧,只用管正负就行了,那一个反应他到底是吸热反应还是放热反应?这玩意是固定的呀,对吧? 你就算在不同温度下带入范特霍夫方程,那你该是吸热反应的永远是吸热反应,该是放热,永远是放热,是这样吧,哎,咱们就只用灌 德特 h 的正负即可。数值管都不用管,那你一开始这个反应是个吸热反应,你就算带了两个不同温度下的范特或负方程进去,那你这个德特 h 就这里最终是不是还是大于零呢?这个东西咱们在这里只用管正负, 好吧?哎,只用管正负,这个是不就是常数?这是两种温度的平衡常数,这是两种不同的温度, ok 吧?那利用这个方程啊,其实可以去判断反应的西方热。 比如说知道某一个反应在 t 一 t 二温度下,化学平衡常数分别是 k 一和 k 二,而是一个常数啊,直接可以推断函变的正负。 比如我知道了 k 一大于 k 二, t 一大于 t 二,那么 k 二除以 k 一,它是不是就是小于一的? 那烙印以后是不是小于零?这个玩意小于零,那这个玩意小于零以后,说明后边这部分小于零,后边这部分小于零。来看一下,由于 t 一大于 t 二,所以 t 二分之一减 t 一分之一大于零,这部分 大于零的,但是这部分是小于零的,是不是可以推出来反应的得 th 必然要大于零,对吧?这个东西啊,其实就给你一个启示, 对于一个反应而言,你只要找准了两个温度以及他们对应的平衡场数,那就可以快速的推出这个反应到底是吸热反应还是放热反应,那当然平时的话,同学们做题也是这个思路,对吧?哎,问一个反应吸放热,那你就先找 两个温度,然后比一下这两个温度平衡常数谁大谁小是不判断西方热,但是到了高考里,人家给你包装一下, 大部分同学就看不出来了,比如说来看一下这个高考真题,全国卷了啊,很多同学可能做过。首先第一个问你,这个玩意 反应分解为一氧化氮和氯气, dh 大于零还是小于零呢?嗯,首先来看一下这个对应的 k p 二斜率是不负的, 正放复吸,对吧?斜率是负的,所以它肯定是吸热,吸热的话的 h 大于零就不用再想了。但是有些同学就是喜欢想啊,就是要看一下随着横坐标的增大可以怎么变,然后慢慢去分析的话,也可以啊,随你变都行的。 反应这个它的 k 等于什么呢?那你注意好,这个反应它其实就是反应一加上反应二是不就可以了,所以这个反应它等于反应加反应二,那它的平衡常数 就等于 k p 一乘以 k p 二,这是最基础的平衡的结论。好吧,接着问你该反应的 that h 大于零还是小于零呢?那这个标准答案的话,就这个样子,很多同学 看了以后就感觉很无语,对吧?啊?当然你数学好的话,细细分析确实能分析的通,但是想把它总结成一个模板,碰到这种题然后就这样做的话,感觉有一点困难,那咱们就可以用范特或负方程,然后给同学们把这个模型总结出来, 你看到了烙印 k 和 t 分之一的图像,让你判断一个反应的西放热,你得想一想范特回复方程,你就相当于把它总结成一种模型,这个做题就很好做了,因为烙印 k 二除以 k 一等于这么一个式子,对吧?那咱们可以由这个式子直接得到罕变的正 负,所以对反应直接开始读图,反应二的话, k 等于 k p 一乘以 k p 二嘛,对吧?当横坐标取二点二的时候,就取个大概就行了。取二点二的时候, k p 一和 k p 二 数值大概就是十的负一点二和十的负二点六,取个大概就行了,好吧,那算出来 k 一是不是就等于十的负三点八?那横坐标等于二点四的时候,咱们再代入一下 大概就行了,好吧,横坐标二点四的时候, k p 一可以读出来大概是十的负零点七, k p 二读个大概啊,大概就是一个十的负三点三,那 k 二是不是也能算出来是十的负四,对吧?这个东西啊,其实就相当于是给同学们一个模型, 并不是说本身有多难,因为你这个标准答案写的我觉得确实有点离谱,不太好,没有必要,对吧?那咱们通过这个模型给同学们总结一下,碰到了烙印 k 和 t 分之一的图像,你就是去找两个温度,就是去算两个温度对应的平衡场数,直接去比得特 h, 好吧。 所以 k 二就直接等于十的负四,来对比一下, t 一 是十的负三点八, t 二是十的负四,那 t 一和 t 二相比呢? t 一的数值是不是小于 t 二?二点二小于二点四吗? 对吧?但是这玩意是 t 分之一的数值好吧,也就是 t 一分之一等于二点二,怕有些同学数学不太好写详细一点, t 二分之一等于二点四,所以 t 一是不是大于 t 二, 这总没问题吧?好,所以 t 一大于 t 二,而且 k 一大于 k 二,那这时候其实不用范特或夫,同学们是不是都能证明了,由于 t 一大于 t 二,就是 t 二到 t 一升温, 升温平衡长数增大,所以反应为吸热反应,或者就说降低温度,平衡长处减小。那降温平衡逆向移动吧,逆向放热,正向吸热都行,是不能推出来这个反应,肯定是吸热的 啊,很多同学的话,可能就是按照大多数地方,教父啊给的答案是这个东西,你如果按这个答案去理解这个题的话,我觉得这个可能下次碰到一个 差不多相同的题,你可能自己又蒙了,对吧?唠个来唠个去,弄来弄去很麻烦,没有必要,对吧?同学们,以后碰到了这种题,那咱 咱们就去想一想犯错后果方程,想一想最基础的,其实你就是确定两个温度,确定两个平衡场数,是不是就能得到最终的结果。那高考的话,人家画图都是比较标准的啊,就算没有这个横纵坐标, 对吧?你自己差不多列个数据也是完全 ok 的,对不对?你用尺子呀,尺子量一下呗,尺子量多少数值就是多少,高考人家做图很标准的,所以说这个 k 你是肯定可以算出来了,比如说就是没有这些数据,对吧?那温度大小你起码知道吗?你就拿尺子量, 你挑两个温度,这两个地方尺子量出来纵坐标乘一下,这两个地方量出来纵坐标是多少?转化成 k 乘一下是不都可以啊?完全 ok 啊,同学们。所以以后碰到这种平衡的证明题,我相信你肯定就会做了, 你看一下咱们数学的答案啊,和这种答案哪一种好?那很明显是后者,相信你用这种方法去思考这种题的话,你是可以学会这种题的, 对吧?啊?也就是说,其实拿这个模型啊,就给同学们说了,这种证明题你就找两个温度,找两个 k 就比就行了,本质还是这样子啊,那具体如果没有中坐标的话,你就直接直接拿尺子量就可以,那当然咱们也可以带到范特护肤方程里去验证一下。你看 浪引 k 二比 k 一, k 二的话,它是小于 k 一的十的负四和十的负三点八吗? k 二小于 k 一,所以这样一除的话,这个东西小于一,浪引后是不是小于零?这个玩意小于零就说明 右边这个整体也是小于零的。好,接着代入 t 二分之一和 t 一分之一, t 二分之一和 t 一分之一,咱们 分别选的是二点二和二点四,对吧? t 二分之一数值是二点四, t 一分之一是二点二啊,直接代入。有些同学啊,你们一定要仔细一点,别带个二点四分之一和二点二分之一。好家伙,你看清楚,人家这个 t 分之一的数值就是二点二和二点四,所以 t 二是二点四, t 一分之一是二点二,那这样一减的话,这个东西大于零,而是长数大于零的,那 that h 是不是只能大于零? 这就是奋斗护肤方程在高考以及模考中的应用。第一个结论,同学们要记清楚 lionk 和 t 分之一的图像, 你是可以直接通过斜率读出这个反应到底是吸热还是放热反应,同时读出它含变的绝对值,到底谁大谁小都是根据斜率看的。第二种 情况的话,就这种现在比较流行的平衡证明题,对吧?啊?这个很多地方反正这种题出来以后给的答案全是这个样子,没有必要,对吧?你就想一想,如果能记住这个方程的话,记一下,那记不住的话你就清楚记清楚啊, 咱们不管碰到哪种题,永远回归到最基础的,别搞什么 log 这种花里胡哨的啊,你自己考场上也想不来,你就记清楚,咱们就挑两个点,找出这两个点的温度, 对吧?再算出这个两个点对应的平衡长数,然后比大小就行了。那这一说如果没有纵坐标的话,你就可以直接说,比如说 t 的时候,由图中可知 啊, k 一大于 k 二,对吧?就可以了啊,就可以了。那你知道了温度,知道了 k 之间的大小,那最终反应的席放热是不是就出来了? ok 啊。
22化学超人本人账号 00:30
00:30







