九年级化学江西人教版试卷该怎么做
来自江西头部公办初中江西师大附中的九年级化学试卷,今天呢,我们给他打印出来了,不过咱是教物理的,不专业,得找一个化学老师来做一下。郭老师,哎,做一下可以啊,限时三十分钟哦。三十分钟?我觉得你看不起我了,好,看一下 果然没有吹牛啊,不到半小时就解决了,考多少分你猜一下没满分 六十九分。朱老师,嗯,评测一下师大的卷子了啊,我觉得其实这份试卷非常亮点的地方是这份试卷在这个精油网上的难度的话呢,难度系数是零点五八,其实还算还可以,挺不错的。最亮眼的两个题目的话呢,是两个实验题,它这个实验题和别的学校的实验题不大一样, 学校的实验题都会有种就是网上随便括笔一些题目的感觉。师大附中这个题目还是真的非常用心的,这两道实验的探索题是真正儿八经的探索,真的是能够体现出学生的水平的。不愧是师大附中啊,虽然我是教物理的,但是我也感觉到师大的实验探索题,尤其在物理的实验探索题啊, 很多时候出的是非常灵活的,很多时候又有坑。其实孩子们要想做试卷呢,就要做这种灵活的卷子,因为我们中考现在他考的越来越灵活了,也越来越考虑你的细心度了。问题来了,接下来你想看权哥测评哪个学校哪个年级,哪个科目的卷子呢?
粉丝2.8万获赞10.2万
相关视频
 00:11
00:11 02:56查看AI文稿AI文稿
02:56查看AI文稿AI文稿哈喽,大家好,今天给大家分享一个特别重要的知识点,叫离子共存问题,离子共存什么意思呢?就是这两个离子在一起不反应,大家一定要注意,能共存一定是不反应, 那不能共存就是反应了,那离子常见的我们都是酸碱盐中的概念,对吧?酸碱盐中的阴阳离子,那也就是说它能不能反应,就是它们能不能结合生成水沉淀气体,也就是说还是很重要的。这里, 呃,一个是沉淀,大家把溶解性表一定要搞清楚,常见的哪几种沉淀好,然后还有一个就是气体二氧化碳啊,对吧?氨气呀,常考的是这几个哦,这氨气常考的是这几个,大家关注一下氨气的话,就是氨根和氢氧根,对吧? 然后碳酸碳酸根和碳酸氢根于氢离子,这个这是生成二氧化碳的,一定要关注。那生成沉淀的,再次强调一下,我们需要通过阴阳离子的判断,比如说我们常考的碳酸根,那它的沉淀很多,你就记那个不是沉淀的, 然后绿离子呢?只有一个沉淀氧化银,你就记这个沉淀,然后其他的都不是沉淀,对吧?然后包括氢氧根啊,碳酸根,硫酸根,对吧?等等,这些怎么去记,一定要关注哦。 好,那现在我们来看一下这样的一个题目,那我们 ph 值为十三哎,这是外部环境,那我们常见的外部环境有哪些?比如说 ph 值,那等于十三,那说明它溶液有大量的氢氧根,那还有一些 ph 值,比如说小于七的,就说明它有氢离子。还有一种描述的话呢,比如说无色呀,对吧? 对不对?就常见的这种提射给的条件一定要关注好,也就是说这道题里面就是人为的给你这些离子里面,你要都要给他补个氢氧根,氢氧根,氢氧根,然后还有无色透明,但无色透明和澄清透明还不一样, 无色透明是真的没有颜色啊,澄清透明是可以有颜色的,无色透明那考的就是那几个常见的二价铁,三价铁,铜,高锰酸根,常见的是这几个有颜色的。 哎,大家注意有颜色的啊,有色的是二价铁,三价铁、铜离子、高锰酸根。 对这几个颜色一定要搞清楚啊,这个前面都有给大家说过啊,这就不再说了,那我们先看一下,有颜色的就先给他排除掉,比如说 c, 有 颜色就先杠掉,然后其次呢,注意他能能能共存啊,也就说还是生成无色透明啊, 大家注意一下啊。然后那这个题我们来看一下 a, 那 他就不行,氢离子和氢氧根要反应,那氢氧根和氨根也不行。好,那再看 b, 哎, b 好 像是可以的,然后 c, 呃, d 选项就 这个镁离子和氢氧根不行,所以这个题正确答案我们选择的是 b 选项。大家注意常见的这种题目应该怎么做,就要很熟悉它的考点到底是什么,同时我们对咱们生成沉淀的气体的要很熟练才行。你看这个题虽然小,但是考点却。
18刘老师的理化课堂 04:26查看AI文稿AI文稿
04:26查看AI文稿AI文稿我们来看下这个题啊,说像某氢氧化钠溶液中低加一定质量的硫酸铜溶液啊,二者恰好完全反应过滤, 原氢氧化钠溶液的质量是生成沉淀质量的二倍,则原氢氧化钠溶液中溶质的质量分数为多少?约为多少?我们来看一下啊,选项有百分之二十五,百分之三十二,百分之四十一和百分之二十五。 那有的同学看到这个题了,不知道该怎么解,我们首先来看到这里边是什么样的反应,好吧,哎,发生一个什么样的反应?首先是什么?氢氧化钠是不是?哎?原如月是氢氧化钠和什么反应?和硫酸铜发生反应是吧?生成什么呀?生成 氢氧化铜的沉淀,哎,蓝色沉淀和什么呀?硫酸钠是不是,哎?是不是硫酸钠配平以后啊,我们来看一下啊,首先看它的亮的关系啊,哎,我们来看 氢氧化钠是多少呀?是不是四十呀?哎,这里边的它的量的关系是二乘以四十,哎,相对质量啊,这是氢氧化铜是多少呀?是不是九十八,对不对?那我们来说,他说 原氢氧化钠溶液的质量是生成沉淀的质量的二倍,那我们这个是不是生成的沉淀啊? 对不对?生成的,那我们给它,我们不知道是多少,是不是我们可以给它设一个值出来是吧?那我们设,哎,设生成的什么呀? 氢氧化铜是多少?九十八克,是吧?哎呀,我们可以设它是九十八克,则什么参加反应的什么呀? 氢氧化钠的质量是 为多少? x, 哎,这样算的话,我们来看这个是九十八克,那根据,根据我们质量手工定律啊,是不是什么?这个是 x, 对 不对? 我们来看一下啊,叫什么呀?什么叫实际什么 质量的比等于什么呀?相对质量的比,对不对?哎,等于相对质量的比啊, 我们来看一下啊,看一下比例关系啊,是不是这个跟这个的比啊?这是叫相对质量的比, 是不是二乘以四十,哎,比上多少?比上九十八等于啥呢?等于实际质量比,是不是?哎?等于 x 比上九十八克,对不对?那我们求出 x 等于多少克?等于八十克, 是不是八十克?那这里边是不是我们说的八十克?是不是参加反应的氢氧化钠质量?那我们说原氢氧化钠溶液的质量是多少呢? 他说是生成沉淀质量两倍,那我们说我们设的生成的沉淀质量是多少呀?是九十八克,那这从这个里边呢?原是吧?溶氢氧化钠溶液,按溶液的质量啊, 质量是多少呢?是不是九十八克乘以二等于多少?一百 一百多少?一百九十六,哎,是不是一百九十六克?那我们来看实际参加的是八十克,那这个质量分数是不是应该该怎么算呢?八十克比上多少? 哎,比上个一百九十六克,然后乘以多少?百分之百得到一个值是多少呢? 百分之四十一,二是大约等于二,我们算出来大约等于百分之四十一,所以这个时候啊,这个时候,那我们就求出来了这个值,所以该选哪个啊?选 c 对 不对?
 04:57查看AI文稿AI文稿
04:57查看AI文稿AI文稿hello, 大家好,今天给大家分享一个非常有趣的叫误差分析,就是配置一定浓度的这个溶液,它的误差我们应该怎么去分析呢?但是我要知道一点啊,就是溶质的质量分数,你要知道是谁除以谁,对吧?就这个质量分数呢,就等于溶质 m 质 除以 m 页乘以百分之百。哎,你说这个溶质的质量分数,它到底是偏大还是偏小,你肯定要看这两个,如果溶质的质量偏大了,你的质量分数是不是就会偏大? 好,那液体的质量如果偏大,那你就我们应该就会,就是溶质成分就会减小就偏小的,以此类推。所以你一定要去做题的时候,你一定要去判断这个公式,我们的误差如何影响这个公式的?我们来举几个例子啊。 比如说你看第一个,你的四季含杂质,比如说你要配绿化纳溶液,结果绿化纳里面有杂质,那我们大家注意啊,你的溶质的质量就会偏小,溶剂不变,这样的话,你的溶质质量分数不就偏小了吗?好,然后还有一个就是乘凉的时候,四季和砝码放偏,要和砝码放 反了,大家这是左误右码,如果没有使用油码,那没问题啊,就是比如说五克,五克都没问题,这个就不影响。但如果你使用了油码的话,我们理论上应该是加油码的质量,就是法码加油码,但是现在你放反就得减啊,所以这个时候呢,我们就说明溶质的质量就得减小, 所以我们算出来结果就偏小,一定要注意好。然后还有你这个量取水的时候,或者量取液体的时候,你仰视或俯视,读出了,我们要知道你腹大养小,然你容质没有变,但是容计变了,仰视腹大养小,对吧? 你仰视的话,你读小了,那这个世纪不是偏大吗?所以你就偏小了。对,以此类推。好,还有你乘凉好的世纪没有完全转移到烧杯中,那这个时候呢?我们这个溶质的质量就是偏小吗?溶质这两分数就偏小,这个注意 好。然后还有一个就是往烧杯中倒水,有少量水溅出来了,那说明你倒的水少了呀,那这个溶他不就偏大了吗?还有干燥,就是溶解的时候,你的烧杯没有干燥, 没有干燥就水多了,所以也是偏小。少量液体溅出,这个没问题啊,你都配好了,溅出来了,溶质的质量分数不会改变你总就是你的整体上都减小了吗?配都都都掉出来,没关系。好,世纪平事后先用水洗涤,未干燥 就世纪平事先用水洗的,没有干燥,说明你的这个。大家注意,这个溶质的质量不变,但你的溶剂仍然是偏大了,所以我们的溶质质量分数仍然是偏小。所以你要看所有的误差,都要看对溶质和溶剂或者溶液它是怎么影响的,你就知道它的误差是什么了。我们举个例子, 举两个例子啊,那你看下来,操作能使溶质质量分数偏小的,比如说第一个绿化那潮湿,绿化那潮湿,你乘凉的时候,你不是乘的绿化,那的质量要比实际的要偏小了,所以溶质质量分数偏小,这是对的。然后下面乘凉的时候,绿化那放到了 u 盘,而且还使用了油马,这个跟刚刚说的一样,你也是偏小了。 好,他说所有的砝码表面生锈,表面生锈,你乘凉的质量不就大了吗?所以你的质量分数应该是偏大。好,用。两桶量取水的时候你仰视了度数,大家知道仰视,仰视,然后呢?你的水是不是就导致你的水就偏大了, 对吧?这个要注意一下。好,那这个时候我们的溶质这样分数就会偏小,要注意五,将配置好的装平的时候有少量撒出,这个我们说是不影响,由此可见,答案选的是 a 选项,这个是偏小的,大家一定要搞清楚啊。好,还有一个大家可能在讲的时候还是有点,我,我把那个 这个两桶的腐大养小,大家是不是不太理解,你看就这个,我要读这个液体的,读这个页面的时候什么叫氧势呢?你看这里,比如说这个, 这就叫仰视,这是平视,这个叫俯视。 a、 b、 c, 你 看 a 的 话呢?你是不是就读的话,你就读大了吗? b 的 话是正常的, c 就 读小了,对吧?就是你读小了,你才。比如说我们现在溶剂你需要一百毫升,你读小了,你还读一百毫升呢,那实际上你肯定是大于一百毫升,所以我们才说溶剂 偏大,这个一定要搞清楚啊,这个不再说了。好,那最后一个,呃,配置百一百克百分之零点九的生理盐水,导致溶脂量分数偏大的是, 那我们看 a, 这个刚刚说了他是偏,怎么样你,你仰视读数,这个就是我们导致咱们的,这个是浓度是偏小的。好,还有将配置好的溶液倒入吸口瓶,瓶中原来有水, 那你肯定溶剂多了呀,所以溶质质量分数偏小,少量水留在,少量水留在两桶中。就是你本来该用一百毫升的水去兑的,结果你只只兑了九十五毫升。那这个时候呢,肯定是溶质质量偏大了。好将泡将配好的倒到细口瓶有部分溢出。我们说这个是不变的啊。
29刘老师的理化课堂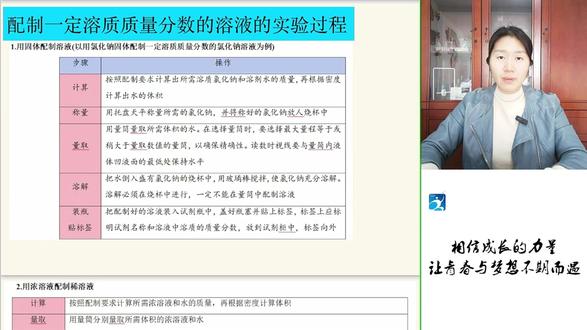 07:43查看AI文稿AI文稿
07:43查看AI文稿AI文稿哈喽,大家好,前面呢我们都讲了很多关于溶质质量分数计算的题型,那今天我们来分享一下如何配置一定浓度的就一定溶质质量分数的溶液,那这个实验的过程我们需要注意哪些内容呢? 大家,我们以绿化钠为例,那你要具备一定浓度的绿化钠溶液,那绿化钠本身是固体,你需要用水来把它混合,所以你需要计算绿化钠的质量,水的质量对不对?所以呢我们首先一定要先算, 比如说你假如我们要配置百分之十的绿化纳溶液,一百克,比如说一百克百分之十的绿化纳溶液,对吧? 那首先我们得计算你需要多少克绿化纳,多少克水,所以我们底下一个计算,然后接着要称出绿化纳,比如说这里面我们绿化纳算完之后发现它是十克,那你是不是要称十克绿化纳,你要用天平来称,接下来呢再去算你的水是不是就要九十克了?因为你这个注意一下,你水正好溶质,加溶剂等于溶液 好,所以呢你要去量出水的质量,但是这样很麻烦,对吧?所以我们其大家知道,九十克相当于九十,直接用密度计算,应该相当于九十立方厘米,那就是九十毫升,你用两桶直接可以量,而接下来是溶解,最后装瓶。好,在这个过程中,那我们要注意它的实验的误差分析,我们后面的视频会给大家介绍。 好,那除了这种直接从固体,我们还可以从浓溶液来进行稀释,得到你想要用到的溶液,比如说我百分之十的硫酸钠, 我把它稀释成百分之一,哎,那我们就稀释,那当然你也要去算一下我需要向里面加入多少水,好,然后呢,先计算再乘凉,对吧?再去量取水,然后再混匀,再贴标签也可以。好,这样一个过程,那我现在带大家, 嗯,看一个完整的题目,他是怎么做的? ok, 这样的一个实验过程。 ok, 那 么现在来看一下百分之六的硫酸钠溶液它的配置过程。一百克,那么用到的器材有哪些呢?你算完了之后发现需要六克硫酸钠,那你先称,称的时候就需要添瓶, 然后呢,你要从这个实验的就是我们的世纪瓶里把硫酸钠取出来,我们要用药食,接下来呢,你开始量取了,是不是要用两桶啊? 哎,两桶测体积,接下来你要溶解了,你是不是得需要玻璃棒啊?啊?玻璃棒,哎,那我们把这个过程搞定,那我就看看它需要用的东西就一目了然,玻璃棒还有烧杯,浇头滴管,这些都是在量取以及我们这个溶解的过程中, 对吧?要用到的啊。好,那接下来我们继续看接下来操作了,继续计算,然后发现硫酸钠的质量为刚刚算出来是不是六克,对吧?那需要水的体积,那需要水的质量是九十四,那体就是九十四毫升。然后接下来乘凉的过程中发现若天平时针向左偏,那我们就要左误右码嘛,所以你需要向 你像是不是加砝码呢?或者是移动油码呢?不是,为什么呢?因为你称入六克,你的砝码还有油码都已经标好了,就是已经通过,你已经就是让他们的市数为相当于啊,就是你拿了五克的 把马加上油马,又移了一克,就是那边已经右边已经是六克了,你必须向里面加药品,加加,加到天平平衡就可以了,所以我们应该移总部分药品,要注意,千万不能再加把马或者是移油马了。 ok, 好, 那两取我们用两桶,和谁两取呢?我用浇头滴管,为什么呢?因为你浇头滴管, 因为你一下子不可能,不可能直接倒的正好,所以我们需要用浇头滴管啊,来去给它滴一下最后的一几滴。好,我们应该选择量程为多少呢?是不是一百毫升的,对吧?好,然后呢?接下来溶解,用玻璃棒不断地搅拌,那这里搅拌的目的是什么?是不是就加快溶解? 好,那在这里面我稍微拓展一下玻璃棒它的作用,在这里是加快溶解,那我们如果是两个反应,你在那搅拌,那就加快反应,如果我们是过滤,你用胶头,你,你用那个玻璃棒是不是可以 怎么样引流,对吧?那后面我们在加热蒸发的时候,我们就是搅拌,就防止局部过热液体飞溅,对吧?等等,就是不同的场景玻璃棒搅拌的作用,它其实是不一样的啊,这个关注一下。好,我们开始贴标签。贴标签应该怎么贴呢?就上面要我们要写绿化纳溶液,然后写个字,就是写绿化纳 溶液,把它写一下,然后呢就写进去啊,然后接下来就底下写百分之六就可以了。好,那再看一下误差分析,他说配置的过程中哪些是会使它小于百分之六呢?大家知道这个百分含量啊,它是 还有谁?溶质, m 质除以 m 液乘以百分之百,那你想让溶质量分数小于六,你要么溶质少了,要么溶液多了,对吧?所以我们看一看就可以了。比如说天平未调平,空载时,时针就向左偏, 那这个要注意一下啊,就是你还没量他左,他左边就就相当于就有绿化,那就要少一点,对吧?这要注意,一是可以的。 好,那下面砝码生锈或者有油污,那这个地方要注意一下啊,你有油污,那待会就会使你测测出来的硫酸钠的质量偏大,因为你已经你的砝码太重了,所以它不行。好,然后硫酸钠固体中有杂质,那这个肯定可以的吧,对吧?好三,然后四 左误右码,并且使用了油码,那这个也错了,对吧?你应该是减,而不是加了。下面将氧化钠转移到烧杯中,滤纸就是称量纸上有残留的固体,那就说明你没有移到,就是烧杯里面没有移完,那肯定也不对,就氧化钠的质量就会偏低。好量。取水时俯视,读数, 俯视,对吧?俯视说明你读大了,那是液体的质量是偏小的,所以那是结果偏大,这也不对。 七,然后呢,他说到将凉,将凉水倒入烧杯中,由水溅出,那也会导致水偏少,溶液偏低,质量分数偏大,也不对, 烧杯不干燥,内壁上有水珠啊,那这样的话,你相当于稀释了你的溶液,对吧?因为这一部分水不是在就是不是你乘凉的那个,就是你用凉的,凉的那部分水,所以你相当于多了水,那这个是偏低。 将配置好的一一道世纪屏中有液体溅出,这个没问题,因为这个是不变啊,因为你已经配置好了它,溶液具有均一稳定性,你是你飞出去了,没有关系,不影响,总的就不影响溶液溶质的质量分数可以注意一下。好的,再看一下,补充一个实验,我们来看一下一个小小的计算啊, 他说如果我们那他说除了用绿化大固体配之后,我们可以用较浓的来配,那我们用百分之十的来去配,那这样的话实验的步骤为计算量取,然后还有混匀,对吧?这个注意下, 你量取了就是浓的,稀的,对吧?你要配稀的,你要把浓的给量好,然后看倒多少水,然后浑不浑,然后这样装平就可以了。我们来看一下,算一下,他说需要百分之十的硫酸钠的质量为多少克呢?咱们利用的应该是溶质的质量相等,对不对?所以呢,这里应该是一百克 乘以百分之六,这是你要配的溶质的质量,那百分之十乘以 m, 那 这个 m 就 应该是六十克,所以你需要六十克,要注意,那所以你需要水多少克呢?你总共就是这个浓溶液是六十克 啊,这个浓溶液呢是六十克,你要配的是一百克,总的是一百克,所以你是不是要加入四十克水进去,所以这是四十克,这个要注意一下,你通过计算就出来了。 所以以上呢是用两种方法,一个是固体来配的,一个是浓溶液来配置的,大家注意一下,整个过程比较重要的,比较难一点的就是这个误差分析,大家把这个公式一写,对哪一步有影响,你就轻松的搞定了。好,你看这道题你听懂了吗?
15刘老师的理化课堂 10:29查看AI文稿AI文稿
10:29查看AI文稿AI文稿宝子们上午好,今天我们看金属和盐溶液反应后所得的绿渣绿叶成分的分析。像这种题目就是把一定量的 某种金属加入到 混合溶液中,然后过滤得到了绿渣和无色的绿叶。好,那像这种一种金属加入到混合的溶液, 我们可以先把它们的金属的活动性先写出来,我们可以一起回顾一下。甲 钙、钠、镁、铝、 锌、铁、锡、铅、锌、铜、汞、银、铂金, 这是我们的金属活动顺序表。对于这样的题目,我们有个原则,就是隔得远先反应,也就是说金属活动性强的 可以把最弱的先置换出来, 隔得远 先反应, 那这句话是什么意思呢?我们可以看到金属镁与这两种溶液中的银隔得更远, 所以金属镁会先和硝酸银发生反应,等金属镁有剩余,那么剩余的镁才会与硝酸铜发生反应,所以这是第二步反应, 所以这是第二步反应。 那我们可以列一个表, 我一般都是让学生列一个表,这样比较清晰明了,等你做多了,反应快了,我们就可以更快的把这个表把它列出来。好,那所以我们这边左边是金属镁, 那隔得远先反应,那我们把隔得远的硝酸银写在这上面,然后其次是硝酸铜, 我写过来点画一个表格。 好,那么镁放入混合溶液中,会先与 硝酸银反应,那这种情况是代表 每与部分的硝酸银发生反应与部分的,所以我们这这里画线只画一部分,那再画一根线, 代表镁把硝酸银给完全反应掉,所以说他就把这里的全部给消耗完了,所以我们就画到顶,代表金属镁与硝酸银恰好完全反应,让我们继续画一根线, 那这代表什么含义呢?代表金属镁不仅把硝酸银给完全反映了,而且还反映了部分的硝酸铜。再画一根线,那 同学们,你们应该也知道它代表什么含义了吧?对,那第四根线就代表金属镁不仅把硝酸银完全反应了,而且把硝酸铜也完全反应了, 这是第四根,这是第四根线。那最后一根线代表什么含义呢?我们看一下,最后一根线代表金属镁, 把硝酸银溶液完全反应,并且把硝酸酮也完全反应,而且还有部分金属镁剩余啊。 那以后做题目,我们都可以这样画图,我们把金属放到左边,隔的远的容易放低格,其次是这个 隔的第二远的啊,所以这样我们就比较容易判断题目。那我们来看一下题目, 得到了绿渣和无色的绿叶,那这样是无色绿叶,说明已经没有铜离子了,这里面镁离子、银离子都是无色的啊,只有铜离子是有色的,那它没有颜色说明无铜离子, 没有铜离子说明硝酸铜被 被完全反应了哈,硝酸铜被完全反应了,那对应的应该是第 这根线哈,对应的应该是第四根线,我画心心也可能是第五根线。第四根,第五根线都代表铜离子被完全反应啊。画了心心的这个这两根线啊,那我们可以做下题目, 第一个绿扎中一定有铜银,那我们看一下,这样是第四根线或者第五根线,我们可以看到, 那我们把这个置换出来的金属也可以写在这个上面,我用绿色的来写,镁与部分的银反应,部分的硝酸银反应,所以说有银置换出来,那这里也是一样的,有银置换, 这里也是有银,这里呢与铜,硝酸铜反应,有部分的铜置换,这也是同样都是有银的 啊。有同有同。好,所以我们可以做下题目。 第四根线,打星星的第四根线, 而第五根线我们可以看到是一定有铜和银的,一定有铜和银啊,这是一定有的,所以这个是对的。那美的话,我们可以看到第四根线是没有美的。 第四根线没有美,第五根线是有美的, 所以说可能是有美的啊,可能是有美的。那么一是正确的,那看二, 那二就错的,因为我们说了,一定是有铜的,一定是有铜的,所以二,这里是错的,一定是有铜的。那第三个月中一定有硝酸美。 我们看一下,我们每只要放到混合溶液中,一定会 反应,所以一定会有硝酸美生成,这是一定有的,那我们看一下后面这句话,一定不含有硝酸铜,硝酸银,这也是对的。我们可以看到第四根线,这根线哈,画了星星的这根线, 硝酸铜已经被完全耗尽了,走完了。第五根线, 硝酸铜也是,硝酸银和硝酸铜也是被完全消耗完的啊,这两根线都是被完全消耗完的,画满了代表已经反应掉了,所以这是正确的,一定是没有硝酸铜和硝酸银的。 那以后遇到这种类型的题目,我们就可以画一个这样的图啊,画一个这样的图, 这样就比较方便做题目。那如果说你们有什么问题可以留言。
34备课汉姆 07:38查看AI文稿AI文稿
07:38查看AI文稿AI文稿宝子们上午好,现在我们继续讲金属,我们这节课讲比较三种金属的流动性顺序怎么设计实验像这种是选择题的一个高频考点,那举个例子 比,比如说我要比较金属镁、铁、铜,比较它们三者的活动性, 想要比较金属镁、铁、铜它们的活动性,我们首先就是先排序, 排顺序,按照活动性进行排顺序,那我们可以把这个金属活动顺序表背一下,钾、钙、钠、镁、铝,然后镁镁完了之后 甲钙钠镁、铝、锌铁,然后是铁、锡、铅、锌,然后是铜、汞、银、铂金。所以第一步排好顺序是镁、铁、铜。然后呢,我们有两种方法, 我们可以采用两单夹一页,两单夹一页的意思是 金属镁作为单质,金属铜也是单质。把金属镁和金属铜片每条和铜片分别插入到 硫酸亚铁溶液中,这里我们的铁我们采用硫酸亚铁,这里用的跟铁有关的溶液,我们统一都用亚铁离子的溶液啊。 所以如果说我们要写这个方法的话,我们就写将 光亮的每条 和铜丝分别放入硫 酸亚铁溶液中。 注意这里我们必须用的是这个硫酸亚铁溶液,而不是硫酸铁啊。 那我们可以看一下能否比较出我们把镁放入硫酸亚铁溶液中。我们知道我们可以看到 镁位于铁之前,所以可以把铁给置换出来,同时生成硫酸镁溶液。通过这个我们可以比较出 金属镁的活动性强于铁。好,那我们把铜 和硫酸亚铁放在一起,铜没有铁活泼,因此铜和硫酸亚铁不能发生置换,说明铜没有铁更活泼。综上所述, 它们的活动性是镁的活动性强于铁, 铁的活动性强于铜。这是第一个方法,叫做两单加一页。方法二,我们采用的叫做两页 加一单。 好,两页加一单是什么意思呢? 也就是说把中间的铁单质分别放入硫酸溶液和 硫酸铜溶液中。我们来看一下,同样的也是将打磨光亮的, 这里一定要注意要加一个这个词,打磨光亮的,因为金属表面可能会有氧化物,我们要除去氧化物才能够看到正确的现象。将打磨光亮的铁丝 分别放入 硫酸镁溶液和硫酸铜溶液。那我们看一下如何比较 把铁放入硫酸镁溶液,铁没有镁更活泼,因此它们是不反应的, 说明镁比铁更活泼。那再把铁放入硫酸铜溶液, 铁位于铜之前,能够发生置换反应,所以把铜给置换出来,同时生成硫酸亚铁,因此 铁的活动性是铁啊,是镁大于铁大于铜 啊。所以做这类题目,我们就先排好顺序,然后再采用两单加页或者两页加一单的方法,注意 一定要写这个打磨光亮的啊,打磨过的金属。然后呢,这里我们也要加溶液两个字,这里一定要加溶液两个字。 好,那如果有问题的话,欢迎宝子们留言。
35备课汉姆 12:34查看AI文稿AI文稿
12:34查看AI文稿AI文稿hello, 大家早上好,那今天我们继续看这个命题点五的练习。第十一题, m 点代表的是什么的?溶液的不饱和状态?我们看到 m 点位于 乙这根曲线的下方,所以 m 对 于乙来说是不饱和溶液,因此这个我们写乙。 我们要知道,曲线及曲线上方的部分代表的是 该溶质在对应温度下的饱和溶液,而曲线下方对应的是该溶质在对应温度下的不饱和溶液,曲线及曲线上方 是对应的是饱和溶液。第十二题, 三十度时,十五克的钾放入五十克的水中,那我们就找到三十度,我们看看到三十度,那我一般教我的学生做题目就这样温度啊,然后呢?一百克的水, 根据比例关系啊,三十度时,一百克的水溶多少克的钾,我们可以看到 啊,这是甲,曲线在这里融二十五克的甲,那我们这里只给了你多少克的水?五十克的水,因此我们根据比例关系,我们这里就列五十克的水, 根据比例关系只能溶解一半。十二点五克的甲, 而我们这里给了你多少呢?给了你十五克,我们这里给了十五克的甲, 此时溶液是一个过饱和的状态,所以说我们这个空,我们填饱和啊,因为他最多最多只能溶解十二点五,我给了你十五啊,此时是一个饱和的状态。 第十三题,五十度时,甲乙丙的饱和溶液降温至十度,那么甲得到的是什么溶液?那我们把这里原来的部分给擦掉, 我们找到五十度饱和溶液,这样是饱和溶液,说明他们都刚好在点上面啊,都在点上面,那丙就在这里,甲乙都在同一个点, 降温至十度,降温,降温,我们可以看到,降温的时候,甲的溶解度在逐渐怎么样, 逐渐减小吧。啊,降温至十度,逐渐减小,所以说它的溶解度在减小,那么它就有晶体析出, 那么溶液仍为什么饱和状态,因此这也是人为饱和溶液。再来看下乙, 乙在降温的时候,溶解度也在逐渐减小,所以乙也有晶体析出,那么乙到达这个点,它仍然是 饱和状态,所以这个孔我们仍然填饱和溶液。 看一下丙,丙, 丙在降温的时候,溶解度在逐渐增大,所以没有晶体析出,因此 溶液没有晶体析出,那么它就是溶质,是原来跟原来一样的溶质是不变的,那么丙就到达了这个点, 丙到了,到达了这个绿色的这个点,所以它指示是什么,什么状态,在曲线的下方,因此它是不饱和的状态,所以丙溶液指示是不饱和 溶液。第十四题,三十度时, 甲乙各三十五克,倒入一百克的水中,充分溶解后升温,还能继续溶解的是,那我们可以看到,在三十度时,我们把这里擦掉。 在三十度时, 乙的溶解度明显是高于三十五的,比三十五更高,所以乙的溶解量是大于三十五克。那甲呢?看一下甲,甲在这个点, 钾的溶解度此时是小于三十五克的,那么你在三十度时,乙的溶解度大于三十五克,那么乙是全部溶解的, 而甲的话,溶解度小于三十五克,有部分未溶解完,也就是说甲有剩余, 那么升高温度,剩余的甲就会继续溶解,因此还能继续溶解的,我们就写甲物质。 十五题,十到三十度时,甲乙两物质能不能配成质量分数相等的饱和溶液? 我们可以看到,十到三十度的范围内,甲乙两物质如果说有交点,那么就能够配成 该温度下对应的质量分数相等的饱和溶液。那如果没有交点,我们看一下有没有交点。 红色的代表的是甲,这是甲在十度到三十度的部分,那蓝色代表乙, 我们可以看到甲乙在这个温度区间没有交点,因此它们不能够啊,不能够配成质量分数相等的饱和溶液,不能。 第十、十六题,十度时,甲的不饱和溶液怎么样转化成该温度对应下的饱和溶液? 十度,那么它是不饱和溶液。我们可以随便找一个点, 比如点在这里啊,这是位于假曲线的下方,是一个假的一个不饱和溶液,那想要把它变成饱和溶液,我们有两种方法,要么就是恒温蒸发溶剂。 恒温蒸发溶剂,那还有个方法,我们可以直接往里面添加溶质,添加溶质,那么它就往上走啊,到这个点就变成饱和溶液,所以我们可以写增加溶质。 那其实上课的时候我会跟学生说,最不饱和溶液转化成饱和溶液,最简单有效的方法就是增加溶质, 换句话说,不饱的你就喂饱它啊,这是比较通俗的说法,喂饱它,喂饱它,那就增加溶质,这是对于所有的溶液都是适用的。 好,那我们再看第十七题,接近饱和的乙溶液转化成饱和溶液。接近饱和,说明原来是不饱和,那不饱和的溶液转化成饱和溶液也是我们刚才说的,比如说增加溶质或者 恒温蒸发溶剂啊,注意是恒温,因为有些溶液它的溶解度,呃,它可能随温度升高而增大,也可能减小,所以最保险的方法是增加溶质或者恒温蒸发溶剂。 那乙溶液它的溶解度是随温度的升高,我们可以看到乙溶液的溶解度,我们用红色的线随温度升高逐渐增大, 那么你也可以通过降温的方式降温,那么溶解度再减小也是有晶体析出的啊,所以说我们也可以通过降温 丙的不饱和溶液转化成饱和溶液,那我们也是可以一样的,通过增加溶质, 也可以通过我们可以看到 丙的溶解度随温度的升高逐渐减小,因此我们可以通过,比如说任意打一个点,比如说这个点对于丙来说 是不饱和溶液,那么想要变成饱和溶液,我们可以平着移,也就是往右移,升温也可以向上移,也就是我们说的增加溶质的方法,我们可以通过升温 或者恒温蒸发溶剂。 那如果说你们还有什么问题可以在底下评论留言啊,看到都会啊回复你们。
24备课汉姆 07:04查看AI文稿AI文稿
07:04查看AI文稿AI文稿好,我们来看到这个例一的第一题,以物质 是它的溶解性是怎么样的?我们可以看到以物质,它在二十度左右,它的溶解度是三十五克。那我们说了,在二十度左右,在溶解度大于等于十克归为易溶,所以这里我们就写易溶, 所以这答案我们写易溶 好,我们把二十度时溶解度大于 等于十克的归为易融好。第二题,三十度时丙物质的溶解度,我们可以看到三十度时丙物质的溶解度 是二十五克。这里带好单位,溶解度一定要带好单位。第三题,十度时甲乙丙物质的溶解度大小关系,十度时我们可以看这个曲线的高低,最高的是丙, 第二高的是乙,第三高的是甲,所以溶解度曲线关系是 b 大 于乙 大于甲。 p 点的含义 好,我们来看一下 p 点的含义。 p 点是甲乙两物质在五十度时的一个焦点,说明在五十度时 甲乙两物质的溶解度相等,且都等于 五十克。 这里焦点的溶解度已经告诉我们是五十克,所以说我们需要把这个也写出来。那如果说题目这里没有明确标出 溶解度相等的这个点,那我们可以不写,这里也要记得带好单位。 第五题,甲乙两物质的溶解度随温度升高,我们可以看到甲乙两物质的溶解度随温度升高而逐渐增大哈,增大, 其中溶解度受温度影响比较大的是,我们可以看到甲受温度影响最大, 那丙物质的溶解度随温度的升高而逐渐减小。 第七题,甲中会有少量的乙或丙, 甲中会有乙,甲受温度影响,甲受 温度影响 大,所以我们就采用降温结晶,只要稍微一降温,就有大量的晶体析出,所以甲的话,我们可以采用降温结晶,或者说冷却结晶 里中混有少量的甲,我们可以看到 乙受温度影响比较小啊,比较小, 所以对于乙的话,我们一般采用蒸发结晶, 当丙中混有少量的甲或乙,我们可以看到丙的溶解度随温度的升高而逐渐减小,那为了把丙给提取出来,所以我们可以采用升温的方法, 那么这里我们就写升温结晶。 最后一题,第十题,从甲的饱和溶液中获得固体甲,好,那我们把原先的这些擦掉, 那我们随便点一个点,可以代表这个甲的这个饱和状态,比如说点在这里 啊, q 点, q 点在这个甲曲线这上面,所以 q 点对于甲来说是一个饱和溶液,那么想要吸出晶体,我们要使得它的溶解度逐渐减小,因此我们应该采用的是降温 啊,也可以说冷却结晶。 好,那么今天的课堂我们就先讲到这里,我们下期再见。
16备课汉姆 00:39查看AI文稿AI文稿
00:39查看AI文稿AI文稿中考化学最难的八大流程图题全部吃透,稳进班级前三!中考化学必会八大工艺流程图题专列类型一,质备与生产流程类型二,回收与利用流程 类型三,海水资源的利用流程类型四,三废处理流程类型五,净水流程 类型六,分离提纯和除杂流程类型七,混合物成分的确定流程类型八,定量测量流程完整版。
23⭕️ 00:30查看AI文稿AI文稿
00:30查看AI文稿AI文稿中考化学最难的八大实验题全部吃透,稳进班级前三!初三化学必考的八大实验,一、空气中氧气含量的确定。二、实验室制取氧气。三、电解水。 四、木炭还原氧化铜。五、一氧化碳还原氧化铜。六、铁的冶炼完整版。
23每周都开心吖 00:18查看AI文稿AI文稿
00:18查看AI文稿AI文稿第二题选啥?我刚才是不是说过溶解度是送分题?老师我选 a, 我 画了溶解度铝底图。你这曲线是给氧化钠和硝酸钾开了个升温派对。我觉得升温他们俩都嗨,溶解度就涨了。你看升温派对确实嗨,但硝酸钾长得比氧化钠猛多了。这题选 b 哦。
16李昂教育 00:43查看AI文稿AI文稿
00:43查看AI文稿AI文稿中考化学最难的十大计算题型全部吃透,稳进班级前三!中考化学计算常考十大题型题型一、有关化学式的计算题型。二、有关化学方程式的简单计算 题型。三,含杂质物质的化学方程式计算题型四,有关溶液溶脂质量分数的计算题型六、化学反应与溶液溶脂质量分数的综合计算 题型八、有关图像分析的计算完整版分项。
40噜噜 00:45查看AI文稿AI文稿
00:45查看AI文稿AI文稿酸的化学性质,记不住中考这八分,直接丢!酸有五大化学性质,只需记住一句口诀,酸与五物都反应,指精碱养颜,一使紫色石蕊变红,分态不变色。二和活泼金属,盐加氢气清前金属才行。 三和碱盐加水,中和反应,中考必考。四和金属氧化物,盐加水除铁锈就靠它。五和某些盐,辛盐加辛酸生成物要满足有沉淀或气体条件。注意,铜、银等氢后金属不与酸反应, 盐必须可溶或满足负分解条件。人教版中考必备收藏!背熟化学稳提分!关注我,帮你刷中考题,为你的中考加油助力!
猜你喜欢
- 2495大治老师们





