反应条件高温生成水要不要标气体符号
粉丝435获赞2159
相关视频
 01:25查看AI文稿AI文稿
01:25查看AI文稿AI文稿哈喽,大家好,我是化学马老师,今天带领大家来记忆化学方程式以及化学方程式的书写。 化学方程式是指用化学式来表示化学反应的式子,他的书写要遵循两个规则,第一要符合客观事实,第二要符合质量守恒定律。好,那书写的步骤呢?有这样几步,第一写 正确的写出反应物和生成物的化学式,第二步呢是配平,那配平的时候我们是依据的质量守恒定律当中的微观的解释部分 原。呃,在化学反应中,原子的种类、数目和质量不变啊,依据这个来进行配合好,第三 呢是要标注条件和气体符号或沉淀符号。那标注条件的时候我们可以写在等号的什么上边, 那我们什么时候标气体符号呢?反应前如果没有气体,那反应后啊,产生的气体,我们就要在这种气体的后面标上向上的箭头啊,那如果在溶液当中发生的反应, 反应前没有固体,那反应后呢?产生了固体。好,那我们就要加沉淀符号啊,你记住了吗?
17🐎小马🐎 00:47查看AI文稿AI文稿
00:47查看AI文稿AI文稿最近收到很多私信说有老师化药真的好难学啊,有那么多的化药方程式怎么都记不住,那现在有老师教你四步搞定化药方程式。好,第一步 就是你要记准反应物和生存物是什么,这个必须牢牢记住。然后第二步就是把反应物和生存物的化学室准确的写出来。第三步就是用你学到的方法把化学方程式进行配平。 然后第四步就是检查一下沉淀符号、气体符号反应条件是否正确。 要想学到更多的化学知识,记得点赞关注哦!
92中学化学尤老师 04:15查看AI文稿AI文稿
04:15查看AI文稿AI文稿对于化学反应中的放热和吸热,相信你已经有所了解,但该怎么具体的表示呢?告诉你,可以用热化学方程式来表示。所谓热化学方程式,就是表示参加反应的物质的量和反应热的关系的化学方程式, 他不仅能表明反应中的物质变化,也能表明反应中的能量变化。比如这个热化学方程式就表示在二十五摄氏度一百零一千帕的条件下,两摩尔氢气和一摩尔氧气反应生成两摩尔水,并放出五百七十一点六千焦每摩尔的能量。 但在书写的时候,还有几点需要注意。首先,热化学方程式中的化学计量数指表是相应物质的物质的量。当然了,计量数可以是整数,也可以是分数,比如这个热化学方程式中就含有分数。 哎,发现没,这两个方程式的前后物质都一样,而且状态也一样。另外,如果这个方程式的计量数都乘上二,那就和这个一样了,同时负二百八十五点八乘上二,就是负的五百七十一点六。 看来反应物和生成物的量变成了原来的两倍,那反应放出的热量也变成原来的两倍。换句话说,前面的物质量一定要和后面的反应热对应。因此,任何一个热化学方程式,从理论上讲可以写出无数个,只要物质量和反应热对应就行。 不过通常咱写的还是最简整数比对应的热化学方程式。其次,由于物质所具备的能量多少和物质本身的状态有关,那状态不同,具备的能量也就不同。比如还是这个方程式只是水变成了水蒸气,那反应热又变成了负的四百八十三 六千角美摩尔。因此,在书写热化学方程式时,一定要注明反应物和生成物的状态,其中气态可以用小写字母记忆表示,液态、固态、水溶液分别用小写的 l、 s、 a、 q 表示。 第三,由于温度和压强不同,那对应的反应热也不同,因此书写时还要注明反应的温度和压强。但有些方程式没有注明,那你就可以默认是二十五摄氏度和一百零一千八的压强。 第四,对于任意反应 x, 也就是 a 摩尔 a 和 b 摩尔 b, 反应称成 c 摩尔 c 和 d 摩尔 d, 那反应热中的单位摩尔负一次方是不是指每摩尔 a 或者指每摩尔 bcd 呢? 其实都不是,它指的是美摩尔反应,也就是美摩尔的这个反应 a 加 b, b 等于 c, c 加 d、 d。 第五,一定要标出反应热的正负,但这个正负不是指数值上的正与负,而是指反应吸热和放热。其中正的表示吸热反应负的表示放热反应。看来他们都有各自的含义,那你书写时也就不能省略。 第六,比较反应热大小时,还得带着正符号进行比较。另外,从这两个化学反应式中可以看出,参加这个反应的物质量更多,那他放出的热量也应该更多。但对比这两个德泰 h, 确实这个值要小一些。看来放出的热量越多,相应的德泰 h 越小。 第七,对于这个可逆反应的 h 值,指的是一摩尔氮气和三摩尔氢气完全反应放出的热量,而不是指达到平衡状态时的反应热。另外,逆反应的热效应和正反 的热效应是相等的,只是符号相反而已。好了,注意事项了解了,那具体书写的步骤又是怎样的呢?简单来说就四个字,写标注定写书写化学方程式 标,标出物质的状态注,注明反应的条件,也就是温度和压强。最后是定定下正确的函变。 总结一下,首先,能表示参加反应的物质的量和反应热的关系的化学方程式叫做热化学方程式。其次,书写热化学方程式时,物质的量和反应热必须对应,同时注明物质状态、反应温度和压强,并标出反应热的正负。 最后,你只要按照写标注定这四个步骤来书写就成了。说了这么多热化学方程式,本宝宝简直要考焦了,得赶紧去美容了,你先刷题去吧!
134H20 03:21查看AI文稿AI文稿
03:21查看AI文稿AI文稿观察化学方程式,向上的箭头表示产生气体,向下的箭头表示产生固体。 书写化学方程式要注意,反应条件只有一个写在等号的上方,若需要两个或多个条件,则分开写在等号上下方。 点燃不等于加热,点燃不等于燃烧,高温不等于加热。 只有生虫物中有气体时,反应物中没有气体。在气体物质的化学式右边标注向上箭头。 溶液中的反应只有生成物中有难溶的固体物质时,在固体物质的化学式右边标注 向下箭头。我们通过几个试题巩固一下本节所学,请同学读题。第一题,下列有关这个化学方程式的读法,正确的是哪一个? a 中没有说明条件 b、 c 中不能读作家,或等于应该读作和或生成,所以选 d。 第二题,下面的反应中生成物都是 c。 若 c 的化学式为 ab 二,则该反应的化学方程式是哪一个? 正确的,化学方程是两边的原则,种类和个数应该相等。二、 c 中还有两个 a 和四个 b, 所以选 c。 第三题,请同学暂停播放读题。 a。 微观图表示一个青分子与一个绿分子发生反应,图中四个圆子连在一起,是四圆子的分子,故不是两个绿化青分子,所以 a 错误。 b 微观图表示一个青分子与一个绿分子发生反应,但生成的不是两个绿化青分子,所以 b 错误。 息,微观图表示一个青分子与一个绿分子发生反应,反应生成两个绿化青分子,故息正确。 d。 微弯 图表示一个青分子与一个绿分子发生反应,但生成的不是两个绿化青分子,故地错误,所以本题选析, 我们对本节知识进行小结。化学方程式的定义是用化学式来表示化学反应的式子,它的意义有,反应物、生成物和反应条件。 参加反应的各例子的个数比,反应物和生成物之间的质量比。 亲爱的同学,本次课程的内容就讲到这里,谢谢观看,欢迎你继续关注华腾微课的其他课程,再见!
 04:02查看AI文稿AI文稿
04:02查看AI文稿AI文稿上个视频我介绍了,醇在氧气中可以燃烧,在同做催化剂的条件下可以发生催化,氧化生成醛。那还有别的氧化剂可以氧化醇吗?当然有,还记得高一时做过的乙醇与酸性高锰酸钾溶液和酸性虫各酸钾溶液的反应吗? 回顾一下,乙醇加入到酸性高木酸钾溶液后,溶液中的紫色就褪去了,发生的反应是这样的。 而乙醇加入到虫个酸钾溶液后,溶液从橙红色变成了灰绿色,发生的反应就是这样的。还记得这个反应有没有啥神奇的功效呢?对啦,就是可以用来检验司机有没有酒后驾驶。 把这俩反应合在一起,就是乙醇。乙酸性高锰酸钾溶液或酸性虫各酸钾溶液反应时直接被氧化成了乙酸。到这儿,醇被氧化 的三种情况就都介绍完了,整体回顾一下,首先,醇在氧气中能燃烧生成二氧化碳和水。其次,醇在铜或银做催化剂的条件下加热生成醛。在此,醇能被酸性高锰酸钾溶液或酸性重各酸钾溶液直接氧化生成酸。 总之,反应条件不同,生成的产物就也不同。这些内容你一定要记清楚了。最后,咱来拓展一下氧化还原反应的定义,你还记得无机化学中是咋定义的吧?氧化反应是指化合价升高被氧化,还原反应是指化合价降低被还原。 而在有机化学中还有另一种定义,通常有机物在反应中如果加入氧原子或者去掉氢原子,那就成为氧化反应。如果加入氢原子或者去掉氧原子,那就成为 还原反应。比如乙醇被氧化成乙醛时,分子是从 crh 六 o 变成了 crh 四 o, 去掉了两个氢原子,所以是氧化反应。这实际上和无机种氧化反应的定义本质是一样的, 发现没,乙醇中碳原子的平均价太为负二价,而乙醛中碳原子的平均价太为负一价,所以碳元素的化合价从负二价变为负一价,化合价升高是氧化反应。 看来,在有机化学中,我们只是更关注原子的转移情况。实际上,有机物中加入氧原子或者去掉氢原子,本质上就是化合价升高的过程。同样加入氢原子或去掉氧原子,就是化合价降低的过程。 那么问题来了,乙醇脱掉一分子水时,既去掉了氢原子,同时也去掉了氧原子,如果按照去氢来说,那 应该为氧化反应。如果按照去氧来说,那应该是还原反应。但这样不就矛盾了吗?到底是氧化还是还原呢?其实这个就不能从氧化还原反应的角度来定义他的反应类型了。 另外,在无机化学中,我们通常说氧化还原反应,也就是把氧化和还原结合起来说。 而在有机化学中,咱们通常说的是该反应为氧化反应或还原反应,也就是把氧化和还原分开来说。 因为在实际的情况中,咱们更关注有机物发生了氧化还是还原。比如前面说过,从乙醇变成乙醛,去了两个氢,发生氧化反应,那通常就说这个反应为氧化反应。 如果把这个反应反过来,从乙醛变成乙醇,那就是加氢发生还原反应,所以就说他是还原 反应,这点你要搞清楚好了,总结一下,纯被氧化共有三种情况,首先,纯在氧气中能燃烧生成二氧化碳和水。其次,纯在铜或银做催化剂的时候加热生成醛。 再次,纯能被酸性高锰酸钾溶液或酸性虫各酸钾溶液直接氧化生成酸。另外,在有机化学中,对于氧化还原反应还有另一种定义, 那就是有机物在反应中加氧或者去氢就是氧化反应,加氢或去氧就是还原反应。而且和无机化学不同的是,有机化学中氧化和还原反应是分开说的。好了,就讲到这里,赶紧去刷题吧!
65H20 04:31查看AI文稿AI文稿
04:31查看AI文稿AI文稿上个视频单学习了书写离子方程式的方法,那书写时还需要注意哪些问题呢?首先,不是所有的化学反应都能写离子方程式,比如不在溶液中进行的反应,不能写离子方程式。 举个例子,绿化固体与氢氧化钙固体混合加热,这时固体和固体的反应不在溶液中进行,所以不能写离子方程式。 类似的,含有气体与气体的反应,比如氢气和氯气反应生成氯化氢。还有气体和固体的反应,比如氢气还原氧化铜以后还会学到固体与脓硫酸的反应,这些都不能写成粒子方程式。 书写离子方程式的时候还要注意,酸食盐在溶液中发生反应的时候,弱酸的酸石根离子不拆,强酸的酸石根离子拆开。比如写出碳酸氢钠与纤酸反应的离子方程式, 应该就是碳酸氢根和氢离子反应生成二氧化碳和水。这里的碳酸氢根是弱酸的,酸蚀根不拆。而硫酸氢钠和氢氧化钠的反应呢?硫酸氢钠是强酸的酸,食盐完全电离,所以就要写成氢离子和氢氧根反应生成水。 以上就是书写离子方程式时要注意的问题,你可能会问,能写化学方程式不就得了吗?干嘛还要写离子方程式呢?单分析一下写离子方程式有何意义?首先,离子方程式表示的是实际参加反应的离子之间的反应,他能接是反应的本质。 咱先写几个离子半程序。第一个,硫酸和氢氧化拉的反应,写出来是氢离子和氢氧根生成水, 带来硝酸和氢氧化钾的反应,哎,也是氢离子和氢氧根反应生成水。后面两个念仍然是氢离子和氢氧根离子生成水的反应。 明明写的是不同的反应,但写出来的离子方程式却是一样的。看来离子方程式不仅可以表示一个具体反应,还能表示同一类型的反应。 那是不是所有的酸碱中和反应都能用这个例子方程式表示呢?答案是否定的,比如醋酸溶液和氢氧化钠的反应,醋酸是弱酸男电离,不能拆,因此写出来就是这样的。 再看这个氢氧化铜和盐酸反应的离子方程式怎么写呢?要知道,氢氧化铜难溶于水,不能拆,应该这么写。所以这个离子方程式只能表示强酸与强碱反应,生成可溶性盐和水的反应。 看来,离子方程式不仅能揭示反应的本质,还能表示同一类型的反应。以前你学过不分解反应发生的条件是生成沉淀气体或者水。 类似的,发生离子反应的条件是生成难溶物或微溶物、生成气体或挥发性物质以及生成难电里的物质。 咱来逐个分析一下,生成难溶物或微溶物的离子都有啥呢?比如倍离子和碳酸钙离子,生成碳酸贝沉淀银离子和绿离子。生成氯化银。沉淀钙离子和硫酸钙离子。生成硫酸钙微溶物。 再看生成气体或挥发性物质的离子都有哪些呢?比如氢离子和碳酸根离子或碳酸氢根离子都会生成二氧化碳气体,氢离子和硫离子生成硫化性气体、氢离子与亚硫酸跟离子或亚硫酸氢跟离子会生成二氧化硫气体等。 第三种情况是生成男电离的物质,比如青离子和醋酸跟离子生成醋酸,醋酸是弱酸男电离。还有氨根离子和氢氧离子生成一水合氨 电离,以及青离子和氢氧根离子生成水分子。除了这三个发生条件,离子反应发生的条件还有可能是氧化还原反应,这个会在以后的视频中学习。 以上是离子反应发生的条件,所以这些离子在溶液中也不能大量共存。为了更好的判断哪些是难溶物、微溶物,你要记清这些物质的溶解性哦。 好了,这个视频的全部内容就讲到这里,咱来回顾一下。书写离子方程式要注意不在溶液中进行的反应,不写离子方程式,弱酸的酸石根不能拆。 离子方程式的意义是不仅可以揭示反应本质,还可以表示统一类型的反应,比如青离子和青氧根生成水,可以表示强酸和强碱生成可溶性盐和水的反应。那离子反应发生的条件是生成难溶物或微溶物、 生成气体或挥发性物质,以及生成难炼力的物质。以后还会学习发生氧化还原反应的情况。 另外,如果离子之间能发生离子反应,说明这些离子在溶液中不能大量共存。可以通过记住溶解性表,方便判断哪些是男人物。好了,就说到这里,说下体质吧。
1044在线学习高中部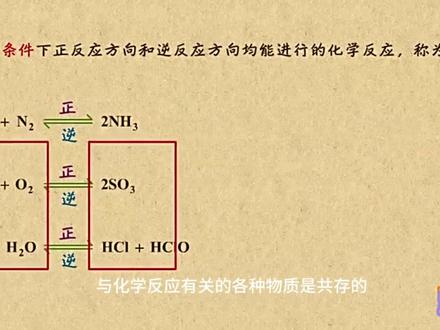 04:52查看AI文稿AI文稿
04:52查看AI文稿AI文稿之前你已经学习了很多的化学反应,咱知道在发生这些化学反应时,物质之间是按照一定的计量数之比来完成的。那在实际的反应过程中,是不是所有的反应物都会按照计量数之比全部转化为生成物呢? 根据科学研究表明,其实很多化学反应在进行时都具有可逆性,也就是正向反应和逆向反应在同时进行,只是可逆的程度有所不同,并且差异很大而已。比如氢气和氮气合成氨气,二氧化硫和氧气化合生成三氧化硫,氯气溶于水生成盐酸和自氯酸等。 咱把这些在同一条件下,正反应和逆反应方向均能进行的化学反应称为可逆反应。那可逆反应有哪些特点呢?首先,向相反的方向进行的俩反应必须在同一条件下同时进行。那这两 组反应是可逆反应吗?先看这组,氢气和氧气生成水的条件是点燃,而反过来的条件是电解,所以反应条件不同,当然不是可逆反应。再看这组,咱知道充电时要外加电源,而放电时不需要,所以他俩也不是可逆反应。 总之,在不同条件下,能向两个方向进行的反应不能乘坐可逆反应。其次,书写时这里都是用可逆符号连接的,他的两边互为反应物和生成物。通常把从左向右的反应称为正反应,从右向左的反应称为逆反应。 虽然绝大多数化学反应都有一定的可逆性,但有些反应的可逆性小,比如氢气和氯气生成氯化氢,银离子和氯离子生成氯化因沉淀等,通常把他们视为不可逆反应。 等号连接表示全部转化为生成物。除此之外,在反应体系中,与化学反应有关的各种物质是共存的,也就是反应物不能全部转化为生成物,生成物也不能全部转化为反应物。了解了可逆反应的特点后,咱再来看看正反应和逆反应的速率是如何变化的。 不妨以这个可逆反应为例,如果开始只有反应物,没有生成物,那此时 ab 的浓度最大,正反应速率也就最大,而 c 和 d 的起始浓度为零,也就是逆反应的速率为零。用图表示。就是这样, 随着反应的进行,反应物浓度不断减小,生成物浓度不断增大,那正反应速率就越来越小,逆反应速率反而越来越大。当反应进行到某一时刻时,他俩就相等了,此时反应物的浓度与生成物的浓度不再 改变,达到一种表面静置状态,咱称这种状态为化学平衡状态,简称化学平衡。同理,如果开始只有生成物,没有反应物,那一段时间后同样可达到平衡。 如果给化学平衡再下个定义,那就是指在一定条件下的可逆反应。同一种物质的正反应和逆反应速率相等,混合物中各组分浓度保持不变的状态, 这个状态具有逆、等动、病变这五大特征。逆化学平衡研究的对象一定是可逆反应,可逆反应才有化学平衡状态。 等平衡时,同一种物质的正反应和逆反应速率相等,也就是单位时间内消耗这种物质和生成这种物质的物质的量相等,从而使这种物质的物质的量保持不变 动平衡时,反应仍在不断的进行,只是正极反应速率相等,但不等于零,是一个动态平衡。 定平和时,反应混合物中各组分的物质的量、质量都不变,因此浓度保持一定百分,含量保持一定,但不一定相等。 变。外界条件改变时,平衡可能被破坏,可能向正反应方向进行,也可能向逆反应方向进行,但过一段时间后又可达到正反应速率和逆反应速率相等,也就是在新的条件下建立新的化学平衡。 换句话说,化学平衡就是可逆反应。达到一种特殊的状态,是在给定的条件下,化学反应能做到或完成的最大程度,也就是该反应进行的限度。他决定了反应物在该条件下的最大转化率。但如果改变反应的条件,就可以 可以在一定程度上改变一个化学反应的限度,也就是改变该反应的化学平衡状态。所以,通过调控反应的条件,可使他朝着咱想要的方向进行。因此,研究化学反应的限度对于化学研究和化工生产都有着重要的意义。 又到了总结时间,首先,可逆反应是在同一条件下向正反应和逆反应方向均能进行的化学反应。注意,必须是在同一条件下并用可逆符号连接。 其次,当可逆反应达到一定限度时,正逆反应速率相等,达到了化学平衡状态,这个状态具有逆、等、动、定、变这五大特征。好了,就说这么多,快去刷题吧!
65H20 01:36
01:36 02:36查看AI文稿AI文稿
02:36查看AI文稿AI文稿哈喽,大家好,今天我们来看非常容易混淆的铁的氧化物,这三种氧化物分别是氧化亚铁、氧化铁和四氧化三铁。我们先来看它的俗名,氧化亚铁没有俗名,氧化铁叫做铁红,也可以称之为赤铁矿。四氧化三铁叫做磁性氧化铁色肽分别是氧化亚铁黑色粉末、氧化铁 红棕色粉末,四氧化三铁黑色粉末。氧化亚铁中的铁是正二价的,氧化铁中铁是正三价的,而四氧化三铁我们可以把它看作由一个氧化亚铁和一个氧化铁构成,所以四氧化三铁有一个正二价的铁,两个正三价的铁与氢气反应的方程式,这个氧化亚铁跟氢气高温反映生成铁和水 这个方程,这个是你经常容易忘的,接下来与氢气反应都可以把铁的氧化物还原成铁单质。氧化亚铁和氢气在高温条件下生成铁和水。氧化铁和三分子氢气结合生成两个铁和三份水。四氧化三铁和四份氢气在高温条件 下生成三份铁和四分子的税。再来看稳定性,氧化亚铁并不稳定,他在氧气的作用下,通过加热能够得到四氧化三铁,把这个方程式配平,那根据这个方程式,我们就已经全部捋过如何制备四氧化三铁了,老师在这里总结一下,第一种方法就是铁直接与氧气点燃, 铁在氧气中燃烧生成的是四氧化三铁。第二种方法是铁与水蒸气反应,注意这里面一定是气态的水能够得到四氧化三铁黑色粉末。最后就是我们这一个方程式所说的氧化亚铁和氧气 通过加热得到的是四氧化三铁,那氧化铁和四氧化三铁相对比较稳定。再来看与盐酸或与硒硫酸的反应,氧化亚铁与两份氢离子反应生成二价的亚铁离子和一份水。氧化铁和六份氢离子反应生成的是两份三价铁和三份水。而四氧化三铁呢?我们刚 刚才说可以把它看成一个氧化亚铁和一个氧化铁,那么他们两个相加就一共需要八份氢离子,所以四氧化三铁需要八份氢离子反应得到一个亚铁离子,两个铁离子和四份水,实际上就是把这两个反应的产物加起来了。 好,再来看与硝酸是如何反应的,因为硝酸它具有氧化性,所以可以把正二价的亚铁氧化成正三价的铁,并且生成一氧化氮。这个方程式的配瓶你一定要会。 再来看第二个氧化铁和六个氢离子,直接就生成两个三价铁和三份水,因为氧化铁中的铁本身就是正三价的了,他的化价不会再升高了,所以这里面不体现硝酸的氧化性。 而四氧化三铁我刚才说他可以看作有一份氧化亚铁,所以这个反应依然涉及到氧化还原这个方式,自己回去试着配一下。老师直接把答案写在这里,三份四氧化三铁加二十八个硝酸,生成的是九份硝酸铁,一份一氧化氮和十四份水,你学会了吗?
80教化学的红柚学姐 00:45
00:45
猜你喜欢
- 2508大治老师们



