物质的量电子数怎么算
粉丝11.5万获赞95.5万
相关视频
 16:47查看AI文稿AI文稿
16:47查看AI文稿AI文稿同学们大家好,这节课我们一起来学习物质的量。第一课时, 我们生活在物质生活非常富足的时代,我们身边琳琅满目的物品大多都是以什么方式计量的呢?有什么规律? 大家不难发现,大件物品一般按单个计量,比如一台电视、一张桌子、一部手机。比较小的物品通常按集团计量, 比如一千个大米,我们几乎从不一粒一粒的数,比如一盒图钉,一盒签字笔, 这些比较小的物品按集团计量可能更加方便。那么你有没有想过,我们最熟悉的 水又是如何计量的呢?水是大家很熟悉也很重要的物质,由水分子组成,那么水如何计量? 有同学说,一吨水,一千克水,有同学说一升水,一毫升水。那么无论按质量还是按体积,这些水中又分别含有多少个水分子呢? 我们看一吨水约含有三点三四乘以十的二十八次方个水分子, 一千克和一升水中均约含有三点三四乘以十的二十五次方个水分子。 一毫升水约含有三点三四乘以十的二十二次方个水分子。 如此庞大的数字,我们用起来很不方便,所以对于这些比较小的例子,通常以集团计量,建立堆量,从而化繁为简。 一九七一年在第十四届国际计量大会上正式宣布了物质的量是国际单位制中的一个基本物理量,其单位为摩尔。物质的量就是我们对这些特别小的例子建立的堆量。 国际单位制有七个基本物理量,分别是长度、质量、时间、电流强度、热力学、温度、 物质的量、发光强度。我们这节课就来学习其中一个物理量。物质的量极其 单位摩尔。物质的量表示含有一定数目粒子的集合体,符号为小写 n, 单位摩尔,简称摩。 我们用摩尔来计量一定数目的例子。我们熟悉的计量方式及数目为,一盒签字笔十二支,一包白纸五百张,一盒区别针一百个。那么一模例子有多少个呢? 国际上规定,一模粒子结合体所含的粒子数约为六点零二乘以十的二十三次方。一模任何粒子的粒子数叫做阿福加德罗,常数,符号为 na, 通常用六点零二乘以十的二十三次方。美模表示,我们一起来回顾历史。阿福加德罗,意大利物理学家、化学家,一七七六年生于意大利都陵市。 阿福加德罗毕生致力于化学和物理学中关于原子论的研究。他的研究对科学的发展,对微观世界的探索起了重大的推动作用。为了纪念他,后人以他的姓氏命名阿福加德罗常数 阿福加德罗长树。他究竟有多大呢? 让我们一起来感受阿福家的罗长树。截止到二零二零年三月, 全球人口将近七十六亿。如果把六点零二乘十的二十三次方厘米给全球七十六亿人吃,每人每天吃一斤,大约可以吃多少年呢? 乘凉六十粒某大米,约为一克计算六点零二乘十的二十三次方,除以六十乘五百乘七十六乘十的八次方,乘三百六十五的机,约等于七百多万年。 六点零二乘十的二十三次方厘米给全球七十六亿人吃,大约可以吃七百多万年。 如果把六点零二乘十的二十三次三个一角硬币直径约一点 点九厘米排成一行,可以绕地球赤道多少圈呐?赤道周长四万零七十六公里。 让我来给大家算一算吧!一点九乘十的负五次方乘六点零二乘十的二十三次方除以四万零七十六,约等于两百八十五万亿 六点零二乘十的二十三次方各一角硬币排成一行,可以绕地球赤道大约两百八十五万一圈。 我们看到,如果描述宏观物质,阿福加德罗常数大到超乎想象,所以作为物质的量的单位,摩尔通常用于记 量原子分子、离子、原子团、电子、质子、中子等。微观粒子,如一模儿铁圆子、一模儿养分子、一模儿那离子、一模儿硫酸根离子等。 下面我们一起来完成以下练习。一、一模水中约含有六点零二乘以十的二十三次方个水分子。 二、零点五摩尔氢氧化钠中约含有三点零一乘以十的二十三次方个纳离子。 三、六点零二乘以十的二十三次方个氢气分子相当于一摩尔氢气。四、一点二零四 乘以十的二十四次方个硝酸根离子相当于两摩尔硝酸根。那么你能发现物质的量与粒子个数之间的转化规律是什么吗? 物质的量与粒子个数之间的关系是,物质的量乘以阿弗加德罗常数,即 na 可得到粒子数。反之,粒子数除以阿弗加德罗常数,则可得到物质的量。 公式,物质的量等于粒子数除以阿福加的罗长数。 我们知道一个水分子中有两个青原子,一个氧原子扩大,六点零二乘以十的二十三次方背可以 看成一乘以六点零二乘以十的二十三次方个。水分子中有二乘以六点零二乘以十的二十三次方个轻圆子,一乘以六点零二乘以十的二十三次方个养元子, 即一模而水分子中有两模而清圆子,一模而养圆子。我们看到了什么规律呢?对粒子数之比等于物质的量之比。 一抹水代表哪些含义呢?我们一起来分享,看看同学们怎么说。 水分子的物质的量为易摩尔,易摩尔水所含的分子数约为六点零二乘以十的二十三次方个。易摩尔水中所含的 清源子数约为一点二零四乘以十的二十四次方个。一模儿水中所含的氧源子数约为六点零二乘以十的二十三次方个。一模儿水中含有两模二清源子,一模儿氧源子。 我们来梳理一下,关于一抹而水,我们究竟能知道什么? 一抹而水,水分子的物质的量为一抹而一抹而水所含的分子数约为六点零二乘以十的二十三次方个。 一抹水中所含的清源子数约为一点二零四乘以十的二十四次方格,所含的氧源子数约为六点零二乘以十的二十三次方格。 同时得到一个水分子中有两个清原子,一个养原子,一模水分子中含有两膜清原子,一模养原子, 两模清原子和一模养原子又组成了一模水。那么一模水的质量是多少呢? 质量才是我们可测的数据。方法一,如果利用一个水分子的质量乘以水分子的个数,可以算出质量。方法二可以总结规律,方法三可以通过数学推倒。 这节课我们主要来讨论物质的量与质量之间有哪些规律。在教材第五十一页,图二杠 二一图片中展示了物质的量为益摩尔的几种物质,并标注了他们的质量。你能发现有哪些规律吗? 我们将图中数据以图表的形式展示,写出他们的相对原子或分子质量,铁五十六,铜六十四,铝二十七,芯六十五,硫三十二,氯化钠五十八点五, 水十八,蔗糖三百四十二。同学们,我们一起来看 其中每一种物质。一、摩尔的质量,其数值与它的相对原子或分子质量相同。我们把单位物质 的量的物质所具有的质量定义为摩尔质量,符号为大写 m。 常用单位克美膜表达是摩尔质量等于质量比物质的量。 注意,摩尔质量数值上等于相对原子或分子质量,但意义不同。摩尔质量有单位克美摩,相对原子或分子质量是个笔直,没有单位。 我们来看,通过已知物质的相对原子或分子质量,我们可以直接得到他们的摩尔质量的数值。 再加上单位克美膜,比如水的摩尔质量为十八克美膜,硫酸的摩尔 质量为九十八克美膜,轻氧化纳的摩尔质量为四十克美膜。 有了摩尔质量,我们就可以将物质的量与质量关联起来,物质的量乘以他的摩尔质量,极为质量。反之,质量除以摩尔质量,得到物质的量 公式,物质的量等于质量比摩尔质量。 刚才我们已经讨论了一抹水的物质的量与粒子数之间的关系,我们继续来完善物质的量与质量之间的关系, 一抹而水,根据公式,质量等于物质的量乘以摩尔质量,水的摩尔质量为十八克,美膜 算出一抹而水的质量为十八克。化学是一门充满神奇色彩的科学,他通过物质组成、粒子分析,引导我们探索那些肉眼看不见的粒子的特征和行为,引导的人们认识整个物质世界。 我们看到物质的量将微观的粒子数和宏观的质量连立起来,起到了重要的桥梁作用,帮助我们更加清晰的认识微观世界, 建够了这样一张关系网,粒子间的转化关系一目了然。 如果我们从微观粒子出发,已知粒子数有六点零二 乘以十的二十三次方个水分子,利用粒子数与物质的量之间的关系,粒子数除以阿弗加德罗常数等于水分子的物质的量,即一抹而水, 借助于物质的量的桥梁作用,利用质量等于物质的量乘以摩尔质量求出十八克水,同时也可以分析水的粒子组成。如果我们从宏观物质的质量出发, 已知水的质量十八克,利用物质的量等于质量除以摩尔质量 算出一抹而水,则同样可求一抹而水中约有六点零二乘以十的二十三次方个水分子 一模,而水中有两模而清原子和一模而养原子,约含有一点二零四乘以十的二十四次方个清原子, 六点零二乘以十的二十三次方个养元子。由此可见,无论我们从微观粒子或是宏观物质出发,借助物质的量是核心, 这个问题我们来讨论。从多水平定量认识物质,分析物质与一抹而水含有相同氧原子数的氧气的质量是多少呢? 一模儿水中含有一模儿养原子,一模儿养原子约为六点零二乘以十的二十三次方个养原子相当于零点儿五模儿氧气分子 乘以摩尔质量三十二克。美膜则与一模而水含有相同氧源子数的氧气的质量为十六克。 学习了物质的量这个物理量,我们可以轻松的将物质的质量和粒子数连理起来。比如我们拿到一份铝,我们可以称量它的质量,利用质量除以摩尔质量计算出物质的量 乘以阿福家的罗长数算出铝原子的粒子数。物质的量是联系宏观和微观的重要桥梁。 我们小结一下本节课所学的知识。物质的量为描述微观粒子的一个基本物理量 乘以阿弗加德罗常数得到粒子数乘以摩尔质量得到物质的质量。反过来,粒子数除以阿弗加德罗常数,质量除以摩尔质量得到物质的量。 物质的量承载着微观粒子与宏观物质之间的桥梁作用,有助于我们更全面、更深刻的认识整个物质世界,将物质之间的定性分析与定量数据完美融合,为我们打开了一个探索物质世界的新窗口。 课后思考,在科学研究或实际生产中,涉及气态物质时,测量体积往往比称量质量更方便。 那么气体体积与物质的量之间又有什么关系呢?我们下节课继续学习,同学们,再见。
5343名师课堂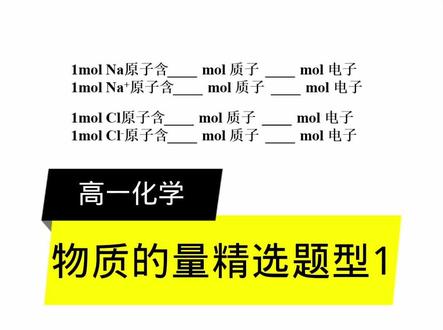 02:53查看AI文稿AI文稿
02:53查看AI文稿AI文稿直子数电子数问题,直子数等于原子序数等于核电核数等于核外电子数,那阳离子的电子数等于直子数减电合数。阴离子直子电子数等于直子数加电合数, 那是十一号元素,所以一模二。那原子含有的直子数是十一门,电子数是十一门。 一门,那离子直子数不变,还为十一门,电子数发生变化了。阳离子电子数等于直子数减变和数,所以电子数是十门。 伊木尔绿原子直子数绿是十七号元素,所以直子数是十七门,电子数是十七门。绿离子 直子数不变和绿圆子是十七门电子数。阴离子是加上电盒数,所以是十八门。 一抹而水直子数我们说轻是一,仰是八,所以一抹而水含石墨尔直子,石墨尔电子 伊木尔七样根。直子数八加一是九门,二直子那印离子在伊木尔复电盒,所以加一是十码电子伊木尔安根,但是七加一,所以直子数是十一门,电子数减一是十门。 十八克水所含的电子数为多少?我们知道一门水所含的电子数,刚才求出来的是十,现在我想知道十八克水是几膜,然后他俩 一成是不就可以了?所以要求水的摩尔质量。水的摩尔质量轻是一,一氧是八十六,所以它的摩尔质量是十八克。美膜对十八克水,它的物质的量是十八比十八, 那么一膜水含的电子数是十膜,那么这么多膜乘,所以是十膜。十八 na 正确, 十八克重水所含的电子数刀是一,二氧是八十六, 一模,而重水所含的电子数是一乘二加八是没变的,是十十八克是几膜。首先求出他的摩尔质量等于摩尔质量,是不是按左上 上角算是二乘二加十六是二十克美膜,所以十八克是几膜呢?是十八,比上二十 一摩尔重水含十摩尔电子,他这么多膜含几摩尔电子,求出来是九摩,九摩就是九恩伟各,所以错误。
508高中化学依依老师 11:39查看AI文稿AI文稿
11:39查看AI文稿AI文稿嗨,大家好,今天陈老师带领大家学习高中化学中特别重要的高考必考的知识模块物质的量,学物质的量。之前,我们先来过渡一下 水龙头地下的一滴水大概有零点零五克,你知不知道这零点零五克的水中含有了多少个水分子?如果想要数清楚水分子的个数,又需要多少人来数多少天?我现在告诉你们,一滴水 它里面大概含了一点七乘以十的二十一次方个税分子。可能有些人对一点七乘以十的二十一次方没有概念,现在我们来看一下这一点七乘以十的二十一次 方个水分子,让全球七十亿的人去数,每人每分钟数一百个,日夜不停,则需要四千五百年才能完成。可能吗?这是不可能的,我们人类完不成啊。为什么这么说呢?我们总得吃喝拉撒睡吧, 我们的寿命也没有这么久啊,是不是?所以这是一个好大的工程,这是一个人类凭自身能力不可能完成的工程,既然没有办法完成,我们来计量微观粒子个数 的时候,还能用个位单位吗?我们如果不能用个位单位,又该如何计量微观粒子的个数呢?在现实生活中,某大型超市,他进货的时候,鸡蛋他是按个进的吗?方便面他是按袋进的吗?啤酒饮料 是按瓶进的吗?显然不是,鸡蛋规定一百枚为一筐,他是按筐进。某超市说来给我进一百筐鸡蛋方便面二十四袋为一箱,按箱进。说来上一百箱方便面,还有啤酒饮料,二十瓶一件,说各来一百件, 那我们就知道他们进货的时候就不是以个数来计算的,都是以像框、箱 件这种为单位来进货的,把具有相同性质的个体以一定的数目聚集起来形成的整体就叫做集合体。 我们身边的集合体很多呀,例如我们规定好每一个班有五十个学生,那这五十个学生所形成的一个班级就是一个集合体啊。 这些相框题啊,答啊、件啊,都是规定好装一定数目的物品的集合体。既然微观粒子不能以个为单位,那能不能以集合体为单位呢?例如我们规定好了每一个集合体中微观粒子的个数, 想要求微观粒子的总数,我们来数集合体不很快吗?很快就能计算出微观粒子的总数了,不是吗?那如果有人问你某学校高一总共有多少人, 那这个话你还要去数是不是?那怎么样才能最快的呢?我就规定好每个班级有五十个人,我就数班级数不就行了,很快我就能知道所有的总人数了,是不是?那微观例子也是这个道理。所以啊, 我们看一下我们化学中常用的物理量,物质的量。先看一下物质的量的概念,物质的量表示含有一定树木。微观粒子的集合体的多少。物质的量表示的是集合体的多少,它的符号是 n, 单位是膜儿,简称膜,我们平常写成 mol 啊。这样我们就将用肉眼难以看见的难以称量的微观粒子和用肉眼可见的可称量的宏观物质,利用物质的量联系了起来。 目前国际上流通了有七个基本物理量,分别是长度、质量、时间、电流强度、热力学、温度、发光强度啊,还有一个,那像长度、质量、电流强度,这些 我们都不陌生,已经学过了。虽说热力学、温度和发光强度我们没学过,但是从字面意思我们也能理解,无非就是温度和光亮的程度啊。那还有一个就是我们今天所学的物质的量。 物质的量有小写的 n 表示,他的单位名称是摩尔,也可以简称模。张卫的符号是 mol, 他也是国际单位至七个基本物理量之一。 我们已经知道了物质的量是微观粒子集合体的多少,所以如果有一个微观粒子的集合体,小 n 就等于一模二, 如果有两个微观粒子集合体,小 n 就等于两模儿。以此类推,如果有 x 个微观粒子集合体,小 n 就等于 x 模儿。好,国际上规 规定一模二,任何微观粒子集合体所含的粒子数都约为六点零二乘以十的二十三次方个,这是国际上规定的啊。哦,那这个微观粒子代表什么呢? 待会我们会解释啊。会解释可和现实生活中宏观可见的物质不一样,像宏观可见的城乡的啊。集合体我们就以 相这个词来表示。乘件的集合体,我们就以件来表示。乘答的集合题,我们就以答来表示。那在微观世界里, 所有的集合体就不会分这么详细啊,件相答题都没有这些字眼了,用什么呀,就用物质的量啊。物质的量代表所有微观例子的集合体。讲,一模二 hro 约等于六点 零二乘以十的二十三次方个水分子,一模二 fe 约等于六点零二乘以十的二十三次方个。铁圆子一模二 so 四二负,约等于六点零二乘以十的二十三次方个。硫酸根一模二 h 正 于等于六点零二乘以十的二十三次方个。清离子,这个六点零二乘以十的二十三次方,可能好多同学没有概念啊,咱们用大米来举个例子,如果有一堆大米,有多少个呢?六点零二乘十的二十三次方个,那么这么多大米到底是多大一堆呢? 咱这么说吧,六点零二诚实的二十三次方力大米有全球七十亿人吃,每人每天吃一斤,大概要吃十二万年才能吃得完。我们就可以看出六点零二诚实的二十三次方 是一个多么庞大的数字啊。关于物质的量的以以下几点啊,我们要说明一下。首先,物质的量是一个物理量的全称,这是个全称,是一个专有名词,不能分割, 不能删减,也不能插入其他字体。有的同学说,老师,我能不能说成物质的量不可以,能不能说成物质的质量不可以, 能不能说成物质的数量也不可以?专有名词啊,不能删减啊!物质的量只描述微观粒子,我们刚刚已经说了微粒、微粒,微观粒子,到底什么是微观粒子呢? 像原子分子、离子,原子团,原子团是哪些呢?硫酸根,碳酸根,硝酸根等等,谋什么什么根啊,这些都是原子团,还有质子、 中子和电子,这些都是微观粒子,不能描述红光物质。什么是红光物质呢?就是有这些微观粒子所形成的物质就是红光物质。第二,用摩尔为单位,表明 某物质的物质的量实,你必须指明威力的名称,或者是符号,或者是化学师。例如,一模二 h 表示的是一模二清原子一模二 h 正表示一模二清,离子一模二 h 二 角马二啊,表示一模二清气分子,而你不能用一模二清这个汉字,清不能这么表示,这么表示是含糊,没有意义的。什么意思呢?他指代不明。这一摸二清指的到底是一摸二清原字,一摸清离子,一摸清气分子,你知道是哪一个吗? 并不知道,所以我们不能这么写啊。四、物质的量计量是粒子的集合体,它是集合体的多少啊?不是单个粒子的多少,它的数值可以是整数,也可以是小数。这个该怎么说呢?例如,你家里买了三箱方便面, 有一箱你已经吃了一半了。现在如果有人问你家里现在还有多少方便面啊?那你会说,我家里还有两箱半,那这个半箱就是一个小数,它就代表着有零点五个集合体,集合体可以是个整数,也可以是个小数。那不满一个集合体,我们不就用小数表示了吗? 我们来判断一下下列叙述他是否正确以及他错误的原因。第一个,摩尔是七个基本物理量之一,这显然是 是错误的。为啥呢?因为物质的量才是七个基本物理量之一。摩尔是什么呀?摩尔只是物质的量的单位,就相当于 m, 他是米的单位,而他不是物理量啊。 好物质的量就是物质的质量,这个也是错误的。我们刚刚说了,物质的量是一个专有名词,它不可以填字,也不可以减少字啊,这是微观粒子集合体的个数。 咱一摸美女,美女啊,我还一摸帅哥呢。一摸美女是什么呀?皇冠物质了是不是 好?所以这个也是错误的啊。四、一母二清。我们刚刚说了,这个清到底指的是清原子、清分子、丁离子,你清楚吗?不清楚,所以这也是错误的, 没有指明到底是什么啊,指代不明。我们再来看一下下列说法是否正确。 a。 摩尔沙子肯定是错误的, 因为沙子是宏观物质,那你要想表示的时候要怎么表示呢?就要看沙子的组成成分。我们知道沙子里有二氧化硅,那你可以说一模二二氧化硅,但你不能说一模二沙子 二,一模二养。刚刚说了,这种只带不明养分子,养离子还是养原子?不知道啊,所以他是错误的。三、一母二 hro, 这个可以。那可能有的同学说,老师,水也是宏观物质啊,它代表的是一模儿水分子啊,一模儿 h o 妇,这个也可以,这指的是一模儿清养根,一模儿 f e, 这个是指的 是伊摩尔铁原子。到底该怎么正确书写呢?我们把公式写出来啊,正确的书写是恩加摩尔加威力的化学符号,这个化学符号呢,可以是化学式,也可以是离子符号。 你如果不想这么写呢?你想写汉字,你就要写恩加摩尔加威力的文字全称,知道什么叫文字全称吗?例如这里你可以写一模二氧气、一模二氧离子、 一摸痒圆子,你把汉字给他全写上啊,才能表示是正确的写法。这个视频老师就分享到这里,如果有疑问可以向老师留言询问哦,拜拜! 哇哦,不错哟。
1214姐姐教化学哦 20:37查看AI文稿AI文稿
20:37查看AI文稿AI文稿各位同学大家好,我是微课网化学主讲老师王木,今天我们一块来看一下物质的量浓度相关的问题。 关于物质的量浓度,他这里边的重难点主要是物质的量浓度的计算方法,以及在整个溶液当中,我进行均分和稀释的时候,会有什么样对于浓度的影响。 然后呢,对于比较难的地方,其实还是在整个计算当中,他的细节注意事项有哪些,我们会需要通过时间给大家一点一点来分析。那最后呢,高频的考点其实就是物质的量浓度相关的计算了, 那我们就直接来进入重点,我们来看一下物质的量浓度的基本定义。对于物质的量浓度来说,呃,他的定义啊,其实跟我们曾经学过的一个叫质量分数的东西,我觉得差不太多, 它表示是什么呀?它表示的是单位体积的溶液中所含溶质的物质的量。啥意思呢?我取出了一升的溶液,这里边有溶质几摩尔, 哎,相当于啊,我把曾经的质量分数给大家做了一个些许的调整,就变成了这样一个新的物理量。那其实我光说这个定义啊,没什么太大的意义,我们直接把公式给大家,这个小 c 一般就是我们所谓的浓度, 它等于什么呢?它等于物质的量,比上我们溶液的体积 v 即可,这个物质的量,注意是溶质的物质的量,这个 v 表示的是溶液的体积,那对应的单位物质的量是摩尔,体积是升,那么摩尔每升这个单位就出来了。但是大家一定要 要注意,在之前的课程当中,我们曾经学过一个叫气体摩尔体积的东西,气体摩尔体积,它的单位是声美摩尔, 来,那表示什么含义?表示每摩尔气体所占的体积是多少多少升,那么跟我们的这个摩尔每升的单位刚好是反着的, 而与此同时,这摩尔美声浓度的这个一个单位用的反而是更多的,所以大家千万不要把这两个单位给弄混了,大家一定要记清楚。 ok, 那把这个放在一边, 关于物质量浓度的一些基本定义计算方法其实摆在这。那我问大家一个问题啊,比如说我现在有一摩尔的氯化钠,我把它配成了一个零点五升的 溶液,那你说它的浓度应该是多少啊?你是不是用物质的量一摩尔除以体积零点五升,结果一除,哎,两摩尔每升,那是不是就是这样一份氯化钠溶液,它的浓度,它的物质的量浓度 就出来了? ok, 来,这一页的基本计算应该不会有什么太多的问题值得去说到来,我们重点还是把它放到具体的问题里边,来,看一下他可能存在哪些注意的点来,在这里边,我希望大家先判断一下这两句话的说法是否正确。 第一句话,二十克氢氧化钠溶于零点五升水中得到的溶液物质的量浓度为一模每升。来,我们想一想哈,二十克,嗯,氢氧化钠相对分子 质量是四十,那二十克刚好应该是零点五膜,那底下甭看了,底下二十克也零点五膜嘛。 ok, 来, 零点五模,零点五升一出,哎,一模每升,零点五模,零点五升,哎,一模每升,哎,那这两句话不都对的吗?来,我们仔细来看这问题在哪?这两句话区别在什么地? 你发现底下这句话都是一样的,得到的,得到了,一毛没剩,都是一样的。上面这句话,二十克氢氧化钠,没错,这是溶解在零点五升的水中,这是溶于水,得到零点五升的溶液。 来,那这就有一个问题了,哪种说法是对的?请大家想,如果我家的水是零点五升,告诉我水是溶剂, 水还是溶液,我相信大家肯定都知道这水呀,它是溶剂。那么我们一定听说过一句话,叫做一升水加一升酒精,它不等于两升,原因是我们的分子间是有缝隙的,那么我们的体积是不能叠加的,对不对? 我这加的是零点五升的水,我真的把氢氧化钠融进来,这溶液还是零点五升吗? 不一定了,他可能比零点五升就多了那么一丢丢,那你还能用这个数去算吗?来,我们回过头来看,这, 他说了是单位体积的溶液,也就是一升,必须得是溶液的体积才可以,你不能是溶剂的体积。所以这第一句话我认为他就错了,因为我的水是溶剂,他零点五升 一点用都没有。你再看底下那句话,他是溶于水,得到零点五升溶液。来,我问你一下,现代零点五升修饰的谁 是不是溶液?那我问你啊,你现在加了多少水?你知不知道?老师,这这,这能算吧?来,告诉你,不能算,你现在根本不知道这零点五升溶液里他的这个溶剂水你加了多少, 怎么配的?之后的课程我们会讲如何用一些方法达到第二句话的这种配配置方式,但是我们现在能做的只是我知道了 二十克是零点五模,但是我得保证溶液是零点五升,我才可以进行这样的一个浓度的一个计算,所以第二句话我认为没错。在进行做题的 的时候,请大家一定要关注他给你的是溶剂的体积还是溶液的体积,这件事至关重要。 ok, 来,那关于这个问题我们就不再多说了,接着往下来 我们做个对比,稍微做一个对比。我们今天学的物质的量浓度和以前学的溶质质量分数之间有什么关系?我不管这个单位换算是什么样子,单位换算一定会有题目考,这个大家自己用公式推就能推导出来。但我只看这个比 比的方法,质量分数是用溶质的质量比上溶液的质量,没错吧?再称一个百分之百,那百分之百我就不写了,你再看物质的量浓度,他用溶质的物质的量比上溶液的体积,你发现问题没有,我改变 的只是他们的物理量,但还是溶质比溶液这件事是一点都没有变化的。所以请大家千万认清楚一件事,我认为甭管用什么都是溶质比溶液跟溶剂没什么关系,这是其一, 其二很重要的一点。呃,我之前就说过了,质量这东西直观不直观不直观。所以啊,溶质的质量不够直观,但换成物质的量,一个两个我数着方便。 ok, 来,再看溶液, 溶液作为液体,您了告诉我,液体是用天平好撑,咱还是用两桶好取啊?我们一定是用两桶取出来是不是更方便一些?那所以这个地方我们把质量换成体积 用量,统一量取这个溶液的多少。比如说我知道他是一摩尔美声,我取一声,那里边是不是就有一摩尔的溶质?我知道这一摩尔溶质,我就知道应该有几摩尔的物质跟他发生反应了, 这个比例简单明了,所以非常的好用,这件事还需还需要大家能够比较准确的记住。 来,那接着往下第二件事,刚才讲了和物质的量浓度计算的一些基本内容,下面我们来说一下物质的量浓度里边有哪些值得我们注意的点。 第一个,物质的量浓度概念,你啊,这个溶质,哎,他指的是溶液中的溶质,但是你要注意,虽然叫溶质,他并不一定必须得是一个物质,他可以是什么呀? 可以只带单质化合物,哎,这都是废话。来,但是他也可以只带离子,也就是我这个地方可以说氯化钠的物质的量浓度是多少,我也可以说这个溶液中氯离子或钠离子的物质的量浓度是多少。比如说看这, 我给您一个一模每升的氯化钠。来,你告诉我一个氯化钠会电离出什么来?是不是电离出一个钠离子,一个氯离子来,那所以钠离子的浓度,哎, 一个氯化钠中一个钠,那所以氯化钠的浓度应该和钠离子浓度是一样的,一模每升。同理啊,氯离子他也应该就是一模每升了,完全没有问题。来,那接着往下呢?一模每升 的氯化镁溶液中,他问你氯离子浓度来,注意到没有?一个氯化镁里边两个氯, 那所以绿的个数是氯化镁的二倍啊。所以一膜每升的氯化镁溶液里边,我认为这个地方氯离子的浓度就应该是两膜每升,也就是他的两倍。 所以大家在进行一个离子浓度判断的时候,请注意一个点,他这里边有几个离子,他的浓度就应该是这个溶质本身的几倍。比如我给您写个硫酸一模为生, 那您说这里边氢离子浓度是多少?一个硫酸电力出两个氢离子,那所以呢,氢离子浓度自然而然两模每升就没什么太大问题了。来,那说到这, 关于我们说物质的量浓度这个问题,基本注意第一件事就算是搞定了。第二件事来,这是我刚才强调过的哟, 体积是谁的体积?体积一定是溶液的体积,而不是溶质的体积啊,而不是溶剂的体积,所以一定要注意加几升水。哎,没用, 水是溶剂,我要的是配益成一升的溶液,这才是溶液的体积,一定要跟溶剂的体积做好一个区分。那说到这,第二件事,我们也就说完了, 再看第三件事来,第三件事其实说到了一个什么问题啊?叫做溶液均分,当然这个均分并不一定指的是平均分配,就比如说喝过可乐没有?我这有一桶两升的可乐。来,我, 我现在把它倒出来一杯,我也甭管一杯是多少了,你告诉我,这一桶可乐的甜度和你这一杯可乐你喝上去的口感一样,不一样,是不是应该是一样的? 所以啊,我甭管从溶液中取多少,怎么取,只要你的溶液是从原溶液变过来的, ok, 他们浓度相不相同, 应该是完全一样的。所以从这个角度来说,我甭管取出多大的体积,我的物质的量,浓度应该不会发生变化。那就意味着什么呢?比如说,从这来看, 我这有一升一模美升的绿化美容液,但是呢,我从中如果取出了十毫升,我只取十毫升,然后你发 发现我的氯离子浓度仍旧是两膜每升,也就是我并不在乎我这个地方是不是一生中只取了百分之一出来。没事,我只要还是这个氯化酶,氯化镁就是一膜每升, 一个氯化镁中有两个氯离子,那所以氯离子浓度就应该是二倍两碗每升,那所以这个东西均分或者叫取出,对于他的影响,请大家一定要辨认清楚。那接着往下来第四个需要注意的点, 在用浓溶液配置稀溶液的时候啊,这个计算关系,我们一定要知道怎么叫稀释。这有一杯浓的溶液,我向里边加水,他就变稀了。来,你告诉我,加水过程中,我的体积变大了,我这里边的 水变多了,但是溶质的物质的量,溶质的质量,这都是不会发生变化的。所以啊,基本的公式在制,就是浓溶液、稀溶液,它的溶质物质的量完全相同。然后因为我知道 n, 如果是固定了来, c 等于 n 比 v, 那 n 就等于 c 乘 v 嘛,所以浓溶液浓度乘以浓溶液体积,哎,一乘 浓溶液溶质物质的量,稀溶液浓度,稀溶液体积一称,哎稀溶液的物质的量。所以这公式往这一摆,你就直接就可以进行稀释了。哎,怎么稀释?底下有题, 但底下这句话您记住了,来,体积虽然变了,但溶质的物质的量没有发生变化,这也 就是这个公式进行计算的一个基本的套路。那这个说完,我们直接拿一道题给大家看就得了。公式我摆在这看着,我们先看第一问, 第一问往这一放,熟不熟?熟的不行。初中问题来,一百克百分之二十的氯化钠,我稀释成百分之十。哎呦,我这质量分数还减半了, 那怎么办?我质量分数减半了,我这质量是不是应该就加倍啊?所以来,你看稀释后的质量, 两百克对吧?一百克乘以百分之二十,二十克溶脂,二百克百分之十乘起来。还是我们说的这样,一个二十克溶脂,所以没变化,没问题。 ok, 来,那你需要加水多少克啊?呃,两百克减一 百克,哎,我加水一百克没问题啊。哎,老师,你这这这问的问题没水平,我这初中就会。 ok, 别着急,咱往下看, 我现在把一百毫升一模每升的氯化钠我稀释成零点五模每升,你告诉我稀释后的体积怎么办?来,带呗。稀释前的浓度一模每升,这个体积是一百毫升,主要我单位全都不换算,无所谓的。稀释后的浓度零点五, 这个不知道,那您算一下呗。是不是来一除两百毫升来出来了,哎,跟刚才一样对吧?一百乘百分之二十等于 x 乘百分之十吧,你这个不也一样吗? ok, 这完全没有区别, 重点在这,咦,不两百毫升减,我这一百 百毫升不就一百毫升水吗?你这凭啥写?不知道啊,来,刚才说了一件事,一升的水加一升的酒精等不等于两升的溶液,好像我觉着不等于。 为什么体积这个东西他不能直接的相加,只能够我用,质量是可以相加,我再用密度去算,很麻烦。体积一加一不等于二。那你说了,我像一百克的溶液中 加一百毫升的水,你告诉我是不是两百毫升的溶液好像体积会变吧,所以出于这样的考虑, 加多少水你直接告诉我不知道。体积是不能直接相加的。没问题,来,这件事是一个比较核心,不是很难,但是大家可能在别的地方会遇到 到的问题来,但是注意,如果做类似问题的时候,题目给你来一句,忽略溶液体积的变化,那想都不用想。这句话的意思不是说一升加一升等于一升,不是,这意思,是一升加一升,他就等于两升,这叫忽略体积的微小变化。 一定要注意审题没有这句话,不要把体积相加,有了这句话,体积随便加。那 ok, 说到这关于注意事项,我们要说的就是这些。那接下来的时间我们稍微来做几道练习题。 第一道题啊,他说了,下列溶液中溶质的浓度是一模每升的,是哪个呀?来,我们来看呗。四十克的氢氧化钠,呃,一模来没有问题, 溶解在一生水,水是溶剂对吧? ok, 水是溶剂。那不好意思,你这就不叫一窝没生了,不行, 将一升十模每升的盐酸加入九升的水中,哎,你看,一升变十升,体积变十倍,浓度变十分之一,哎,一模每升吧。问个问题, 一升加九升等于十升吗?刚说完,不等于体积不能直接相加。第三个啊,二十二点四升,哎,老师之前课你提到过二十二点四升不是一模二吗?一,哎,溶于水配成一升溶液,溶液是一升一模,除一升一模每升没错。 问个问题啊,二十二点四升是一模的话,呃,什么条件?你这好像啥 啥都没说吧?应该,我们认为是应该认为的,是在一个标准状况下才可以,但现在 啥都没有。所以来 c, 我认为不对,你得注明标框,你才能证明他是一个我们说的一生的溶液。 ok, 来,那最后一个十克零点二五摩尔的 氢氧化钠没问题吧?来,零点二五摩尔的氢氧化钠溶解在水中,少量水没有问题,然后再加水,直到溶液体积为二百五十毫升,也就是零点二五膜。 呃,零点二五升啊,零点二五模,零点二五升,那一模每升问题不大,所以这道题的答案应该是四 d。 注意, a、 b、 c 错在了几个不同的点,第一个是 说的溶剂不对,第二个是体积相加了不对,第三个是没说标矿不对。所以这几件事大家一定要注意这个问题。来,接着往下第二个, 他说了关于零点一五膜每升的硫酸钠溶液中来,他的说法正确的是,他说一升溶液中有这些离子总数零点三 n a。 来想这件事。哈 纳离子两个,硫酸根一个,一个物质里三个离子,那么我认为离子的浓度是不是应该是他的三倍?离子是零点四五摩尔每升, 对吧?离子是三个嘛?对, ok, 离子浓度是这么多,那一生的溶液中就应该有零点四五摩尔的离子,那不就零点四五 n a 吗?你这零点三,不了,对了, 来第二个,一升溶液中含有钠离子数目零点一五 na 一升,那就是零点一五摩尔,零点一五摩尔,一个里边两个钠,那他就是零点三摩尔的钠。呃,零点三 a 不对, c 一升溶液中钠离子的浓度是零点四。哎,刚刚说了吗?没错,你钠离子是两个嘛,那所以是他的二倍,零点三摩每升, c 是对的。最后一个,四 d 两升溶液中含有浓度。呃,首先一点,我说过, 浓度这个东西跟体积大小没什么关系,你一升也好,两升也好,硫酸根,一个硫酸钠一个硫酸根,那浓度零点一五膜每升,你不能给我乘二,所以答案应该选择是 c。 那 ok, 到这为止,这道题就算是结束了。那说到这,我们对今天的课程进行一个小结,那物质的量浓度,我们计算的时候一定是溶液的体积,而不是溶剂的体积, 这点大家一定要注意。而我取出溶液啊,它的离子浓度没有任何的变化,你也许取出之后体积小了,但浓度完全是相同的,但稀释的时候体积变了,但不过我的溶质物质的量 没有发生任何的变化。那所以说到这,这一节课的内容,我们主要就是这些。
863爱学习的她 14:07查看AI文稿AI文稿
14:07查看AI文稿AI文稿我们这节课来介绍一下物质的量在化学方程式计算中的应用,我们先来看一下基础知识,基础知识呢,就是根据化学反应方程式当中啊计量数, 剂量数和什么有关系呢?剂量数是和物质的量相关联的,也就是粒子个数比 等于物质的量之比, 其实最关键的就是用这样一个信息啊,那具体呢,我们来看计量数是一一二,那么扩大恩贝呢,就是他的粒子个数,粒子个数呢,是和物质的量之间是成正比 的,也就是大恩正比于小恩。所以呢,我们把质量转化成物质的量,把体积转化成物质的量, 都是与记账书成正比的,所以我们在进行画一式方程的这个 化学方程式计算当中啊,计量数值比就等于他的例子,个数比等于他的物质量值比,那同温同压条件下也就等于他的体积比。 有了这样一个基本的关系,那我们就来看一下具体的例题。步骤上来看呢,就是 转化,不管题目当中给出你什么样的物理量,我们都把它先转化成物质的量, 然后其他的过程都和我们用质量在进行计算是一样的。我们具体来看例题啊,第一题先说个简单的,把它的格式了解一下, 五点四克的铝合足量的绿化氢生成氢气的标框下的体积,这个题并不难啊,上来我们先设氢气的物质资料未知, 再将已知转化,已知的是质量,把质量转化成物质的量零点二末,再根据化学反应方程式 列关系,然后这是比例式, 这都不难啊,大家只要 找出来这个,最后再把它转化成我们所需要球的物理量体积就可以。零点三魔球出来了。 呃,再乘以二十二点四。答案,这个题如果我们做填空题后选择题什么的就用不着,那就是两个铝生成三个氢气,直接列出来就可以啊。我们管这种叫关系式法,刚才那是写方程式,如果有了关系式,零点二末, 这零点三末, ok, 这就可以去求了。 v 请起等于零点三乘以二十二点四。好,我们来看第二题。 五百毫升的氢氧化钠溶液当中加进去十点八克的铝,二者恰好完全反应 球氢氧化钠物质的量浓度,球生成氢气的体积,非氢气 c 氢氧化钠一样的道理啊,我们列出方程式八五十四克, 五十四克。就是啊,我们把这十点八克呢转化这种形式去写,就是质量上下单位统一,大家看啊, 我要求的是什么?看,这是你的单位是统一的,这个单位呢也是统一的,他们俩的单位呢是统一的,只要上下单位统一,那么他们就都成正比。关系 单位统一列比例是,我一般情况下不推荐你用这个啊,虽然这个也可以。一般我情况下就是不 管什么样的物理量,我都转化成物质的量,这是比较省事的。呃,我说的这个省事是省的想是吧,我用不着在这里有多少的这个转化。 好,下面我们看具体一些常见的方法。第一种方法呢叫关系式法,就是把已知量和未知量之间 靠多个关系联系,联系起来的时候只要知道其实和,就是知道已知和未知之间的比例关系,我们就可以进行计算,这里呢,还经常用到一种的方法叫原子守恒,请看例题。三,把一定量的一氧化碳还原, 三氧化二铁得到二氧化碳,通入澄清石灰水当中,得到十克的沉淀,那这是沉淀,就是碳酸钙参加反应 氧化碳的质量。这里面啊,我们知道啊,根据他的反应过程要经历两个反应,第一步,第二步在这个反应的过程当中有原子守恒, 我们刚才讲这个原子,这里的原子是哪个原子守恒呢?就是碳原子,大家看碳原子,碳原子, 碳原子这三个地方,所以一氧化碳转化成二氧化碳,二氧化碳转化成碳酸钙,所以这里面的关系是就有了,既然有了这个食客,我们是不是就可以求出一氧化碳的质量啊? 啊,你说你用质量去做也可以,你说我的物质量也可以,这都没有关系的好,列出式子来,就可以求出他的质量。二点八克, 这是第一种方法,叫守恒法啊,这个观世法,第二种方法守恒法,守恒法有两种守恒,一种呢叫做元素守恒, 就是元素的种类,质量和原则各数之别。我们来看这道题,由氧化铜、氧化铁组成的混合物十克,加入五百毫升的某浓度盐酸中,混合物完全溶解,再加入二百五十毫升 两膜的炝化钠中,也得到的沉淀。最多该盐酸的物质的量浓度是多少?一看这反应挺多,是吧? 挺多,那怎么叫手王呢?我们分析他的过程,通常的方法呢,我们是把所有的防潮式写出来,在这里呢,我不写了,毕竟是个选择题啊,那我们来分,我给大家分 一下盐酸,他在这里了,是不是要先变成了绿化铜, 绿化铁,而在这里绿化铜,绿化铁,再加上氢氧化钠之后,最后变成的是不是都是氯化钠呀?所以在这里的关系就是我们有多少氢氧化钠就消耗了多少盐酸, 氢氧化钠的量就是盐酸的量,这就是守恒。为什么这个绿在这里守恒,你看钠和绿的关系是一比一, 剩下的氢氧化物,氢氧化铜,至于有多少氢氧化铜都要氢氧化铁,和这道题实际上是没有关系的,就是找到最终的根据。守恒就是绿化氢全都 变成了氯化钠,而氯化钠的钠是从氢氧化钠来的。氢氧化钠有多少?零点二五乘以二, 零点五膜,零点五膜,那么绿化氢的量就是零点五膜除以他的五百毫升,所以他的浓度就是一抹每升。 复杂的变化当中一定存在着守恒,越复杂越守恒。好,第二个我们来看转移电子的守恒,转移电子守恒呢?这是氧化还原当中的一种定量反应, 我给大家写一下他的过程啊,这个结合仰望还原定量计算可以分析,他说一模每升的亚硫酸钠三十毫升,恰好将二乘以十的负二次发完。膜 xo 四还原 氧化产物是硫酸根,则 x 在原还原产物的化合价。这个方法呢,我们把它分成半反应来分析, 就是氧化还原的办法。亚硫酸根他变成了硫酸根,在这个过程当中,他一个是失去了两个电子,由正四变成了正六,失去两个电子, 那用量多少?用到多少物质的量呢?一抹每升 乘以三十毫升,也就是零点零三升,这是氧化过程。 我们再来看还原过程, 在还原过程当中, xo 四负,这是正期价,变成了一个我们不知道价太的啊,我们未知价太的。在这里,他得到多少个电子呢?我们假定得到 x 个电子, 他用的物多少物质的量呢?用了二乘以 十二十的负二次发膜。那么在这两个过程当中, 失去的电子总数和得到的电子总数,这二者应当是相等的, 总数相等,这样我们就可以求出来 x 等于多少,求出来这俩相等啊, x 等于三,由正七加得到三个电子,所以他是几加正四加。这种题你明白了吗?把氧化和还原分成两个半反应,这失去两个电子是指 每个园子转移电子数, 电子报数后面是他的物质的量啊,有多少这种啊,他们相等。 第三种类型,差量法,什么叫差量法呀?所谓差量啊,就是 是在物理量发生了理论上的差量。我们具体来看一下提议啊,将一定质量的钠投入到二十二十四点六克的水中,最后得到三十一点二克的氢氧化钠溶液, 所得呛化钠溶液中溶值的质量是多少?这个是水啊,只告诉我们水钠有多少,不知道氢氧化钠溶液。那么我们马上先观察一下他的方程式,大家来看,方程式写出来在这里啊, 这个反应当中的方程式,两个纳进来,有进来的纳,有出去的清, 所以这之间差了四十四,那么这三十一点二和二十四点六之间的差值就是他们进来的纳和出去清的差值, 这就是差量法。有了这个质量,三十一点二,减去二十四点六,求出来这个差量。 由差量的比例就可以分别求出纳的质量和氢氧化钠的物质的量。因为这样我列什么上下单位统一就可以了。我要求氢氧化钠溶脂物质量上这是两模,下面就是他的物质的量,求纳呢,求他的质量,所以这呢就说他的质量就可以求了。 所谓差量,就是化学反应影响的物理量的变化。 第四种方法叫做手方程组法。这个 方程组法其关键就是解决混合物,把混合物的问题解决了。 土合物分别求各自有多少,你就说特别在合金问题当中啊,这合金铁和锌的合金搁到二百毫升某浓度的细硫酸当中,生成了氢气,六点七二升,你看他是两物质, 有俩物质啊,后来呢是俩反应,再后来呢,就是这个,就是两个总量啊,两物质,俩反应,两总量,两个总量,哪两个总量? 总质量,总体积量物质量,反应量。总量的题就可以用方程组法来解决。那写出化学反应方程式, 化学反应方式,铁和气流算,反心和气流算。反应分别设为 x 和 y, 射他为 x, 射他为外,这个生成的氢气就是 x, 这生成的氢气就是外。所以五十六 x 加上六十五万,五十六 x 加上六十五万,就等于十八点六 x 加外等于生成的气体,气体给出的是六点七二, 那就是六点七二,除以二十二点四,已列出来, sy 求出来完事。这种题。
719小王不不不讲化学🧙 10:55查看AI文稿AI文稿
10:55查看AI文稿AI文稿今天给大家整一波福利啊,讲一讲这种混合物质类型,去算物质的量啊,就算 n a 的这种问题, 很多高一的学生看到混合物就害怕是吧,有些高三学生说,我也害怕,我们现在来讲一讲这种问题,我先给大家讲一讲,其实混合物这类型,你只要抓到一种基本方法叫急执法, 其实大多数的这种混合问题你都能想明白,都能做对。什么叫及止法,我家给大家举些例子,然后这里面还有些技巧方法,我就顺便给你一块一讲啊。第一个标抗性二十二点四升,是不是相当于是一模二的一氧化碳二氧化碳混合气体?问你碳原子数为 gna, 那我们这里啊,用其指法就是假设他只有一模二一氧化碳,是不一模二碳,假设只有一模二二氧化碳是不也是一模二碳?那他们俩一氧化碳二氧化碳混合气体是不总共一模二,所以他的碳源之处是不也就是一模二, 也就是 ena? 这个正确。那这个题呢,其实我用的常见的方法就是比较快一点啊,就是极致发也行吧,我可以把它这样设设为它的通式一氧化碳和二氧化碳,它的通式其实是碳氧 x 啊,因为你问我碳原子数 x 氧是不是是一到二之间的,那你一模二碳氧 x, 碳原子数肯定是一模二呀, e n a 啊,自己去悟一下啊。第二个一模二甲烷和一模二乙烯, 这个高一的学生可能还不认识啊,但是你见他给你化学事就可以了,也是混合气体氢原子数,你看用几指法,一模二甲完似模二氢,一模二以稀,是不是也是似模二氢?他的氢原子数就是 c n a, 对吧?啊,那肯定是对的, 那用是吧?我刚才讲的也可以变形啊,你可以把它设为通式是不?碳 x 清四,它们俩无论怎么混合清都是四,是不是就相当于它是一目二?问的是清原子数碳又没什么关系。 完事了啊。第三个呢,标准状况下,二十二点四升的氮气和氢气混合,这也是一模二,对不对?氮气和氢气混合有些说老师,这俩是不是要反应啊?啊,要生产氨气啊,那个生产氨气的是高温高压催化剂啊,所以他俩一般常温长压下,这个标矿是零摄氏度一百零一千帕,不反应 混合气体,问的是多少个原子?那一模二你可以把它设为通视,都是双原子分子对不对?那原子数肯定是二,二模二的 x 原子,那就是二 na 吗? 你用鸡翅法试一下是不是啊?第四个呢?同同鸭下,质量相同的氧气和臭氧含有的氧原子数相同。 这个如果我们用这这个不是混合物啊,但是他跟这种思路是一样的,质量相同,你就分别去算就行了啊。这个单数有点慢啊,我给你算一下,比如说小 m 都一样,然后氧气呢,是不是太大 m 是十六乘二对不对?但是要算的是氧原子的数,是不是一个氧气还有两个氧原子是要乘个二的,所以最后算出来是十六分之 m。 那对于臭氧来说呢,也是一样的呀, 质量小 m, 然后臭氧一个氧是十六,他有三个氧,这是臭氧的大 m, 然后他的氧原则数数乘以三,是不还是十六分成 m, 所以他俩肯定是相同的。 但这个题这么做呢啊,就是稍微慢一点啊,但是你要是正常能想的明白,无论是氧气还是臭氧,看我写的这里,他们这里面其实都是由氧原子构成的嘛, 你们的总质量是一样的,这总质量不都是养原子的质量?那你小 m 比大 m, 这个比的是不都是养原子的石榴?你求的也是养原子的石榴,明白吗?啊,这个玩玩意相等肯定是对的好吧,好看。第第五个十 斯克,乙烯是碳二氢四,丙烯是碳三氢六,它的混合气体当中的氢原子是为二 a, 这个对不对呢?这个有些人就不太会这种了。那你用极脂法也可以去做的啊。这个极脂法我说到这吧, 十四克乙烯呢,就是十四,比上乙烯,他就是两个碳氢二啊,这个相当于是两个碳氢二,这个呢,是不是相当于是三个碳氢二 碳氢二啊,对吧?好,那你乙烯两个碳氢二,一个碳氢二是十四,两个碳氢二就是乘个二,他要求的是氢原子数,那乙烯是有四个氢的,这样比下来是不是就像那等于二了? 同理啊,丙烯也是一样的十四,丙烯是有三个碳纤二的,它总共有六个千元子嘛,对不对?这约下来是不是还是等于二?所以即执法就搞定, ok, 机制法就搞定了。但这个题有一个技巧啊,这个高三学生一般可能会熟一点,就是什么最简式,还是我跟刚那个臭氧气思路是一样的,你看,比如说这个框框里面,你是乙系也好,丙系也好,你们总共只有十四克,你们其实都是无数个探亲二构成的。 而且你问的是氢原子数吗?我最后十四克碳氢二,其实除以十四克每亩二,这个就是碳氢二的物质的量啊,算出来 m 二是量,算出来就是一亩二碳氢二嘛, 对不对?那氢原子的物质的量可能就是二 n a 了,就搞定了。好吧,这就是常见的方法啊。来,第六个 一模儿丙烯、乙烯和丙烯的混合气体氢原子数为多少?你看我给大家讲保这个保底的方法就是挤脂法。很多人其实用技巧是想的比较死板的,那你要用刚才这个啊,丙烯和乙 乙烯的碳氢二,老师他是一模二,那他的清源子数是不是二人也对了,这个是不对的,用这件事就不对了。为什么?因为刚才是十四课,是你算出来是一模二碳氢二的。你现在乙烯 是不是他相当有两个碳氢二,丙烯是有三个碳氢二的,那你一摩尔乙烯和丙烯,他的碳氢二的数目是多少?用极致法思考一下,一摩乙烯是不是有两摩尔碳氢二,一摩丙烯是不是有三摩尔碳氢二,他的碳氢二是二到三摩尔之间的, 所以他的清源子数你是不知道的,知道吗?那你要算,比如说老师这个题,我该怎么去算清源子数呢?你就用及指法,一摩尔以西呢,是一摩尔,探二清四,对不对?来,你自己去想啊。 如果假设只有一亩二乙烯,是不是一亩二贪二氢四,那就是四亩二氢原子。如果假设有一亩二丙烯,是不是有六亩二的氢原子,那他最后的氢原子数肯定是四到 到六之间的,所以这个 rna 就压根都不对,所以我说这个技巧呢,一定要理解啊,我们保底用机制法。好吧,来第七个,常温常压下四十六克。很多人看到老师常温常压这个气体啊,错了, 因为不知道他 vm 等于多少,这给的是质量,有些人就特别嗨,是吧,总有人犯这样的错误。这个四十六克相当于是不是小 m 呦,这混合器械含有的原子数为三 a, 这怎么做啊? 也一样的嘛,你看啊,用极止法是吧,我写在这里四十六克的,如果是四十六克的谁二氧化氮?他刚好就是一母二,他问的是原子数是不刚好对应的一母二氧化氮是不是有三母二原子, 对不对?那如果是四十六克的二四氧化二蛋呢?它是零点五摩尔, 他的原子数是不是零点五乘个六,是不还是三三摩二?所以你看两个极端都是三摩二的原子,最后原子数肯定是三 a 是正确的啊,这个基指法。但这个题呢,跟第七第五个是很像的啊,因为他们都知道这个框框里面看又来, 因为四氧化氮相对是两个二氧化氮,但你总质量是四十六克呀,你看你们这里面是不是相当于无数个二氧化氮的质量是四十六克?你反正问的是原则数吗?对不对?那我四十六克,那我是不是就能算出来这个二氧化氮的物质量?四十六克,二氧化氮是四十六克每亩二,我算出来是不是一亩二, 那它的原子数是不是就是三摩尔原子啊?三 a 就直接搞定了啊,这个就是快一点,但你前提要理解啊,所以一定要算出混合气体最碱式的物质的量,算出最碱式物质的量,你再去算这些问题,就比较简单一点好吗?来,第八个呢,第八个你看 这个还是一种另一种类型的,你用极值法标框下也无所谓了,二十八克二一氧化碳的大 m 是二十八克每亩二,氮气的大 m 也是二十八克每亩二,你用极值法你发现算,他问的是体积。嘿, 第八个我写的这里啊 n 等于 vbvm, 那标框下是不二十二点四升每模二是知道的,那这个体积是不就去算物质的量就可以了,对不对?那你二十八克每模二都是二十八克每模二是不算出来都是一模二。如果集值法的话都是一模二吗?那一模二体积在标框下肯定是二十二点四升。那肯定是对的啊,集值法。 但这个题呢,也可以用混合物直接来吧,因为你们俩你是二十八,我是二十八,那你这个 n 总等于什么呢?是不等于小 m 总比像大 m 平均是不是就是混合气体的平均模式质量?那就是二十八克,你俩都是二十八,那平均 下来也是二十八克面膜,所以是吧,你们俩其实就是一模二的混合气体。那一模二混合气体一样的嘛。 v 直接带到这个公式里面去算就行了, 这个是不是叫一一对应啊?公式你带的这个是 n 总的,你算的这也是 v 总,二十二点四升没问题啊。好,第九个呢?第九个呢?这里面也有点麻烦的,就是要算工人电子队的事啊,这个是高一,目前确实解决不了啊。一样的,我们来看第九个, 常常按下乙烯和丁烯,他们的混合气体共用电子兑数为九 n a, 对不对呢?这个你用及时法还是一样的啊,你比如说只有四十二克的乙烯, 碳二千四,只有四十二克的丁硒碳四千八,你要去算他们的公益电子费怎么做呀?你先把乙烯的电子式画出来, 几个共赢电子队啊,一对,两对,三对,四对,五对六对,是不?他是有六对的,那你想四十二克的乙烯是几摩二呢?那,那你就来除吗?四十二小 m 除以他是碳二千四是十四乘个二啊,这算下来等于二分之三, 这是乙烯的物质的量,再乘以他的六,这算出来等于九九摩尔,所以他是有九摩尔。公用电子队就九 na, 我算到一个极端了吗?再算另一个极极端啊, 丙烯啊,其实更容电坠,也是我们常说的这种供价件数目啊,一样的。好吧,那你那这个丙烯呢?那我直接给你画了,我就不画这更容电坠,蹲起来比较麻烦。就这样, 每个探程四个键, 你自己去数一下它有多少个键,多少个键就 多少。公用电子队,一二三四五六七八九十十一,十二十二对,那就十二对公用电子队。好,然后四十二可以吸呢,你四十二丁吸啊,那是不是它是有四个碳氢,二十四乘以四 四分之三,四分之三亩二再乘以十二,这是他的是吧?一个丁西啊,就相当于有多少个十二个垫子吧。十二个垫子一除,是不还是九亩二?所以用机制法就搞定。 ok? 这个题制法呢,就一般比较通用。但这个题有些老师也总结了。老师你看这个乙烯和丁烯,他们最简示也是碳纤二, 我可以总结出来啊,其实一个碳氢二平均是含有三对公用电子队,那你这样一算,四十二克的碳氢二是不是相当于只有三摩二三摩二,三三得九九个 a 直接就出来了啊?但这个结论我觉得其实有点没必要了啊。有极致法一般就够,你做一下就行了好吧。
804你们的化学胡老师(Hg) 20:31查看AI文稿AI文稿
20:31查看AI文稿AI文稿同学们大家好,这节课我们一起来学习物质的量。第一课时, 我们生活在物质生活非常富足的时代,我们身边琳琅满目的物品大多都是以什么方式计量的呢?有什么规律? 大家不难发现,大件物品一般按单个计量,比如一台电视、 一张桌子,一部手机。比较小的物品通常按集团计量,比如一千克大米, 我们几乎从不一粒一粒的数,比如一盒图钉,一盒签字笔,这些比较小的物品按集团计量可能更加方便。 那么你有没有想过我们最熟悉的水又是如何计量的呢? 水是大家很熟悉也很重要的物质,由水分子组成,那么水如何计量? 有同学说一吨水,一千克水,有同学说一升水,一毫升水。 那么无论按质量还是按体积,这些水中又分别含有多少个水分子呢? 我们看一吨水约含有三点三四乘以十的二十八次方格水分子,一千克和一升水中均约含有三点三四乘以十的二十五次方格水分子。 一毫升水约含有三点三四乘以十的二十二次方个水分子。 如此庞大的数字,我们用起来很不方便,所以对于这些比较小的粒子,通常以集团计量,建立堆量,从而化繁为简。 一九七一年在第十四届国际计量大会上正式宣布了 物质的量是国际单位制中的一个基本物理量,其单位为摩尔。物质的量就是我们对这些特别小的粒子建立的堆量。国际单位制有七个基本物理量, 分别是长度、质量、时间、电流强度、热力学、温度、物质的量、发光强度。 我们这节课就来学习其中一个物理量。物质的量及其单位摩尔 物质的量表示含有一定数目粒子的集合体,符号为小写 n, 单位摩尔,简称摩。我们用摩尔来计量一定数目的例子。 我们熟悉的计量方式及数目为,一盒签字笔十二支,一包白纸五百张,一盒区别针一百个。那么一模粒子有多少个呢? 国际上规定,一模粒子结合体所含的粒子数约为六点零二乘以十的二十三次方。 一模任何粒子的粒子树叫做阿弗加德罗长树,符号为 n a, 通常用六 六点零二乘以十的二十三次方美模表示。我们一起来回顾历史。阿弗加德罗,意大利物理学家、化学家,一七七六年生于意大利都灵市。 阿弗加德罗毕生致力于化学和物理学中关于原子论的研究。 他的研究对科学的发展,对微观世界的探索起了重大的推动作用。为了纪念他,后人以他的姓氏命名阿弗加德罗常述。 阿弗加德罗常树,他究竟有多大呢? 让我们一起来感受 受。阿弗加德罗常述, 截止到二零二零年三月,全球人口将近七十六亿。 如果把六点零二乘十的二十三次方粒米给全球七十六亿人吃,每人每天吃一斤,大约可以吃多少年呢? 称粮六十粒某大米约为一克,计算六点零二乘十的二十三次方,除以六十乘五、百乘七十六乘十的八次方乘三百六十五的积,约等于七百多万年。 六点零二乘十的二十三次方粒米给全 全球七十六亿人吃,大约可以吃七百多万年, 你能想象六点零二乘以十的二十三次方格硬币排列在一起有多长吗? 如果把六点零二乘十的二十三次方个一角硬币直径约一点九厘米,排成一行,可以绕地球赤道多少圈呢?赤道周长四万零七十六公里。 让我来给大家算一算吧!一点九乘十的负五次方乘六点零二乘十的 二十三次方除以四万零七十六,约等于两百八十五万亿。 六点零二乘十的二十三次方个一角硬币排成一行,可以绕地球赤道大约两百八十五万一圈。 我们看到,如果描述宏观物质阿弗加德罗常数大到超乎想象, 所以作为物质的量的单位。摩尔通常用于计量原子分子、离子、原子团、电子、 质子、中子等微观粒子,如一摩尔铁原子、一摩尔氧分子、一摩尔钠离子、一摩尔硫酸根离子等。 下面我们一起来完成以下练习,一、一、膜水中约含有六点零二乘以十的二十三次方个水分子。二、零点五膜二氢氧化钠中约含有 三点零一乘以十的二十三次方个纳离子。三、六点零二乘以十的二十三次方个氢气分子相当于异摩尔氢气。 四、一点二零四乘以十的二十四次方个硝酸根离子相当于两摩尔硝酸根。那么你能发现物质的量与粒子个数之间的转化规律是什么吗? 物质的量与粒子个数之间的关系是,物质的量乘以阿弗加德罗常数 g、 n、 a, 可得到粒子数。 反之,粒子数除以阿弗加德罗长数,则可得到物质的量 公式,物质的量等于粒子数,除以阿弗伽德罗长数。 我们知道一个水分子中有两个氢原子,一个氧原子。扩大六点零二乘以十的二十三次方倍。可以看成, 一乘以六点零二乘以十的二十三次方个水分子中有二乘以六点零二乘以十的二十三次方个氢原子。一乘以六点零二乘以十的二十三次方个氧原子, 即一摩尔水分子中有两摩尔氢原子、一摩尔氧原子。 我们看到了什么规律呢?对粒子数之笔等于物质的量之笔。一抹水代表哪些 含义呢?我们一起来分享,看看同学们怎么说。水分子的物质的量为一摩尔,一摩尔水所含的分子数约为六点零二,乘以十的二十三次方个。 一抹水中所含的氢原子数约为一点二零四,乘以十的二十四次方格。一抹水中所含的氧原子数约为六点零二乘以十的二十三次方格。 一摩尔水中含有两摩尔氢原子,一摩尔氧原子。我们来梳理一下,关于一摩尔水, 我们究竟能知道什么?一摩尔水水分子的物质的量为一摩尔,一摩尔水所含的分子数约为六点零二,乘以十的二十三次方格。 一抹水中所含的氢原子数约为一点二零四,乘以十的二十四次方格。所含的氧原子数约为六点零二,乘以十的二十三次方格。 同时得到一个水分子中有两个氢原子,一个氧原子。 一膜水分子中含有两膜氢原子、一膜氧原子。两膜氢原子和一膜氧原子又 组成了一抹水,那么一抹水的质量是多少呢?质量才是我们可测的数据。方法一,如果利用一个水分子的质量乘以水分子的个数,可以算出质量。 方法二,可以总结规律。方法三,可以通过数学推导。这节课我们主要来讨论物质的量与质量之间有哪些规律。 在教材第五十一页,图二杠二一图片中展示了物质的量为异摩尔的几种物质,并标注了 他们的质量。你能发现有哪些规律吗? 我们将图中数据以图表的形式展示,写出他们的相对原子或分子质量,铁五十六, 铜六十四,铝二十七,锌六十五,硫三十二,氯化钠五十八点五,水十八,蔗糖三百四十二。 同学们,我们一起来看其中每一种物质。一、摩尔的质量,其数值与它的相对原子或分子质量相同。 我们把单位物质的量的物质所具有的质量定义为摩尔质量, 符号为大写 m。 常用单位克美模表达是摩尔质量等于质量比物质的量。 注意,摩尔质量数值上等于相对原子或分子质量,但意义不同。摩尔质量有单位克美摩,相对原子或分子质量是个笔直,没有单位。 我们来看,通过已知物质的相对原子或分子质量,我们可以直接得到 他们的摩尔质量的数值。再加上单位克每膜,比如水的摩尔质量为十八克每膜硫酸的摩尔质量为九十八克每膜氢氧化钠的摩尔质量为四十克每膜。 有了摩尔质量,我们就可以将物质的量与质量关联起来, 物质的量乘以他的摩尔质量即为质量。反之,质量除以摩尔质量得到物质的量 公式,物质的量等于质量比摩尔质量。 刚才我们 已经讨论了一抹水的物质的量与粒子数之间的关系,我们继续来完善物质的量与质量之间的关系。一抹水根据公式,质量等于物质的量乘以摩尔质量, 水的摩尔质量为十八克,每摩算出一摩尔水的质量为十八克。 化学是一门充满神奇色彩的科学,它通过物质组成、粒子分析,引导我们探索那些肉眼看不见的粒子的特征和行为, 引导着人们认识整个物质世界。我们看到物质的量 将微观的粒子数和宏观的质量连立起来,起到了重要的桥梁作用,帮助我们更加清晰地认识微观世界。 建购了这样一张关系网,粒子间的转化关系一目了然。 如果我们从微观粒子出发,已知粒子数有六点零二乘以十的二十三次方个水分子, 利用粒子数与物质的量之间的关系,粒子数除以阿弗加德罗长数等于水分子的物质的量,即一抹水 借助于物质的量的桥梁作用,利用质量等于物质的量乘以摩尔质量求出十八克水,同时也可以分析水的粒子组成。 如果我们从宏观物质的质量出发,已知水的质量十八克,利用物质的量等于质量除以摩尔质量算出一摩尔水, 则同样可求一抹水中约有六点零二乘以十的二十三次方个水分子。 e 摩尔水中有两摩尔氢原子和一摩尔氧原子,约 含有一点二零四乘以十的二十四次方格氢原子,六点零二乘以十的二十三次方格氧原子。 由此可见,无论我们从微观粒子或是宏观物质出发,借助物质的量是核心。 这个问题我们来讨论。从多水平定量认识物质,分析物质与易摩尔水含有相同氧原子数的氧气的质量是多少呢? 一抹水中含有一抹氧原子,一抹氧原子约为六点零二,乘以十的二十三次方个氧原子,相当于零 零点五摩尔氧气分子乘以摩尔质量三十二克,每摩则与一摩尔水含有相同氧元子数的氧气的质量为十六克。 学习了物质的量这个物理量,我们可以轻松地将物质的质量和粒子数连立起来。比如,我们拿到一份铝, 我们可以称量它的质量,利用质量除以摩尔质量计算出物质的量 乘以阿弗加德罗长数算出铝原子的粒子数。物质的量是联系宏观和微观的重要桥梁。 我们小结一下本节课所学的知识。物质的量为描述微观粒子的一个基本物理量 乘以阿福加德罗长数得到粒子数乘以摩尔质量得到物质的质量。反过来,粒子数除以阿福加德罗长数,质量除以摩尔质量得到物质的量。 物质的量承载着微观粒子与宏观物质之间的桥梁作用,有助于我们更全面、更深刻地认识整个物质世界,将物质之间的定性分析与定量数据 完美融合,为我们打开了一个探索物质世界的新窗口。 课后思考,在科学研究或实际生产中,涉及气态物质时,测量体积往往比称量质量更方便, 那么气体体积与物质的量之间又有什么关系呢?我们下节课继续学习,同学们再见!
159在线学习高中部 02:45查看AI文稿AI文稿
02:45查看AI文稿AI文稿第一个,马尔质量等于质量,服务员负责量,从这能推出来两个都是。第一个,质量等于 物质的量乘以什么摩尔质量。第二个,物质的量等于质量,属于摩尔质量。第二个,摩尔质量等于什么?一个威尼单威尼的质量乘以哈佛加多多常数,因为 单位的质量乘以阿富加罗常数,就是阿富加罗常数的威力的什么质量?第二个,毛的质量等于二十二点四六, 这个要求必须是比较好,这个肉你们肯定应该认识啊。第二个,这是通过质量跟物质上之间转化的一些公式,对不对?那下来我们再看,什么 n 等于 c 除以 二十二点四啊,这个上面一定要备注是什么气体的体积啊,气体体积除以二十二点四 等于五十的量,然后呢?这个第二要求他必须是什么?要靠,也就是说在这里面我们把他的衍生公式就是 a 等于二十二点四, a, 明白了吗?嗯,然后在这还需要个几个叫么?而体积等于 rt 比上个 p 二十等于八点三十四啊,这个 t 和 t 这个公式是告诉你膜体积等于这个数,也就是说灯 t 等于二百七十三, k 压下到一百零一千八的时候,这 vip 等于多少?是二十二点四,这是我们要知道的,但是 你 viv 等于二十二点四的,他不一定是标准货,放放,明白了吗?还有 c 等于 s, b 对不对? 溶制的物质的量处于溶液的体积等于溶质的物质的量浓度,明白了吗?那么也就是说在这里面还能衍生出来 a 就等于 c, 乘以什么 v, v 就等于 a, b, c, p v 等于 a r t, p, v 等于 m p, m r, t p 大 m 等于六二七不,质量等于所谓的一数除以 什么阿福加德罗长处,然后在这里边是不是能推出来自己一处,等于什么物质量乘以阿福加德罗长处?这都为什么我们说一模二十一人,两个人是两人一个吧?三个二十三人一个吧,对不对?
2407松哥化学 07:00查看AI文稿AI文稿
07:00查看AI文稿AI文稿的化学微课堂,这几课我们学习物质的量及其单位。摩尔,请同学们先明确本节课的学习目标。 水是生命之源,人体一切的生命活动都离不开水。 你知道我们喝到的一杯水中有多少个水分子吗?按照一杯水五百毫升计,大约有一点六七乘十的二十五次方个水分子。 这个数字也许惊到了你,这么庞大数字,如果用个来衡量他的多少,是不是不方便呢?再比如,你去买 大米,你肯定不会说老板给我买一百万粒大米,大米颗粒又小又多,于是袋这个新的衡量大米多少的单位就有了, 但是有不同规格的数量的集合,我们可以根据需要购买一定袋数的大米,就很方便了。 同样构成水的分子数目庞大,我们只要确定类似于带的一定个数的集合,然后用这个集合多少去衡量微观粒子多少,是不是就很便捷呢? 所以,为了描述宏观可称量物质所含微观例子多少,人们引入了物质的量这一物理量 来请同学们看一看。国际单位制的七个基本单位,长度、质量、时间、电流。这四个物理量对我们并不陌生,单位也很熟悉, 你找到物质的量及其单位吗?摩尔,原来摩尔是拉丁文大量堆积的意思,用这个为单位很贴切哦。 我们整理一下思路。物质的量是一个物理量,是用来描述物质所含微观粒子多少的物理量。 他表示含有一定树木粒子的集合体,因为摩尔是他的单位。我们也可以通俗的说, 物质的量表示物质含有多少摩尔粒子的物理量规范表达为 x 摩尔某粒子, 也就是说摩尔只能描述原子、分子、离子、原子团以及质子、电子、中子等例子,后面不能是宏观物体。一模二大米,一模二桌子都是错误的。 那么问题来了,摩尔既然和我们刚说的代以及生活中的答等都是一定数母粒子的集合。 答,这个特殊单位量大家都知道,一答为十二个,那么多少数目粒子集合 规定为一模二呢?国际上规定一模二粒子集合所含粒子数与零点零一二千克碳十二所含碳原子数相同,约为六点零二乘十的二十三次方。 为了纪念,意大利物理学家阿福加德罗把易摩尔任何粒子的粒子数叫做阿福加德罗,场数符号为 na。 通常用六点零二乘十的二十三次方各美膜或者摩尔的负一次方表示, 这个数字大的令人发指。如果把六点零二乘十的二十三次方立大米给全球七十一 一人吃,每人每天吃一斤要吃十二万年。 我们可以这样理解摩尔的概念,摩尔和霜达一样都是特殊单位量。所不同的是,摩尔后面必须跟的是微观粒子 e 摩尔,任何例子含有 na 个对应例子,那么 n 摩尔例子就含有 n 乘以 na 个例子。 总结公式如下,大 n 为例子,个数等于小 n 乘以 n a, 那么小 n 就等于大 n 除以 na。 同学们掌握了吗?我们通过练习来巩固一下, 有四个判断证物题,请点击暂停键完成 第一题。易摩尔,任何物质都含有六点零二乘十的二十三次方个分子错误,比如氯化钠中就没有分子,氯化钠是由氯离子和钠离子构成的。 第二题,三摩尔氧气分子中含有三 na 个氧气分子,正确。 也可以计算出约为一点八零六乘十的二十四次方格。 第三题,含有三 na 个养原子的养气分子为三模二三 na 个养原子。记,一点五 n a 个氧气分子。根据公式,小 n 等于大 n 除以 na, 计算出氧气分子为一点五模二三错误。 第四题,零点五摩尔的硫酸分子中含有零点五 na 个硫原子,含有二 na 个氧原子。因为一个硫酸分子中有一个硫原子,四个氧原子,所以四正确。 这节课我们学习了一个重要的物理量,物质的量。注意,物质的量四个字不可增减,不能写成物质量或者物质的质量。魔二是他的单位,规定了一魔二任何例子含义。 阿佛加德罗长数个例子,这个数字同学们一定要记住。约为六点零二乘十的二三次方。 关于公式,小恩等语,大恩除以 na, 要通过课后训练加以巩固同学们化学。
36一剑天涯 22:41
22:41
猜你喜欢
- 4715文老师
最新视频
- 4715文老师

![暑假初升高化学衔接真实课堂:物质的量概念通俗易懂理解,前面内容收音有杂音,后面没有
#初升高[话题]##高中化学[话题]##物质的量[话题]##摩尔[话题]##重庆[话题]#](https://p9-pc-sign.douyinpic.com/image-cut-tos-priv/e6372cd574ed97a1d075f7d693a31439~tplv-dy-resize-origshort-autoq-75:330.jpeg?lk3s=138a59ce&x-expires=2080537200&x-signature=9VRG57qYvNPUtMadOC%2FQttfYOkY%3D&from=327834062&s=PackSourceEnum_AWEME_DETAIL&se=false&sc=cover&biz_tag=pcweb_cover&l=20251208151114132AB37C53ABF80469EB)







