判断分子中某原子的杂化轨道类型
杂化方式的判断是物质结构的必考内容,有很多宝子还是不知道如何去判断,这个视频就再来给你们总结一下杂化方式的七种 判断方法。很多宝子只知道其中的两种或者是三种,因为这几种方法他们之间的判断是相通的,所以我在我的资料里面给你们总结了最常考的几种判断方法,并且还配了一个 杂化轨道类型的判断题目。这是我从一百套题当中挑出来的三十多道非常具有代表性的,并且非常全的杂化轨道类型判断的题目。有资料的包子一定要先自己做,然后再去看视频讲解。下面我们开始来总结 杂化方式的这七种判断方法。第一种方法叫架层电子对法,这种方法它是有两种的,一种是直接法, 一种是间接法,很多宝子学习的是间接法,但是我教的是直接法,因为直接法更简单。我们先来看一下直接法是什么,就是可以直接通过公式计算出夹层电子对数目的方法。 来看一下这个公式很多宝子不知道,如果你不知道,你要把它记下来了,因为真的超级超级好用。架层电子对数 n 就等于二分之中心原子,架电子数加上配位原子提供的 配位数,就是这个公式。配位原子通常是青或者是鲁族元素,比如说氟、氯锈点,养族常见的养牛硒等,氮族呢?氮、磷参等,这是我们常考的配位原子。如果配位原子是青和鲁族,那么他提供的配位数就是一,如果是养 足,提供的配位数就是零,如果是弹足,提供的配位数就是负一,这三个数值需要我们记住,其实也特别好记,因为就是一零和负一。来看一下 怎么运用这个公式,比如说甲烷,我们可以算一下, n 就等于二分之中心原子的加电子数,碳是中心原子,所以他的加电子数是四。氢作为配位原子提供的配位数是一,但是四个氢原子呀,所以是一乘以四,这样加起来,我们算出来的结果就是四。 加电子对数等于四,那么它对应的杂化类型就是 sp 三杂化。再来看碳酸根这种离子,加电子对数, n 就等于二分之,中心原子仍然是碳,它的加电子数是四,加上仰式配位原子提供的配位数是零,那么零乘以三还是零,对吧?因为它带了两个单位的负电 和,所以从外界得了两个电字,我们就再加二,算出来结果是三,对应的就是 sp。 二咋画?再来看三幅画棚, n 就等于二分之棚是中心原子,它的加电的数是三,再加上符, 作为配位原子,提供的配位数是一,有三个符,所以是乘以三,算出来等于三。那蓬原子就是 spr 杂化。再比如说氨基,氨基它是一种官能团,这个单元子它也是要杂化的,那我们来算一算, n 就等于 二分之,但作为中心原子,他的家电的数是五,对吧?清,这里是配位原子两个清吗?所以是一乘以二,这样我们算出来的是三点五,当你算出来是小数的时候,我们就往前进一位,把它变成四就可以了,那么他也 是 sp 三杂画,这是在我的资料当中出现的,我们高中特别常考的一些分子或者是离子,他的家电的对数杂画类型 vsep 模型,固定的对数空间构型是什么 都有。这个图片我已经把它发到 b 站的图文里了,需要的宝子可以自己去下载,自己去算一下。再来看这个间接法,间接法我想很多宝子都非常非常熟悉了, 它是架层电子对数,就等于 sigma 键电子对数,加上中心原子上的孤电子对数。比如说碳酸跟碳作为中心原子,它肯定 跟三个氧之间会形成三个 c 格麻件,所以 c 格麻件电的对数就等于中心原子结合的原子数,那这里就是三孤电的对数,我们带入这个公式去算就可以了。二分 之一 a 就是中心原则加电子数四,因为从外界得了两个电子吗?再加上二,再减去羊,它的最外层是六个电子对吧?有两个是未成对的,减去它的未成对的电子数,一共有三个羊吗?所以这里是乘以三,我们算出来的孤电子对数为零, 那么 n 就等于三,加零等于三,所以碳也是 sp 二,咋画也能算出来这两种方法, 哪一种方法适合你,你就用哪一种方法。第二种方法就是电子式结构式法,如果给我们的物质,他不是 abm 型的,你就没有办法代公式去计算。 这个时候如果我们知道他的结构式或者是电子式,我们一样也可以求出来他的杂化类型,比如说京单二、青四,这是他的结构, 就是蛋上呢,它是有孤对电子的。根据假电子对数, n 等于 c 个嘛建数加上孤电子对数,我们可以算出来 c 个嘛。建三个孤电对是一个,所以旦的假电对数就是四呀,一样可以算出来它是 sp 三大话。 比如说乙缺当中的碳,它是形成了两个 c 格码键,没有固定对,因此它的 n 就等于二,是 sp 杂化。 乙烯,它形成了三个 c 个麻件,没有固定对,那它的加电对数 n 就等于三,所以是 sp 二杂化。我们再来看一下双氧水当中的氧,如果我们知道它的结构了,你就知道它是有两个 c 个麻件的,需要结合一下。电子式 仰上,它是有两个估电子对的,所以加电子对数, n 仍然等于 c 个嘛。建数加上估电子对数等于 四,我们也可以求出来他的杂化类型是 sp 三,这就叫根据电子式或者是结构式来求杂化类型。第三种方法是构型反推法。比如说告诉我们这个物质 说环上所有的原子在同一平面上,这就相当于告诉了我们构型平面构型呀,因此这个羊他就不再是 sp 三了,而是 spr 大话,这样他才可能是平面构型。再比如说这个物质, 他也告诉我们了环上所有的原子都在同一平面上,那因此这个蛋就不再是 sp 三,而是 sp 二大花了, 这就叫构型反推法。第四种方法是派件判断法。比如说这个物质,我告诉你分子中是存在大派件的,并且为平面构型, 其实只要他告诉我们分子中存在大排件,我们就得推出来他为平面构型,那么这个蛋,这个蛋,还有这一个就都是 sp 二大话了,这个蛋就不可能是 sp 三大话,因为 在这个分子当中存在大牌店,一定为平面构型,如果是 sp 三杂画,怎么可能为平面构型呢?第五种方法就是等电子提法。 比如说二氧化碳,我们都知道它是 sp 杂化,这个就是流清酸根,那它的碳的杂化方式是什么呢?它也不是 abm 型,我甚至都不知道它的结构,不会写它的电子式,怎么办?这个时候我们可以运用等电子提法。 电子提法在我的资料里也有非常非常详细的总结,在这里给大家随便举两个例子。比如说二氧化碳,他的夹层电子 加起来就是四加六,加六等于十六,那么流清酸根它也是六加上四加上五,因为得了一个电子嘛,所以还得再加上一,也是十六。他们两个的加电子数之和是相等的,而且都是三个元字, 那么他们两个就是等电子体,等电子体他的杂化类型是一样的,空间构型是一样的,所以碳的杂化类型也为 sp 杂化。再来看一下二氧化硫和臭氧,二氧化硫我们都知道他是什么杂化, sp 二对吧?代公式就可以了。臭氧他也不是 abm 型呀, 我也写不出来他的电子式。那怎么办?就可以用等电子提法,他们两个的架电子数之和加起来都是十八,并且都是三个元字,所以臭氧当中中间氧的杂化方式和流的杂 化方式就是一样的,为 sp 二杂化,这就叫等电子提法。判断第六种方法就是见角反推法,比如说二氧化氯,他告诉我们氧氯氧的夹角约为一百二十度,等 约为一百二十度了,那你说这个绿的杂化方式它应该是多少?是不是应该为 spr 杂化?因为如果你代公式去计算它的杂化方式,比如说 n 就等于二分之七,加零等于三点五,当等于三点五的时候,我们就给它约为四,相当于进了一位,那我们 会推出来它是 sp 三杂化,如果是 sp 三杂化,它的键角怎么可能约为一百二十度呢?所以当题干当中给我们信息的时候,一定要以信息为专,事实上在这个结构当中也是存在大排键的,对吧?第七个就是同族互推法,比如说 二氧化硫和二氧化硒,硫和硒它是位于同一驻足的,并且配味原子都是氧嘛,所以他俩的结构就是相似的,那么硫和硒的杂化类型就是一样的。再比如说双氧水和清二六,二 氧和瘤也是位于同一主族的,并且都是跟两个氢原子去结合,所以他们两个的结构是相似的,那么氧和瘤的杂化方式也是相似的。这就是以上我给大家讲的七种杂化方式的判断方法,你掌握了没有?
粉丝5.1万获赞35.5万
相关视频
 10:00查看AI文稿AI文稿
10:00查看AI文稿AI文稿同学们好,这里是田园课堂,我是廖敏老师。这个视频呢,我们来讲一下砸画轨道类型的判断。第一种方法就是根据驾乘电子队来判断。怎么判断呢?就是驾乘电子对数就等于参与砸画轨道书。 我们举几个例子,绿化皮我们之前说过,他的驾乘电子对数是两对,那么我们就可以知道他参与杂话的轨道数据是两个。那么杂话类型呢?就叫 s p 杂话了啊,因为我们知道 s 加上一个 p 就两个杂货轨道了,所以是 s p 杂话。 再比,比如说绿化盆,我们知道其中的盆圆子加成电子对数是三对,那么也就是他参与杂画的鬼道数,也就是三个杂话类型呢,也就是 spr 杂话了。哎,有 同学就问,难道只有 spsp 二或者 sp 三吗?没有其他的杂话类型吗?有,当然有,只是我们高中暂时不讨论。而你目前接触到的物质,基本上也就是这三种类型的杂话方式了啊,所以不要考虑太多。 那么讲完我们之前说过了,他原子的驾乘电影对数是多少?对啊,四对。那么他参与杂话的轨道数也就是四个杂话类型呢,也就是 s p 三杂话啊,指的就是一个 s 轨道跟三个 p 轨道发生了杂话, 再有氨气里面的大圆子,他的加成电对数是四对杂话类型呢,就是 sb 三杂话。 好,有的同学问,这驾乘电影对数怎么计算啊?我们三节课都讲过了,对不对?好,这里就不深入去探探讨了,自己再回去 看一下,就知道怎么去计算了。第二个呢,根据分子的空间结构来判断啊,现在给一些分子的空间结构,比如说告诉你直线型,那么我们马上就知道他驾乘电的对数是两对,然后转化轨道类型呢,就是 sp 转化。 同样的道理,平面三角形,我们马上知道他驾乘电子对数是三对,从而推出他转化轨道类型是 sb 二杂话,如果是正式面体型的话,驾乘电子对数就是四对,从而可以推出他转化轨道类型就是 sb 三转化。 哎,那么有同学就问我,怎么根据科分子空间结构推出驾乘电子对数啊?啊,之前呢讲驾乘电子对数的计算也都讲过了,所以这里就不多讲了,其实本质上也仍然是通过驾乘电子对数去推出来的,对不对?那为什么这里 还要单独的提出来讲呢?也就是告诉大家,以后呢,我们熟悉之后呢,可以马上的根据分子结构迅速的推出杂号轨道类型 啊,这个过程呢,慢慢的我们会省略不讲啊,比如说直线型,马上想起来它是 sp 涨滑,平面三角形,马上可以想起来它是 sp 要涨滑,正式面体型就是 sp 三涨滑了啊,慢慢的要熟悉这个过程, 然后要特别注意三角锥形呢,他的加成电子对数,我们之前说过了,他是四对,所以他是 sp 三掌滑。 那么有同学问,不对啊,四队的驾乘电子队数不是正式面体型吗?为什么是三角追形?之前的课程我们也提过了,四队可以理解为驾乘电子队的空间结构,或者说空间排列,他是一个正式面体验,但是呢,他的 分子结构是不是正式媒体呢?那么要看他连了几个圆子,如果连了三个圆子,就叫三角锥形,如果只连了两个圆子呢,那就叫 b 形啊,就要看中心圆子连了几个配备圆子啊。 那么杂画鬼的类型,我们知道 sb 章杂画,他也是一个正式面体型 啊,也就是说这个中心原直的轨道砸坏之后,他的轨道的空间结构也是正式面体。注意,是轨道的空间结构啊,就跟驾乘电子队的空间结构意思是一样的哈,都是正式面体啊, 但是由于他中心原子只连了三个原子,所以呢,也就理解为他的空分子的空间结构呢,是三角锥形。好分子的空间结构跟电子堆的空间结构以及转化轨道的空间结构是 不一样的哈,掌握给他的空间结构跟电子队空间结构可以理解为是一致的啊,但是分子的空间结构跟这两个不一定一样啊。 再比如说 v 型的分子空间结构,它分为两种情况,一个是驾乘电子对数是四对的,还有驾乘电子对数是三对的,那么如果是四对的啊,也就是正式面体型, 那么他的杂化轨道类型仍然是 sb 三杂话啊,他的轨道的空间结构也是真实面体性,那么如何形成了 v 形呢?就在于他们中心原子只连了两个原子啊,这也是连了两个原子。 圆子最形象的就是 v 形好,比如说我们说一个掌握轨道,我们来画一下啊,一个大头,一个小头,一个小头,一个大头,一个小头,一个 大头,一小头一个大头。好,这是 s p 三转化的一个。呃,轨道的空间结构啊,实际上是个正式面体型,那么他如果只连了两个圆子啊,我们随便画一个啊,假设这里连了一个圆子,这里连了一个圆子啊,这是中心圆子, 那么好,我们看到它的分子的空间结构就是这个形状的,我们把它给旋转一下,是不是就是这个 v 型啊?好,这个要理解。那么还有一种情况就是三对加成电子对,那么三成加,三对加成电对,它的空间结构应该是平面三角形,对不对? 那么 sps 杂话形成的轨道的类型呢?它的空间结构呢,也是三角形, 但是同样,由于他们的中心原子只连了两个配位原子,他也是 是,意思是连了两个原子,所以呢,呈现的分子的关键结构就是 v 型了啊,就是 v 型,他就有可能有两种情况啊,他的杂货类型也就有两种情况。 接下来我们来举个例子,判断一下这个物质中碳原子的砸花类型,好,也就是实习题啦,大家自己尝试做一下看一下。 那么首先我们要知道,有机物当中的碳原子一般是没有固电子对的,所以画出结构式就可以算出四个码件数也就知道了。驾乘电子对数,那么杂货类型马上就出来了,那我们看一下这个物质它的结构式是怎样的, 这在以前我们是学过了,他就是以息啊,以息的结构是就是这样的一个结构,那么中间的一个探险者,我们选一个吧,或者选右边 也可以哈,我们先选左边看一下,这个探险者连了一个单键清,单键清,再连了一个双键烫,那么这个双键里面有一个是四个麻尖,一个是派件,所以四个麻尖总的加起来是几个?三个,四个麻尖对不对?所以他的驾乘电子对数是多少?三对, 所以杂话的轨道数也就三个,所以他是 s p 二杂话,或者我们也可以根据他的空间结构来推他的杂话类型。好,那么我们以这个摊位中心的话,那么旁边连的原子都叫配位原子了,我们把这些配位原子用线把它连起来, 我们看到他是一个什么形状,平面三角形对不对?好,那平面三角形的一个结构,这个杂话类型马上就想出来是 sp 二杂话了啊,当然或者你可以先推出他的驾乘电子对数啊,是三对 啊,然后呢再推杂话类型是 spr 杂话,那么这个探险者呢?是完全一致的哈,跟左边这个是一样的,也是 spr 杂话。那么接下来我们来探讨一下这些杂号轨道如何形成了四个码件又如何形成了太监。首先 左边的这个碳原子呢,它的杂话类型是 spr 杂话,那么它形成的轨道的空间结构呢?也就是一个平面三角形的一个结构, 那么我们从侧面看过去啊,大概就是这个样子的,那么注意,我们这个碳原子砸画的是三个轨道, spr, 那 p 轨道还有一个对不对? 那么他是没有参与打画的,上面还有个垫子啊,那么我们把它画下,本来 s 轨道上面是有两个垫子的,然后 p 轨道上面有两个垫子,这是碳原子的 驾乘电子排布对不对?那么现在我们砸画之后呢,这个电子先会跳出来,对吧?跳出来之后砸画的话, s 跟两个屁砸画就变成了这样的一个结构, 还剩下这一个屁没有,咋画在旁边,对吧?好,这三个,呃,轨道呢?我们已经画出来了,那么这个轨道在哪里呢? 这个轨道是个屁轨道,实际上是垂直于这个平面三角形的,那么从这个角度来看的话,实际上就是这样子垂下来的, 那么另外一个太原子也是一样的哈,也是这样的一个杂话,还剩下一个屁轨道,然后这两个太原子形成公家界是怎么形成的?是相互靠近之后,这个轨道跟这个轨道发生了 头碰头,电子云重叠,然后形成了四个码结,然后靠近到一定程度,这个屁轨道跟这个屁轨道是相互平行的,然后呢开始重叠形成了肩并肩的派,呃,派件啊,肩并肩, 这也也就是形成了碳碳酸碱的过程了啊,一个是这个马键,一个是太监, 那么这个视频就讲的差不多,我们总结一下,首先我们根据驾乘电子队速判断了杂号轨道数,然后呢,我们还可以根据分子的空间结构判断了杂号轨道数。 最后呢,我们举例子了解了一下啊,以西的他的探员的转化类型,还有他形成控压键的一个过程,那么这个视频就讲到这里,再见。
214虚空之遗 03:59查看AI文稿AI文稿
03:59查看AI文稿AI文稿在上节课中,我们知道很多原子在形成共价键时,会发生轨道的杂话,有 sp 三杂话、 sp 二杂话和 sp 杂话三种。 由于 sp 三杂话轨道是成正四面体的分布, sp 二杂话是平面三角形的分布, sp 杂话是直线型的分布,就造成了不同的分子有不同的空间构形。 我们今天就来总结一下如何去判断 abn 型分子的空间构型以及中心原子的杂话方式。 在 abn 型分子中,我们根据 b 原子的不同分两种情况来看,第一,如果 b 是轻原子,有素原子,这种就看成一个 b 原子对 a 原子提供一个电子。第二种情况, 如果 b 原子是养原子或者留原子,我们则看成 b 原子不与 a 提供电子。第二步呢,我们就去计算 a 原子上一共有多少个电子参与杂话,就是将 a 原子的最外层电子加上 b 原子提供的电子。 第三步,将参与杂话的电子数除以二,得到的数字就是杂话轨道的数量,也就是下层电子对数, 一共会有三种情况,当然,杂话轨道数是二,那就是 sp 杂话分子就是直线型,当轨道数是三,就是 spr, 杂话分子呢,就是平面三角形,轨道数是四,就是 sp 三杂话就是正四面体了。 光看方法是不是觉得有点复杂,我们用栗子来试一下,就会发现,方法其实还是很简单的。 四绿化碳,中心原子是碳,绿原子给碳提供电子,一共四个绿原子就是提供了四个电子,再加上碳最外层的电子数,一共有八个电子参与杂话,那么轨道数就是四。嗯,四绿化碳是正四面体没错, 再看氨气,三个轻圆子提供给蛋,一共三个垫子,加上蛋圆子最外层的五个垫子,一共就是八个垫子参与杂话。 没错,大圆子也是 s p 三杂话。不过由于在安气中,大圆子的四个杂话轨道只有三个是形成了共价键,还有一个轨道是一对孤队电子,所以在正四面体的基础上矮了一截,所以安气就是三角锥形了。是不是很简单呢? 掌握了分子空间构形的判断,我们再来延伸一下吧,看看离子吧,我们就用俺跟离子和碳酸跟离子来介绍一下。方法其实很简单, 先不看离子所带的电鹤量,用刚刚的方法计算出参与杂话的电子数量,然后呢,再算上离子所带的电鹤量, 就是离子中参与杂话的电子数了,这个数除以二就是驾乘电子对数就可以判断了。比如俺跟离子半圆子最外层是五个电子,四个轻圆子提供四个电子, 但是俺跟李子是带一个正电鹤的,所以还要再扣除一个电子,那么参与杂话的电子数就是五加四减一等于八,所以俺跟李子中半圆子 也是 sp 三杂话,但原子连接了四个轻原子,所以板根离子的空间构型就是正次面体。再试试碳酸根,碳原子最外层是四个电子,两原子不提供电子, 碳酸跟离子带两个负电荷,所以再加上两个垫子,一共就是四加二等于六,六个垫子参与杂话, 下层电子对就是三,所以是 sp 二杂话。碳原子连接了三个氧原子,所以碳酸根离子就是平面三角形结构了,怎么样?简单吧?
331化学星 07:47查看AI文稿AI文稿
07:47查看AI文稿AI文稿第七讲杂话轨道理论。大家好,今天分享的是高中化学选秀二第二章第二节杂话轨道理论的内容,点赞收藏加关注,防止需要的时候找不到 这块的内容呢。其实相对来说解释起来还是比较复杂的,但是考试考起来呢,却是非常简单的,咱们从两个方面先解释一下这个理论到底是怎么回事啊?为什么轨道要砸化?然后咱们再讲一下考试的时候我们应该如何解决考试的试题, 考试的事情解决非常简单,但是理论我们也要理解。首先第一个,为什么轨道要发生杂话,那么我们呢,以甲完为例来解释一下这个事,甲完四 h 四非常熟悉,甲完的电子是怎么写呢?一个碳连接了什么?四个青和每 每个清之间都形成了一个共用电子,对,也就是说探出了一个电子,清出了一个电子,对吧?形成了共用电子,对,那我们思考一个问题,清肯定用的是什么清?最外层只有一个电子,就是 es1, 他肯定用的是自己的 es 轨道当中那唯一的一个电子 去和谁呢?去和探当中某一个轨道上的某个电子去形成共用电子,对,这对共用电,对,既会在 s 一轨道一 s 这个轨道上旋转,又会跑到什么这个碳的那个轨道上去旋转, 那我们就得思考碳那个轨道是哪一个轨道和这个氢融合在一起了呢?那我们这里我们就知道了,这个碳应该是谁去呢?最外层电子对吧?碳最外层有四个电子,是这四个,最外层四个电子, 这个轻形成供应链的。对了,我们写一下碳的什么电子排布式碳是一 s 二,然后呢?二 s, 二,二 二 p, 二最爱层四个电子,也就是说我们在可以再画一个什么,画一个这个图像啊,这个就是什么他的二 s 轨道里面有俩电子, 然后的话还有谁呀?还有二批轨道,这二批轨道能量比二 s 要略高一些啊,有三个轨道,这一个电子,这一个电子, 那这样的话不行。为什么?这样的话二 s 轨道是一个天中满的一个状态,是不可能和轻形成什么形成这个共用电子?对的,所以呢,要在和轻形成共用电子之前,先把这个电子调整一下,这个电子拿走放到这, 这样的话每个轨道上电子怎么样都是一个半充满状态,允许轻再提供一个什么一个电子过来形成更多电。对,但是有一个问题了,如果你是轻,请告诉老师, 你是把自己的电子打算和二批轨道上的这个电子形成供应链,对,还是和二 s 呢? 他就会产生一个分针,对吧?我们说这就叫选择困难综合症,当你有选择的时候,你就会挑剔,凭什么?我哥四个清来了,对吧?有一个清就非要和什么这 s 轨道融合在一起,不和 p 轨道融合在一起呢? 这就是一个问题。那这个时候碳为了解决这个纷争,他想到了一个办法,我有四个轨道,一个 s 轨道,三, 三个 p 轨道,那我可不可以把这四个轨道怎么样融合在一起,然后重新怎么样划分?这个我就不要了,变成一个什么能量居于 p 轨道和 s 轨道之间的一个新轨道,这个轨道名称就叫什么 sp 三轨道, 他叫 s p 三轨道,这个叫不叫?这个也叫,这个叫不叫?这个也叫。这四个新轨道都是 s p 三轨道,很特殊,他的能量介于 p 轨道和 s 轨道之间的一个新轨道,然后每个轨道怎么样?电子都放一个,那你清来了,是不是每个轨道都可以容纳轻的电子一个,对吧?这就很容易, 这就是为什么要进行轨道砸化,从二 s 轨道二批轨道融合成四个 sp 三轨道,这个过程就叫做砸化轨道理论解 是清楚了,那上节课咱们在讲什么?呃,公家舰的时候咱们没讲啊,学校老师会讲公家舰的时候说过哈。这个,我们说这个有西戈马舰,有派舰,一般双舰当中就是一个西马舰,一个派舰, 那么七个马键这里又形成了什么?原子与原子之间你竟然形成共价键了。有什么 ss 七个码键啊?就是代表 s 轨道上电子和 s 轨道电子形成共用电子段。那 s 轨道和 p 轨道呢?就是 sp 七个码键,或者叫 pp 七个码键。 那甲完这种碳和轻之间的共加键应该叫做什么西格玛键呢?轻用的是 s 轨道对吧?碳用的是什么 sp 三轨道,所以碳轻用的西格玛键应该叫做 s 杠 s p 三西格玛键啊,它是这样的一个西格玛键, 咱们就解释清楚了。好,这是第一个考点,第二个考点给你一个分子,比如说咱们熟悉的甲烷,比如说熟悉的什么二氧化碳流,比如说熟悉的暗器,问你什么中心原子,他叫什么轨道?杂话是什么杂话? s p 三吗? s p 二吗?还是 s p? 那这个怎么看?非常简单,一个小技巧,不需要纠结那么多原理,你就记好查中心原子周围的电子队 啊,不是电子座啊,应该叫做电子团。哈,这个很关键,电子座你能数出来电子团是什么?有的那个形成双电的两根电子放在一起的,对吧?放在两个圆子中间的,形成这个两个共加,两根共加键的。这种啊, 通通算上一团电子。那我们知道探探周围是几团电子?四团,对吧?四个成见电子队, 四团电子,所以他是什么? sp 三,二氧化瘤。上节课咱们讲家庭电子护持理论的时候说了二氧化瘤,这里面瘤有一个固顿电子,还有怎么样两团和养的承建电子。对,所以他周围是三团电子,因此是 sp 二杂话,安系周围是多少?三个城建电子队和一个孤军电子队,所以他是 s p 三。如果说他是一个什么特殊的,就是说这个是两端的,比如说谁呢?这个一圈 cra 三啊,我们画他的一个这个结构点式结构式吧,我们说也乙圈,乙圈当中这个碳原子怎么样?换这边啊,换,换那边。老师头像 挡住了,看不到乙圈对吧?碳原子中心原子,他的左面有一个供应电线墩,对吧?右面有三对供应电线墩,但是老师说按团算,这是一团链子,这也是一团链子,他有几团链子,两团链子,所以乙缺当中的碳是几杂话? s p 杂话, 那如果说你这个原子和其他,比如说绿化清,对吧?你中间就有一个规则电子,那你这个就不用砸化了,哈哈,没得挑没得选,就有一个功能,电子轨道一样就可以了啊,不需要纠结砸化的问题。好吧,记清楚了,砸个轨道就属什么中心原子周围 孤队电子,加上什么城建电子队的,一个团数就可以了啊。有几团电子就对应的一团电子不用砸话,两团电子 sp 三团电子 sp 二,四 团电子 sp 三。那五团呢? sp 三六团呢? sp 三永远的哈大于四团之后都是 sp 三杂话。好吧,这个内容呢,老师就讲到这,有任何问题评论区老师互动,拜拜。
8327范老师的化学自习室 01:06查看AI文稿AI文稿
01:06查看AI文稿AI文稿同志们好,我们用三种方法来判断分子中心原子的杂话类型。第一个,根据驾乘电子对数来判断。驾乘电子对数为二,那就 sp 杂话为三为 sp, 二杂话为四为 sp, 三杂话 根据结构简式来判断。结构简式中,若碳、蛋等原子形成,单建设为 s p, 三咋画,双建设为 s p, 二咋画,三建设为 h p 咋画。 第三,根据等电子原理进行判断。如二两化碳是直线性分子,这种根和蛋三根与二两化碳是等电子体,所以分子的勾形均为直线型,中心原则 均采味 sp 杂话。所以说我们通过这几种就可以判断他的杂话的类型,希望大家好好的体会去掌握好,再见!
67化学有道 05:01查看AI文稿AI文稿
05:01查看AI文稿AI文稿好,今天我们继续来看一下如何来判断杂烩类型以及分子的构型,那么再回一起回顾一下判断方法。首先第一个我们先怎么样呢?先要判断中心原子加减对数, 那么中轩子加减数等于什么呀?他等于中轩子的加减数加什么呀?周围轻或鲁肃原子个数或者什么呀?加上或减去所在定格数,同时整体除以二。 那求出中心原子加点对数之后怎么办呢?根据中心原子加点对数判断其杂化类型,如果说其等于二,那么就 sp 杂化等于三, sp 二等于四, sp 三杂化, 然后再怎么样啊,再算出其孤电对数,那么孤对电子数啊等于什么?它等于刚才求的值,中心原则加电对数再减去什么样?配位原则数,然后求助孤电数之后接下来判断什么呢?分 构型对吧?哎,那我们一起来看看这道题。看两个题啊,第一个以硫酸跟离子为例,那我们来如何来判断硫酸跟离子的杂化类型呢?那么首先第一个还是按照步骤。第一步我们先怎么样啊?先判断中心原子的中心原子 加电子对数,那我们来看一下它是不是等于 整体哎,除以二对吧?什么除以二呢?中心原子的加电子数,中心原子加减数留对吧?哎,这不就相当于中心原子吗?留多少啊?加电子数是六对吧?然后加上 周围清或卤素原子个数有吗?哎,没有,所以说加几啊?零呗,然后再加减所在电和数。那你看这,我这是 带两个单元附件和是不是应该得到两个电子啊?所以说我加二对吧?哎,这值正确的几啊?等于四,就这块啊,不要整,不要整错,因为什么呢? 你要是带两单负电荷,证明得到两电子,所以加二。带两个负正电荷呢?是证明失去两电子,所以减二,这数字不要错啊。然后中心那么原子加电的数等于几啊?四了,那接下来这是几啊? 这等于 s p 三大化,对吧? s p 三大化,然后接下来再来判断什么呢?第三步,判断一下 孤队电子数。那孤队电子数等于什么呀?等于中心原子加电队数四,对吧?减去什么呀?减去配位原子数,那配位原子数在这呢吧,四个对吧?哎,减四等于零,也就是什么呀?他没有孤电队啊, 对吧?没有孤独电子啊。所以第四步,我们来看一下分子构型。分子构什么呀?中心流对吧?哎,一共什么呀?四个?中心 原子加减,对,所以说有四个坏键,哎,四条,然后分别连什么呀?四个氧啊?二三四,这什么结构啊?叫正四面体对吧?哎,正四面体结构 同理啊,看第二个,那么三六化磷,那么这里头啊,也是一样。第一步,还是这样判断一下中心原子的假电子对数, 哎,那么重要的加减数,对数得几啊?等于零零的七 下电的数为多少啊?等于五,对吧?哎,然后接下来还是一样加减周围什么呢?氢或卤素原则脱数,那么这样浮绿嗅点,哎,里头是不是有绿啊?所以几个啊?三个加三,然后加减所在电的数,他没有电和,不用管了,整体再除以二等于四, 然后还是这样,中心原子加电,对,等于四,所以说还是属于 s p 三杂化,对吧?哎,今天讲的都是 s p 三的,然后接下来那么第三个我们来判断一下孤对电子数, 那孤队电子数等于什么呀?等于中心原子的加电队数四,减去什么呀?减去配电子数这几啊?三等于几啊?一,哎,证明有一个孤队电子,对吧?孤队电子数啊,是看不到的啊,孤队电子看不到,所以说我们来看一下它的分子构型什么样的? 哎,你看也是一样,中心一个林,然后中心原子加电都是是不等四啊,所以有四条键出来,对吧?然后接下来那么这里头有一个什么呀?有一个孤独电子吧,所以有一个是看不到的,哎,这个看不见, 然后再来其他这三条分别连接什么呀?三个绿,对吧?来三个绿 a o, 把它画一下,对吧?那这看不见的不用去管它最终这结构应该什么形状啊?是不是一个零,然后这一个绿, 这一个绿,这一个绿,那这叫什么形状?这叫三角锥,对吧?哎,这就是咱们常说的三角锥形, 那么你学会了吗?我们来看一下下面几个练习,明天我们继续分享这四个练习如何来做好。
63日常说“化” 17:57查看AI文稿AI文稿
17:57查看AI文稿AI文稿好,今天我们来讲一下分子的空间构型啊和分子的杂化轨道,那么我们来看一下啊,对于这种杂化轨道的计算方法啊,我们只需要一个公式啊,就可以完成啊,秒杀。那么这公式是什么呢?首先我们来看一下啊,对于 a b m 型分子啊, a b m 型分子,也就是说,比如说像水, 对吧?他就是属于 ab 二,对吧?比如说氨气,他就是 ab 三,比如说甲烷,他就是 ab 四,再比如说三氯化磷,对吧啊,他就是 ab 三,类似这个东西啊,我们把它归类为 abm 型分子啊, abm 型分子,那么你看一下这个杂化轨道数 x, 也就是下层电子对数,他就等于二分之一中心原子的最外层电子数。那么中心原子的转成电数是啥意思啊?比如说中心原子像这个是氧元素,氧元素的最外层电子是多少?是六,那这个时候就带 直接带六就行了,加上它的配位数,你看中心原子是阳,那配位原子是谁呀?配位原子我们默认为它是什么?它是氢元素对不对?那这个时候它配位数就是多少,它配位数就是二,能理解吧?如果是 离子,那这个时候加上或者是减去离子所带的电和数,加减离子所带电和数,所以这里面的话,我们应该说的是 a b m 型微粒啊,这个应该改成微粒, 啥意思呢?就是说分子或者是离子,它都是可以适用的分子或者是离子啊,对于这个公式,它都是可以适用的,那么我们首先来看一下啊,一定要先记住,这公式等于二分之一的中心原子的最外层电子数加上配备原子数,那么这个配备原子这边要强调一下,如果配备原子是养牛时, 那这个时候配位数末了为零,这个是在计算过程中需要注意的点,如果配位原则是养牛时, 这个时候配位数我们是按零带进去算的,能理解吧?然后再加上或者是减去离子,得到或者是失去电子数,能理解吧?得失电子数,那么现在我们来看一下这个 abm 型分子。首先的话,我们来看一下什么是中心原子,中心原子的话,一般我们说的是原子个数较少,原子个数较少,或者是 原子个数较少,或者是呈现的数母是最多的,那你看一下对于 a、 b、 m 型,首先 a 它只有一个原子,所以一般情况下 a 它原子个数较少,它就是中心原子。那么谁是配备原子呢?配备原子的话,一般就是原子个数较多的那一个 原子,个数较多的那个原子。所以的话,这里面啊,我们首先要分清楚谁是中心原子,谁是配备原子,分清楚以后就按照这个公式代入计算,就可以算出杂化轨道数啊。杂化轨道数,知道杂化轨道数以后就知道 它是 sp 几杂化啊?知道它是 sp 几杂化,比如说啊,比如说我们举个例子,比如说氨气,对吧?氨气,你看一下这个杂化轨道数, x 等于 sp 的 x 减一等于 二分之一。什么蛋的最大增变数是几?是五,对吧?中心原子是蛋吗?那么他的配备原子数是谁?是氢?配位原子个数是氢,那氢的配备数是三,所以二分之八等于四,四减一的话,他就是 sp 三转化, sp 三转化能理解吧?所以用这个公式去算的话,我们会发现杂化轨道 数的计算方式是非常简单的。那我们再比如说啊,如果是二氧化硫呢?这个时候打好轨道数 x 是等 sp 的 x 减一等于什么?二分之一的中心原子的最外层电子数,这个时候中心原子是谁呀?中心原子是瘤,瘤的最外层电子数是多少?是六。那这个时候配比原子是谁呀?配比原子换一个 颜色,配备原则是氧。我们讲过,如果说配备原则是氧或者是流时,它的配备数只能记为多少啊?只能代表的是零计算,所以这边是二分之六加二,零等于多少?等于三,等于三的话,它就是 s p 二的话,它就是 s p 二的话,能理解吧?那么这个是分子中 杂化方式的计算方法,当然了也有可能是离子,那如果是离子的话,我们看一下啊,如果说离子啊,我们在上面写,比如说氨根离子 啊,我们用红笔吧,比如说氨根离子,那同学们看一下,如果说这个是氨根离子的话,杂化轨道数 x 还是等于 s p 的 x 减一等于什么?二分之一的中心原子的最外层变数。中心原子是谁?是蛋,蛋的最外层是五个,加上它的配位数是氢啊,它配位原子是氢,加上配位数是四个,对吧? 但是因为它是什么氨根离子,氨根离子的话,它要带上一个单位的证件,所以这个时候它要减一,它要减一,那这个时候就等, 等于二分之八,就等于四四的话,它就是 sp 三角化, sp 三角化,所以如果是离子的话,你要加上或者是减去它所得到或者是失去的相对应的电子数,能理解吧?啊?我们再举个例子,比如说碳酸根,离子, 碳酸跟离子,那碳酸跟离子中中心原子是碳,碳的杂化方式, x 就等于二分之一中心原子的转成电数,中心原子是碳,碳的转子电数是四, 对吧?那你看一下这个数配备原则是谁?配备原则是氧,氧的话他的配备数我们说的是代入是什么?是零不能算啊,代的是零,那么这个碳酸根整体是得到了两个单位的电子,所以他应该再加啊, 那它就等于三,所以它是什么? sp 二杂化?碳酸根中的碳原子是 sp 二杂化,那么这个是杂化轨道数的计算方法。如果不是 abm 型,那比如说有机物,有 机物中碳原子的杂化方式,那么我们来看一下有机物中如果是碳碳单件,全部是碳碳单件单件的话,它是什么杂化? sp 三杂化,单件是 sp 三杂化,那如果是双键呢?碳跟碳里面存在一个双键,那么你们要记住它是 sp 二杂化,双键是 sp 二杂化,那么如果是三件呢? s p 打发,能理解吧?三件是 s p 打发,所以这里的话自己啊,首先要记清楚有机物中碳原子的打化方式,我们只看它形成的碳碳之间的化学键,那到底是单键还是双键,或者是什么三键,对不对?那我们来看一下啊,比如说已完, 已完是碳二氢六,对不对?我们知道一个碳原子他可以生出四条化学键,那么每一个碳可以生出四条化学键,那你看一下碳二氢六里面,其实的话相当于是什么一个氢啊?一个碳原子,应该是一个碳原子,他已经分走了 三个氢链子,一个碳是分走了三个氢,那一个碳分走了三个氢的话,也就是说一个碳已经跟三个氢形成三条共价键,这个时候碳跟碳之间只能是什么单件,所以你看它是带这样的,所以这里面的话,碳跟碳之间是单件的话,它就是什么 sp 三杂法,有机无踪 乙原着碳原子的杂化方式,那就是 sp 三。接下来我们看一下啊,如果是乙烯呢?乙烯啊,碳二氢磁,那你看一下一个碳它其实是平均分了两个氢原子, 一个碳分成两个氢,那碳总共可以伸出四条化学键,所以你看一下这里面碳他还剩余两条化学键,所以这个时候碳跟碳之间形成的是什么键?是单键啊?成成成的是双键啊,口误, 碳跟碳之间形成就是双键,那如果是双键的话,它就是 sp 二的话,双键就是 sp 二的话,能理解吧?再比如说乙缺碳二氢二, 那以前他二清二号,我们可以看一下,平均一个碳原子是分一个清,那一个碳可以伸出四条化学键,剩余的三条键就是碳碳三键。 所以你看碳跟碳之间是形成三条化学键,那这个时候他就是遵循的是什么 sp 杂化,因为他是碳碳三件,所以同学们一定要记住啊,有机物中碳原子的杂化方式,单件是 sp 三,双件是 sp 二,三件是 sp 杂化,这是第二种杂化方式的判断,那最后一种根据空间过程来判断, 根据他的空间过程来判断,比如说立体结构, 它如果是立体结构的话,我们就默认为它是 s p 三掌法,比如说我们后面学到的金刚石啊,它就是立体结构,它就是 s p 三。再比如说平面结构,面结构是 s p 二掌法,平面结构是 s p 二掌法,比如说本环中本环中碳原 数的砸画方式,因为本环里面所有的探探键,它都是介于单键和双键之间一种独特的化学键, 它既不是单键,也不是双键,所以这个时候你判断的时候,就没有办法根据上面说单键、双键、三键啊去判断它杂化方式。但是我们知道本环六个碳原子和六个氢原子全部是共平面的啊,只要是平面结构,它就是 sp 二杂化。第三种情况,如果是直线型的话,它就是 sp 杂化,比如说二氧化碳,它是直线型, 二氧化碳中碳原子就是 sp 杂化。所以你们记住啊,杂化方式只需要记住这三个类别就行。分子的立体构型,分子的立体构型,那么再看分子的立体构型的时候,我们要讲一下如何去判断该分子的立体构型。 第一种情况,对于 a、 b 二型分子,中心原子如果说没有孤对电子剩余,它就是直线性, 如果说有固定对象语言,那这个时候是微信,那这个怎么去判断呢?那么要去判断这个之前,我们首先要了解一个 a、 b m 型,讲过 a b m 型里面 a 是中心原子,中心原子是提供电子的, 那 b 是什么呀? b, 我们这边说的是 k 位原则。 配味原子是干嘛的?配味原子是来拿电子的, 所以 a、 b、 m 型里面一个是提供电子,一个是来拿电子,那么这个中心原子最多可以提供多少个电子呢?他提供的其实就是电子数,就是看最外层电子数,他有多少个电子,那么他就能提供多少个电子。如果说最外层有六个,他被拿走了四个,那就是意味着他还剩两个,那就是有孤电子。对剩余,这样的话 就是有固定的对手。鱼能理解吧?比如说啊,比如说水,那么我们知道在 hro 里面中心原子是氧,对吧?中心原子,中心原子的话,你看氧要从几个?六个, 对吧?那轻的话,你看轻是来拿电子的,一个轻离两个电子的稳定结构,还少几个电子呢?还少一个电子,一个轻拿走一个,两个轻就拿走两个,这个时候他剩余的是四个。四个电子,那么四个电子的话,他就相当是有两段 孤电组队,那这个时候 h、 r、 o 它就是有孤电,对剩余,有孤电,对剩余的话,它就属于什么型,它就属于微型。 在这里微型如果说他没有固定的对称为,他就是直线型,比如说二氧化碳,二氧化碳的话,我们知道中心原子是碳,碳的转层电数是四个,对不对?那么偏微原子是氧,氧的转层电数是几个?六个, 六个离八电子的稳定结构还少几个?还少两个,对吧?一个氧意味着他要达到八电子的稳定结构,他还需要再得到两个,那一个氧拿走两个,两个氧就拿走了四个,这个时候相当于碳最外层点数全部被氧拿走了,那这个时候就是没有固定的一条鱼, 没有固定的最剩余,没有固定最剩余的话它就是呈现,它就是直线型,你看这个水,这个水,你看它的结构是路易石结构,结构是是这样的,也就说你看一下养了最爱成长树是六个,六个的话你看一个跟青共用, 这里面一个金跟金光,另外一个,一个另外一个青光,对吧?那你看一下这样的话,这个水中的氧,也就是中心原子氧的转成电速是六个,对清共用了两个,还剩几个?还剩四个,四个就是两段,看到没有四个的话就是两段。那么如果说你是求他的 v、 s、 e、 p、 r 模型的时候, 他这个 vsepr 模型里面是含孤电子队的同学们,他这里面他说的是含孤电子队的,那么含有孤电子队的话,意味着你看这边一个孤电子队变成了一条化学线,这边一个孤电子队他也变成了一条化学线,所以这个时候变成了什么? 四面体结构,那这个时候他的空间构型变成了什么?四面体结构。那么如果他求的是分子的立体构型,分子的立体构型,那么这个时候是把这个固垫子对给省略掉,直接把这固垫对省略掉,那也就说上面这两对还有没有了,没有了没有的话他就是这样一个形状,这样的形状我们称为是什么?微型啊?微型或者是角形, v 型或者是角型,能理解吧?好,接下来我们再看一下下面这个,你看氨气,氨气的话,你看中心原子弹弹出来沉淀数是几个?五个,弹的最外层电阻数是五个,那么弹的最外沉淀数是五个的话,你看它跟三个青共用了三个,还剩什么?一段古典 对还是一对固定对,那么他有一对固定对。剩余的时候,如果说你在写他的 vsepr 模型里面,你看他就要把这一对算上,然后这边一条件,这边条件,这边条件,他形成的是四个,所以那些什么四面体型,四面体型,那如果是立体构型的话,你看把上面这一对固定的对直接给省略掉,把上面这对固定的对给他省略掉,上面这对固定对省略掉以后,他就变成了什么三角锥形, 三角锥形,所以你一定要去判断一下什么是 v s e p r, v s e p r 的话,其实是他把孤电子队,他把这里面的孤电子队也给他算进去了,能理解吧?孤电子队把他算进去了,那么孤电队如果说算进去了, 那孤电一对孤电子队就相当于是一条化学键,一对孤电子队就相当于是一条化学键,能理解吧?所以你在算他的这个空间构型的时候,那就不太一样了,那就不太一样了。那你看一下这个是含有孤电子队的,如果说他没有孤电子队,那这个时候你会发现没有孤电子队 的话,它的 v s e p r 的模型和它分子的立体构型它是一样的分。好,现在我们来看一下这个,我们把这个表格研究清楚,它基本上 这里面所涉及到的啊,什么价电子对数对吧?价成电子对数、孤电对数、中心原子的杂化分子、过离子的立体构型,包括 vsepr 模型,基本上我们都能啊,轻松应对,我们都能轻松应对。 比如说算这个硫化氢,它的固定对的数目我们来算,我们讲过了,中心原子是硫,硫的重要层电子数是六个,对吧?中氢原子是给别人提供电子的,它最多可以提供六个,那么这个配比原子是氢, 那么轻是来拿电子的,轻是两个电子的稳定,结果他拽成原本自己已经有一个了,这个时候再拿走一个,就达到了两个电子稳定结果,也就是说一个轻只需要再拿走一个,那这里面的话有两个轻,所以他拿走的是两个,他就是有四个固电子对称于, 既然有四个孤电子队的话,他这边算的是孤电子队的数目,所以这边如果说算对数的话,那就是二啊,他剩余的是两对,但是他有四个孤电子剩余,所以这里面说的是两对。 三、氧化的中心原子是瘤对不对? pm 原子是氧,氧的最外层电子数离八电子还少两个啊,你看一下,氧是第八号元素,他是二六,对不对?二六的话离八电子还少两个,离八电子还少两个的话, 那他达到八电子的稳定结构,他就必须要共用两步,也就是说一个氧元子拿走了两个电子啊。那你看一下,他总共有三个氧元子,那这个就是二乘以三,这个时候呢?等于零,等于零,所以这个时候固定对没有啊?没有他就是零。好,接下来我们再看一下 甲烷的啊,固定对称鱼,那你看甲烷的中心原则是碳,碳的转成电数是四个,对吧?一个氢拿走一个,四个氢刚好拿走四个,所以他固定对称的也是零。 好,接下来我们看三绿化氮,氮的转乘电数是五个,对吧?那么绿的转乘电数是七个,离八电子稳定结果还少一个?一个绿拿走一个,三个绿拿走三个,他就是等于二,等于二的话,他就是有一对孤电对称于有这个轻轻酸。有些同学说,老师,我现在 不知道他的中心原子是谁了,为什么?因为我们之前讲过,他是 abm 型的时候,原子个数较少的那个是中心原子,但是你看现在的话,所有的原子个数都是一个呀,那怎么办呢?那这个时候我们来看什么?我们来看城建电子对数最多的那个, 呈现电子对数最多的那个就是中心元子。那我们来看一下氢要达到两个电子的稳定结构,他只需要再共用一对,对不对?那么碳要达到八电子的稳定结构,他需要共用几对?四对,为什么?因为碳的转成电数是四个呀?你要达到八电子,是不是要共用四个?那么氮呢?氮元素的转成电子数是几个?五个,他离八电子稳定结构还少几个?还 少三个。所以我们来看一下蛋的钻石电数是四,他的共用电子兑数是最多的,也是四多。所以这里面的中心原子是谁呀?中心原子是碳元素, 那像中心原子碳的话,你看他四对供电队轻拿走了一对,是不是?然后氮元素拿走了三对,所以他剩余是零,他就是零对,固定对,明白吧?剩余的固定对数目就等于零。好,接下来我们再看一下磷酸根, 那我们来看一下这个磷酸根,它有没有固定对称鱼呢?首先我们来看一下零的重要沉淀数是五,对吧?但是它这个是个离子的,看到没有?它是一个阴离子, 阴离子的话,你要加上他所得到的电子数,他带上的是三个单位的负电,所以这边需要是五加三,对吧?这个三指的是得到三个电子数,然后你看一下啊,一个氧是拿走两个,四个氧是拿走八个,他刚好生命在这里,所以他估电子对数是多少?是零,那加成电子对数是怎么算呢?等于二, 二分之一,中心原子的转乘电数加二分之一,中心原子的转转电数是六,加上硫化金的配位数是二,等于四啊,所以它的加电加成电子倍数就等于四,等于四的话,它就是 sp 三转化,那三氧化硫呢?是等于二分之六等于三,它是 sp 二转化,能理解吧? 他讲完了,讲完是二分之碳原子转能电数是四,加胚原子数是四等于四,他就是 s p 三。如果是三氯化氮呢?氮的转程电数是五,加上他的绿原子的配比,原子数是三,那就等于二分之八等于四,他也是 s p 三。那么这晶晶酸呢?晶晶酸的话,很明显他是直线型的, 但是直线型的直线型是 sp 打法。那么磷酸根呢?你看一下零的最外成见数是五个,零的最外成见数是五个,对吧?然后你看配位原则是氧,配位原则是氧环的,这个时候需不需要算法,这个时候不需 要去算,那就是五加三等于八,那就是四四的话,它其实就是 s p 三角,能理解吧?那我们来看一下分子的立体构型,如果是硫化氢的话,它是有固定对称鱼的,它就是微型三氧化硫的话,它没有固定对称鱼,所以它是平面三角形。 平面三角形,那你看甲完是正四面体,因为他没有固定对称于,对吧?三氯化氮呢?三角锥形,他有固定的对称轻轻酸,他是直线型。 磷酸根呢?磷酸根是 p o 四啊, p o 四它属于正式面积,那么如果算它这个 v、 s, e, p, r 模型,你看一下,如果说它固定的倍数是等于零的,你看三氧化硫、甲烷、氢氢酸、磷酸根这些物质的这个 v、 s, e, p、 r 模型跟它的立体 柱形是一样的,因为它的固定字对数是等于零,能理解吧?那这个时候我们来看一下固定对数不等于零的,你看这个是两对,那么它就是四面体。 好,这个话你看它有一度固定,对上语言它也是四面题啊,直接写四面题,那么这个就是固定的对数中心原则的杂化方式、分子等立体户型,包括 v, s, e, p、 r 模型啊,所涉及到的一些知识点。
 04:17查看AI文稿AI文稿
04:17查看AI文稿AI文稿中心原子杂话轨道类型的确定,一个是根据威力的结构、空间结构来判断。 若为正四面起 或三角锥形, 说明 s p 三咋画, 这里要注意,正四面起没有估电子罪, 三角锥形有一个固定的,对,这样他的 架层、电坠模型都是正四面起,所以是 sp 三杂化。当然分子形状是不一样的,因为一个有孤电子队,一个没有。 如果为平面三角形, 那么砸画为 s p 二砸画, 因为对称没有估计样子,对三个 c 跟把键自然是 sp 二杂话,如果是直线型 很对称,就是 sp 杂话,这里要注意, sp 三杂话, 剑角一百零九度二十八分, sp 二杂话,剑角一百二十度, sp 杂话,剑角是一百八十度。 第二,根据建角判断,若建角为一百零九点五度, 也就是一百零九度二十八分这个左右,那么砸化为 sp 三砸化, 剑角一百二十度,砸画为 sp 二剑角一百八十度 杂话, sp 杂话,由剑角判断。第三,由等电子原理判断,比如二氧化碳是直线性 碳 sp 杂话,那么等电子起到硫氢酸根离子 蛋的阴离子与二氧化碳,他的杂话都是 sp 杂话, 这是一致的。 第四,根据 中心圆子的驾乘电罪判断,如果中心圆子驾乘电罪是四,那么自然是 s p 三杂话, 如果为三 sp 二杂话,如果为二 sp 杂话, 这样的话对杂话的方式, 一个有分子或者微粒的形状确定。第二,根据剑角确定。第三,由等电子原理相似性来确定。 第四,有驾乘电子队来确定。 第一题。
 10:47查看AI文稿AI文稿
10:47查看AI文稿AI文稿首先,我们来观察碳元素的原子轨道。 r s 的原子轨道是一个球体,而三个 r p 轨道形似哑铃,并倾向于三条轴, r p x, r p y 和 r p c。 有百分之九十的机会电子会出现在这四个原子轨道里。 现在把它想象成三维图形。我们注意到电子可以活动到二批轨道的两页。 通过观察碳的简易电子组态,我们可以把电子从 r s 轨道 提升到未填满的二 p g 轨道。尽管有四个不成对的电子可以合成化学键,我们还是不可以解释实验观察到的四架碳的键脚。因此,当我们把二 s 和所有的二 p 轨道杂交起来,会得到四个新的减并能量的杂交轨道。 这个新 s p 三轨道的形状是一个 s 和三个 p 轨道的结合。 正如其他所有轨道百分之九十的机会,我们可以在杂交轨道的三位图形里找到电子杂交碳。现在有四个不成队架电子,并且命名为 s p 三杂交碳。 当我们重叠四个 s p 三杂交轨道在碳原子上,它会变得笨重并无趣。 因此我们只是介绍杂家轨道里电子的活动轨迹在三维中倾向于什么形状。四个新的杂家轨道为了最小化电子互吃力,会尽量远离对方, 因此他们会倾向于移动到四面体的棱角,并且各自形成一百零九点五度建角。 老师会把 s p 三的杂交碳画成黑板上展示的样子。图中两条实线在平面板上,线形物带 代表向着外面的电子,虚线代表向着内侧的电子。 在这四个 s p 三杂交轨道中,各带有一个可以形成共加建的电子, 这个 s p 三杂交探现在可以形成四个共加键。 在这里, x 代表任何有一个能形成供价件的价电子的原子。由于电子密度相对称的存在于一条穿过两个相邻的原子河的假象线上,我们称这些化学件为塞马件。 甲烷就是一个 x p 三杂交碳的例子。 由于他有四个一样大小的氢原子,这些原子会为了把护士力减到最小而尽量远离对方。所以甲烷的理想建角是一百零九点五度。 老师会把甲烷的结构化成黑板上显示的样子。线形物代表平面上其中一个向着外面的氢原子,而虚线代表另外一个向着内侧的氢原子。与解决 s p 三杂交轨道的第一步 相似,我们可以把二 s 轨道上的电子提升到没有被占据的二 p c 轨道。把二 s 轨道和两个二 p 轨道杂交起来,我们就有了三个新的简并能量的杂交轨道。 新的 s p 二杂交轨道的形状与 s 轨道的一部分和 p 轨道的两部分结合,形状非常相似。 与所有的轨道一样,在这些杂交轨道的三维结构中,我们有百分之九十的机会找到电子。现在这个 s p 二杂交碳的三个电子占据了杂交轨道一个电子。在非杂交轨道二 p c 轨道上。 当我们把三个 s p 二杂交轨道和一个二 p c 非杂交轨道重叠到碳原子上,这个结构会变得非常复杂。 因此,我们只需要简单的展示杂交轨道上电子在三维世界中的导向,并且为了更容易观察非杂交轨道,劈的电子密度会被收缩到其大小的三分之一。三个新的杂交轨道会尽量远离对方, 因为他们要将互持力降到最小,因此他们的导向会呈一百二十度角。 老师一般会把 s p 二杂交碳的形状画成黑板上的样子。同样的实现代表在平面板上的 氢原子,血型物代表向着外侧的氢原子,虚线代表向着内侧的氢原子。在展示 spr 杂交结构块是如何参与化学件的形成之前, 我们必须记得非杂交的二批轨道上的电子可以活动到轨道的两页。每个 s p 二杂交轨道有一个电子可以形成一个 sigma 键,因此 s p 二杂交碳可以形成三个 sigma 键和一个拍键。 其中一个由多个 s p 二结构的碳组成的碳化合物的例子就是乙烯。从平面的路易斯简图我们知道每个碳原子会组成三个 sigma 键和一个拍键,因此两个碳原子都会杂交化为 s p 二。 以两个 s p r 杂交模板为基础,我们可以通过碳元素之间形成的 sigma 键在三维中建造分子的整体结构。然后四个构造以稀平面 sima 键的探清键也会形成。第二个在碳元素之间形成的化学键叫拍键。 我们可以把它想象成两个相邻平行并且非杂交的二 p c 原子轨道重叠起来。与分析 sp 三和 sp p 二杂交轨道相似,我们可以想象从 r s 原子轨道中提升一个电子到没有被占据的二 p c 原子轨道上。 将 r s 原子轨道和一个二 p 原子轨道杂交在一起会产生两个新的简并能量杂交轨道。 这个新的 s p。 杂交轨道的形状与一个 s 轨道和一个 p 轨道的重合相似。 就像之前章节中提到的,当我们从三维世界观察轨道,我们有百分之九十的机会在这些杂交轨道中找到电子。现在, s p。 杂交碳有两个电子占据了杂交轨道,另外两个电子占据了非杂交二批轨。 当我们把非杂交的二 p y, 二 p c 轨道和 s p。 杂交轨道附加到碳原子上,碳原子的结构会变得非常复杂。 因此,我们只需要展示三维世界中杂交轨道里的电子活动倾向于什么形状。另外,为了更容易观察非杂交劈,轨道中的电子云密度会被缩小到他本身大小的三分之一。两个新的杂交轨道会为了减小互吃力而尽量远离对方, 因此他们会乘一百八十度角分离。在展示 s p。 杂交轨道在形成化学件中的作用之前,我们必须回忆起非杂交二 p 轨道中, 老师一般会把 s p。 杂交碳画成黑板上展示的样子。同样的实线代表平面上的原子团。画了阴影的页面向着平面外,虚线代表向着内侧的原子团。 每个 s p。 杂交轨道带有一个可以形成 sigma 键的电子。 s p。 杂交碳现在可以形成两个 sigma 键和两个拍键。 一个简单的 s p。 杂交碳物 是乙缺,俗称电池器。从二维路易斯检图中我们会发现,每个碳会形成两个 sigma 键和两个拍键,因此这两个都是 sp 杂交碳。 我们可以以双碳之间形成的 sigma 键为基础开始建造整个 s p 杂交的三维结构。接着两个碳氢 sigma 键会形成,他们负责组成以缺平面 sigma 键的结构。 第二个和第三个化学键会在碳原子之间形成,称为拍键。我们可以想象他们为两对相邻平行并且非杂交的二批原子轨道相重叠。
 04:00查看AI文稿AI文稿
04:00查看AI文稿AI文稿在上节课中,我们知道很多原子在形成共价键时,会发生轨道的杂话有 sp 三杂话、 sp 二杂话和 sp 杂话三种。 由于 sp 三杂话轨道是成正四面体的分布, sp 二杂话是平面三角形的分布, sp 杂话是直线型的分布,就造成了不同的分子有不同的空间构形。 我们今天就来总结一下如何去判断 abn 型分子的空间构形以及中心原子的杂话方式。 在 abn 型分子中,我们根据 b 原子的不同分两种情况来看,第一,如果 b 是轻原子,有素原子,这种就看成一个 b 原子对 a 原子提供一个电子。第二种情况, b 原子是养原子或者留原子,我们则看成 b 原子不与 a 提供电子。第二步呢,我们就去计算 a 原子上一共有多少个电子参与杂话,就是将 a 原子的最外层电子加上 b 原子提供的电子。 第三步,将参与杂话的电子数除以二,得到的数字就是杂话轨道的数量,也就是下层电子对数, 一共会有三种情况,当然,杂话轨道数是二,那就是 sp 杂话分子就是直线型,当轨道数是三,就是 sp 二杂话分子呢,就是平面三角形,轨道数是四,就是 sp 三杂话就是正四面体了。 光看方法是不是觉得有点复杂,我们用栗子来试一下,就会发现,方法其实还是很简单的。 四绿化碳,中心原子是碳,绿原子给碳提供电子,一共四个绿原子就是提供了四个电子,再加上碳最外层的电子数,一共有八个电子参与杂话,那么轨道数就是四。嗯,四绿化碳是正四面体没错, 再看安器,三个轻原子提供给弹,一共三个电子,加上弹原子最外层的五个电子,一共就是八个电子参与杂话。没错,弹原子也是 sp 三杂话。不过由于在安气中,弹原子的四个杂话轨道只有三个是形成了共价键, 还有一个轨道是一对孤队电子,所以在正四面体的基础上矮了一截,所以安汽就是三角锥形了。是不是很简单呢? 掌握了分子空间构形的判断,我们再来延伸一下吧,看看离子吧,我们就用俺跟离子和碳酸跟离子来介绍一下。方法 其实很简单,先不看离子所带的电鹤量,用刚刚的方法计算出参与杂话的电子数量,然后呢,再算上离子所带的电鹤量, 就是离子中参与杂话的电子数了,这个数除以二就是驾乘电子对数就可以判断了。比如俺跟离子,大圆子最外层是五个电子,四个轻圆子提供四个电子,但是俺跟离子是带一个正电鹤的, 所以还要再扣除一个电子,那么参与杂话的电子数就是五加四减一等于八,所以俺跟例子中大圆子也是 是 sp 三杂话,但原子连接了四个青原子,所以俺跟离子的空间构型就是正次面体。 再试试碳酸根,碳原子最外层是四个电子,两原子不提供电子,碳酸根离子带两个负电荷,所以再加上两个电子,一共就是四加二等于六,六个电子参与杂话, 下层电子对就是三,所以是 sp 二杂话。碳原子连接了三个氧原子,所以碳酸根离子就是平面三角形结构了,怎么样,简单吧。
551化学杜杜老师来了 06:04查看AI文稿AI文稿
06:04查看AI文稿AI文稿我们来看一下杂化轨道理论,所谓杂化轨道理论呢,就是怎么说呢?他是解释分子结构的时候呢,用到的一个理论,那么谈到杂化轨道理论呢?我们要从哪开始?我们要从甲烷开始啊,最早我们在认识甲烷的时候呢, 甲烷的分子式,那么这个甲烷的分子式呢?我们写成这个样子啊,我们是不是这个结构式啊?结构式写成这样子,那我们明确的发现碳是分四个清洁的,当时我们在学甲烷的时候呢,我们有两个考虑,第一个你到底是平面的结构, 还是一个正四面体的一个,所以我们探究这个问题,那么现在我们在选修二的时候呢,在探究这一块问题,我们从这往下来走啊,我们来看一下,那么首先我们拿到探,我们看他的具体成见是怎么成见的啊?我们拿到探以后呢,我们知道探的价面 试试二,二 s 二,二 p 二,那么我们化成他的轨道排出图以后呢,应该是这个样子啊,那么轨道排出图,那么他在反应的时候,首先啊他要形成四个单电子,也就是说他会把这一个 二 s 的电子激发了什么二 p 轨道器,把二 s 电子激发的二 p 轨道以后呢,让我们来看一下这样的,那么在二 s 里面呢,有一个单电子, 那么在二 p 的三个轨道里面呢,每一个 p 轨道里面都容纳一个什么单电子?那然后呢,如果说我们用这四个单电子去承建,那我们都知道 rs 能级和二 p 能级,他的能级的能量是不一样的, 那么能机的能量是不一样,那么形成的化学剑剑能也是不一样,形成化学剑他也是不一样的,也就 我们不会得到四个完全相同的什么快捷键啊。但是通过我们的实验呢,他这四个快捷键是完全一模一样的四个快捷键。所以在这里面有人就提出了一个构想,提出一个什么样的构想呢?那么在这里面有二 s 二系,那么他把一个 s 给到 和三个是轨道,那么进行了什么杂化,那这个杂化是什么意思呢?就是说对于我们原先的轨道来说,那么他的轨道呢?在我们的 呃原则的空间,他是有四个不同的什么区域,那么经过杂化以后呢?他完成这两个任务,第一个将空间均分,就是把他所占据的什么电子所专用空间的均分啊, 然后呢能量均分,那么在刚开始我们看一下是不是有一个 s 三个 p 进行了什么杂化,那杂化 以后呢,我们当然有几个轨道参与杂化,就会形成几个新的什么杂化轨道啊?那么这是第一个他的过程,第二呢他的结果是什么呢?有几个轨道杂化,那么他就会形成几个新的杂化轨道。那你比如说在这里面我们是一个 s 轨道 和三个轨道杂化,那么我们把它就叫 sp 三杂法,那么也就是说有四个轨道参与杂化,那么他就会形成四个新的什么 sp 三轨道。 那么在这里面我们下来要了解一下这 sk 杂化轨道和没杂化轨道是什么样的呢?我们都知道原先呢我们的 is 轨道它成一个什么球,那么二 p 轨道它分别存在于什么? 停在三个空间啊?首先是不是有这样的 s 弯向上的一个什么球啊? 然后呢他还是在一个什么在黑上的一个什么,这样啊,那么同样他还有一个是什么?他有 xyz 三个方向的什么三个皮轨道啊?对应的什么? py、 pc 和 ps, 那么在这里面,当然如果这是二 p 的二 py、 二 pc 和二 px, 那么当这三个轨道进行杂化的时候呢,那么他会形成一个新的杂化轨道,那么新的轨道长什么样子啊?他,这你记住啊,他是一头小一头大, 那这样的话,你会发现他明显一个好处,有利于什么?这边去发现电子鱼重叠啊,有利电子重叠,那么他会形成几个?一个、两个、三个、四个,有四个轨道杂化,那么他会形成四个这样的杂化轨道,那么四个这样的杂化轨道在空间怎么均分?那么在空间均 飞的话,他那么他会得到一个什么样的形状啊?他会得到这样一个形状啊,在这里面这样一个形状。最早呢,这个杂化轨道呢?也就是那个谁呀?用这个球啊,用气球甩出来的啊,甩出来的,那么他的箭轴基本上就是这样的一个方向啊,在这里面呢,他有一个什么轨道,对不对?在这个方向上呢?他有一个, 那这个方向呢?有一个在这个方向呢,那么他会有这四个什么杂化轨道?那么杂化轨道完以后,我们每一个轨道里面填充一个断电子再去乘电,你会发现他这会乘着四个键是不是一样的,那么通过这个里面呢?那么我们把清颜色,哎清颜色进行轨道重叠, 那么这样呢很容易,其实其实就解释什么讲完的时候是正四面积结构啊,所以在这里呢杂霸呢?我们其实在我们中学阶段能提到杂霸,我们提到几个杂霸 三,一个是什么 sp 咋办啊?他是成什么直线型?一个是 sp 二咋办?他是成什么平面三角形啊?还有一个 sp 三咋办? 他是成什么?这么思念,那么也就是对应的我们在这里面啊,用气球甩出来的话,这这是什么 sp 三,那么在这里面我们如果很形象的去理解他的话啊,站在这里面我们就更好去理解了。你看倘若如果说是两个轨道打法,那 sp 打法,那么他就一百八十, 如果是 s p 二的话呢?他就是什么一般是不是,那么这样的话呢?你看在这里看到正式电子杂法,他就很明确,他接完四个清理以后呢,他就是正式电子结构,所以在这里面啊,对于解释讲完就很清楚,重点的问题在于什么呢?第一个他有几个轨道进行杂化,他就会形成几个 叫什么杂化轨道,所以我们把它叫四个 sp 三杂化轨道,这个过程呢,我们叫什么杂化?然后呢在这里面他在这里的杂化的过程注意空间均分和什么能量均分,所以他四个键的能量是什么是一样的啊。
5622松哥化学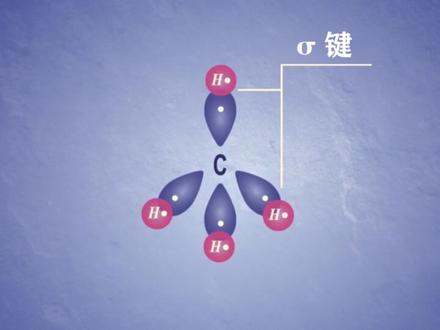 01:23查看AI文稿AI文稿
01:23查看AI文稿AI文稿go wanna birthday but you watch it i want the dress third ok。
3.7万地球小视 15:00
15:00 14:19
14:19 15:15查看AI文稿AI文稿
15:15查看AI文稿AI文稿好最近的各位同学啊,今天我们继续学习呃这个高山一轮复习啊,今天主要是讲那个砸骨刀理论和配微键啊。 呃这一块呢,就像我之前说的一样,就是对于炸好轨道理论,家电家电子城呼哧理论呢,呃这也是高考必考的内容啊,所以说大家呢还是一定要学会。呃,如果有问题呢,也欢迎大家随时与我沟通啊,咱们来共同看一下这一块的内容啊。 呃首先呢第一个呢就是呃咱们看一下打滑轨道理论啊,那么理论的要点呢还是那样的啊,就是对于原子成建的时候啊,原子的架电子轨道呢,是相互的混杂 混杂形成啊,与原轨道的树木呢,呃这个相等啊,而且呢能量呢也是相同的啊。杂号轨道,呃什么 意思呢?就是呃咱们知道呢,对于这个呃 p 啊 p 能级呢,咱们讲有 pspipc 啊,他们三者呢是相互垂直的啊。那么按照咱们讲的这个这种情况呢会出现一种 嗯问题就是说,呃我们看某些分子呢,他们的见角呢,并不是九十度啊,而是比如说像一百零九度,二十八分啊,一百零七度啊,啊是甚至一百零四度啊等等啊,就是他不一定是九十度, 那么在这个过程中为什么不是九十度呢?这个地方呢就是提出了一个新的理论啊,就叫杂话轨道理论,也就是说呢对于杂话轨道理论来讲呢,就是咱们认为呢,就是他在组成分子的时候, 就是原子在组成分子的过程中,在成建的时候呢,呃原子的架电子轨道呢,它是这个呃相互 混杂的啊,就形成了,跟原来的轨道不太一样了,但是呢,跟原来轨道的树木是相等的啊,但是能量呢是相同啊,就形成这么一个,那么砸轨道树不同呢,呃,轨道间的这个夹角呢,肯定也是不同的啊, 啊,肯定也是不同的,那么形成分子的空间结构呢,也是不同的啊,就是咱们讲的杂货轨道理论啊,通过之前讲的那个价电的层呼词理论呢,其实咱们也知道啊,不同的分子啊,呃,他们这个轨道数不一样,或者幻觉着就是驾乘电子数不太一样的哈, 那么他们之间的夹角或者他们这个形状呢,也会略有差异啊,这个是咱们说的杂二轨道理论。呃,那么杂二轨道的模型呢?这个地方主要是咱们在高中呢,主要学三个啊,一个是呃,咱们说的 sp 杂话,还有一个呢,就是 s p 二杂话,还有一个就是 sp 三杂, 这个呢是咱们学了三个,呃轨道的类型啊,那么对于 sp 杂话来讲呢,它是有什么呢?它是有一个 s 啊,一个 s 轨道和一个 p 轨道啊,杂话而成的啊。那么对于这种情况的杂话呢, 杂话轨道间的这个夹角是多少度呢?是这个九十度啊,不是,是一百八十度啊,呃,呈现的是直线型啊,这个呢,大家就是如果要是不懂的话就记住他就行了啊,那么对于咱们说直线型的这种分子啊,比如说你像乙缺 啊,对吧,他肯定是什么呢?肯定啊,也轻叹叹轻啊,他们之间加小是多少呢?是一百,呃,一百八十度,原因呢?就是碳原子作为中心原子啊,他采用的砸化方式呢?是什么呢? sp 砸化对吧?当然呢,他俩是 相互推的啊,就是直线形呢,他就是 sp 扎画,对吧?啊,那么咱们看 s p 二扎画啊,那么对于 s p 二扎画呢,他是有什么呢?一个 s 轨道啊和两个 p 轨道,咋画成的啊?还是三个轨道?对, 呃,那么对于三个轨道来讲呢?呃,他们形成的这个形状呢?是平面三角形啊,对啊,那对于夹角来讲呢,你看三个轨道平分的话呢,当然就是一百二十度,对吧? 呈现的就是平面三角形,同样呢, sp 三达画呢,就相当于有四个轨道了,对吧?啊?呃,一个 s 轨道和这个三个 p 轨道杂画而成,那么对于夹角来讲呢,就是一百零九度二十八分, 呈现的就是正市面体型啊,就是关于这个杂话轨道的类型啊。然后呢,咱咱紧接着来看一下啊,杂话轨道与分子立体构形的那么一个关系啊,咱们可以看一下,首先呢,可以看一下 绿化皮,那么对于绿化皮本身来讲呢,它采用的杂话类型是什么呢? sp 杂话啊? sb 杂话。呃,那么咱们可以通过咱们讲的那个架垫子成护士理论来推一下啊, 对于皮垫子来,呃,对于皮原子来讲呢,他的最外层呢,是有两个垫子,对吧?那么两个垫子呢,形成了两个 c 个门键,是不是形成两个 c 个门键, 那么两个 c 哥们见呢,这个地方没有固坠电子,所以说呢,他总共是有两个架层电子,那么形成的这个立体构形呢,根据咱们之前所讲的也知道应该是直线型, 既然是直线型的话,那么他杂话的类型就是什么呢?就是 sp 杂话, sp 杂话,那么轨道的数目呢?就是多少个呢?就是两个啊,加角呢?就是一百八十度啊,立体构形呢?就是直线型,呃,第二个呢,就是咱们讲的三幅画棚,那么对于三幅画棚 本身来讲呢,他跟咱们刚才已经讲的这个呃三绿花棚是一样的啊,三幅花棚呢? 他呢按照啊呃假电子城呼哧理论呢,他应该是什么形状呢?他应该是一个呃平面三角形,对吧?既然是平面三角形啊,他应该就是什么呢? sp 二的话, sp 二的话三个轨道对吧?呃,所以说他的杂话轨道的这个数目是几呢?是三个, 然后呢夹角呢?是一百二十度啊,对于分子的立体的构形来讲呢,他就是平面三角形, 呃,对于假娃来讲呢,他是 s p 三达化啊,那么达化轨道的,呃数目呢?就是四个了啊,比咱们刚才讲的那么四个呢,咱们也知道假娃本身呢,他是这个正四面体啊,那个加角呢,就是一百零九度二十八分啊,哎,他是正四面体结构啊, 就是关于甲烷的,呃杂号轨道与分子立体构形的这么一个关系啊,关系好,咱们看一下下边一个问题啊,这个问题呢也是在高考里边特别爱考的啊,呃,那么比较建角大小的三种思维啊,给大家说一下啊,就是我们 呃之前呢是没有怎么涉及到有关建角的相关知识的啊,但是呢就是未来呢,在考试当中呢,就是他会考建角大小比较啊,我们比较建角大小呢,我们大致上呢,呃第一点呢我们要看什么呢?他的杂话类型 啊,那么由于杂话的时候呢,就是 sp 杂话是一百八十度, sp 二杂话呢是一百二十度, sp 三杂话呢是一百零九度二十八分,所以说呢,呃杂话类型不一样,那么见角呢肯定会有差异啊, 他们分别是 h 一、 h 二和 h 三,那么对于杂话类型相同的啊杂话类型相同的,呃我们看什么呢?我们这个地方呢啊主要是看什么呢?看这个,呃 他们之间的这个吃力怎么样对吧?一般情况下呢对于这个拍电呢,他这个吃力呢要大于什么呢?要大于这个,呃就是拍电的吃力要大一些啊,就是咱们教程上讲的什么呢?孤电子,对 啊,要大于三件啊,大于什么?双件啊,对吧。从排斥力的角度来讲啊固定的,对呢,是大于这个 啊,双剑啊,大于三剑大于双剑啊,对吧?三剑大于双剑,双剑大于单剑的啊,是这么一个排序,呃所以说呢,呃咱们知道啊,你比如说像这个水啊,对吧? 啊像水是吧?哎和这个氨气他们之间这个夹角咱们大家可以想一想啊。呃对于他们来讲呢他们,呃两个呢都是 s p 三达化啊都是 s p 三达化。呃那么对于水来讲呢他有两对固定,对,所以说这个地方吃力大,使得轻氧轻, 这个建角呢要变小啊,没有清淡清,这个建角大啊,对于这个来讲只有一对固定的水是不是?哎没有这个建角大啊,所以说咱们知道水的这个建角确实比安吉的小, 对吧?啊安庆的当然又小于谁啊?小于甲丸,因为甲丸呢,正好咱们说是正式面体一百零九度二十八分,对吧?这个地方呢,就是就是因为他没有固定,对啊,四个均分,对于这个来讲他是不均分的啊,所以说他是一百零七度多一点,他是一百零四度多一点啊,是这样的,这是咱们说的第二条啊,就是看什么呢? 看这个,呃拍键的啊,这个吃力啊,换句话说就是孤天对大于三件啊,大于双件啊,大于这个单件啊,是这样的,第三个呢,呃我们看什么呢?看这个 看这个,呃电复性啊,主要是看电复性啊,就是对于杂话类型相同啊,然后呢就是他的这个分子当中呢,这个拍键的吃力也是相同的。这种情况对于这种情况来讲呢,我们看什么呢?我们看这个, 呃看这个啊,垫腹性,对吧?中心原子的垫腹性越大呢,就是当孤垫队相同的时候啊,中心原子垫腹性越大啊,垫脚呢就应该是越大的,比如说像这两个,对吧?像这两个,那么对于氧本身来讲他的垫腹性大,对吧?氧的垫腹性大, 那么养的颠覆性大。这个地方呢?呃咱们就存在一个什么问题呢?咱们就存在这么一个问题,对吧?那么养和青在连接的时候啊,养和青在连接的时候啊,咱们知道啊,那么 由于这个养的电费应大,所以说这个电子呢,它更接近于谁呢?接近在养的周围啊,接近于养的周围,这样的话呢,两个 这样,这个垫子呢,更接近的话,那这个地方视力就会变大啊,变大呢?呃垫脚就会变大啊,所以说水之间的这个清氧清,这个键要大于硫化氢当中的清流清啊,这个键啊,这是关于第三个。 那么还有一种情况呢,就是孤电子队也相同,中心原子也相同啊,但是呢,这个地方呢,会出现什么呢?配位原子的电电浮性啊,就看什么呢?看配位原子的电浮性,比如说像三伏化旦和三伏啊,三 三六画蛋,那么对于三幅画蛋和三六画蛋也是一样的道理啊,那,那在这个地方呢,说白了,这个蛋和这个符啊,他们之间呢,这个加角,由于这个蛋呢,他这个垫幅性呢,是相同的啊,不论是蛋还是这个这个地方的绿是吧,他们俩的加角是一样的, 但是呢,由于这个符呢,它变分性大,所以说这个垫子呢,更靠近于什么?更靠近于符啊,他俩之间这个次立呢,就会怎么样?就会这个变小一些,也就是这个夹角呢,就会变小一些,也就意味着这个三幅画蛋的这个呃间角呢,是小于三的画蛋的。好吧,呃,咱们来看一下几个例子啊,比如说这个 对他遵循一个什么样的规则啊?咱们看啊,首先三幅画棚和三六画蛋啊,他们的杂话形式不太一样啊,杂话形式不太一样,这个呢,他是这个 s 是 p 二杂话,而对于这个来讲呢,他是 sp 三杂话,对吧?所以说从这个杂话形式来讲就能推出来啊,哪个大是吧?第二个呢,呃,水和二流化碳也是一样的道理啊,这个呢是 sp 呃杂话, 而对于这个来讲呢,是 s p 三杂话啊,所以说这一个呢也能很容易推出来。呃下一个呢,这个呢就属于三个都是 s p 三杂话,都是 s p 三杂话呢。这个地方咱们看什么呢啊? 刚才呢,咱们在讲课的时候咱们也说了,遇到这种情况呢,就看什么呢?看这个,呃 电子对的个数,对吧?对于水来讲呢,他固电的对数是两个。呃,然后呢,安庆呢?是固电对一个,而碳呃而甲烷里边是没有固电的,对的,所以说在这个过程中呢,呃这个水呢?呃他的这个夹角呢应该是最小。 好的啊,啊,这是最小的安气呢,相对来说大一点啊,打完了最大啊,那么再往下呢就是三五花流,跟这个啊流生根啊,也一样道理啊。对于对于他们俩来讲呢,呃这个呢是采用的 sp s p 二杂话,对吧?哎三个轨道 s p 二杂话,而对于这个来讲呢,它是采用的 s p 三杂话啊,所以说从这个杂话的形式啊,就能看出来应该是这样的。 然后呢刚才已经讲过水和硫化氢了啊,这个结果呢?刚才已经讲过了啊,由于这个中心原子的电缝性大啊,所以说这个夹角大啊,也就说这个地方应该填大雨。 这个呢也是两个步行都是一样的,都有一对固定的,对,是吧?啊所以说呢,就是杂话类型相同,都有一对固定的。对,那这样的话 就看中心原子的电复性啊,这个电复性大,所以说这个夹角大啊,下一个呢就是一样。下一个呢跟刚才那个呢是一样的,对吧?呃电复性也是一样的,对吧?这杂话轨道杂话形式是一样的,都是 sp 三杂话。 呃然后呢他们的这个,呃他们的这个都有一个固定电子啊,也是一样的,对吧?也是一样的。然后呢?呃中心原子的电复性啊,也是一样的。那就看什么呢?啊?配原子了,就是这个地方的配原子,配原子来讲呢他的电复性大,所以说这个地方的夹角呢就会呃这个 小一些啊,对吧?这个地方加角就会小一些,因为他离得远嘛啊刚才他们说离得远,所以说加角小一些。呃这个呢跟刚才那个是一样的,都是有一对固定的,对,都采用了 sp 三达化,对吧?那 他的电风性大,所以说这个地方呢电子呢往外拉伸了,所以说这个夹角呢也会变小啊,是这样的。好吧,这是关于这几个尖角的比较。再往下呢就是在甲醛分子当中的这一个啊,呃轻 碳氧他是大于哪一个?对于这个来讲呢咱们说了啊,就是呃双剑的这个刺力,因为他不存在固定的,对吗?呃这个双剑的这个刺力呢肯定是大于单剑的啊,所以说这个地方的这个夹角呢应该填什么呢?这个应该是轻 碳氧应该是大于啊,这个的啊理由是什么呢?理由就是咱们说了就是开键的磁力啊,大于 c 个门键的磁力啊,就这么回答就可以了,好吧,呃那么下一个那个配微键,配微键这地方咱们简单的说一下,就是配微键的形成一定要有什么呢?一定要有固定,对是吧?还要有什么呢?还要有空轨道啊,所以说 他在行程的过程中一方提供孤电坠,另一方呢提供空轨道啊形成。那配配件的表示呢?咱们常用 a 杠 b 啊,这个 b 代表着什么呢? b 代表的是接受孤电子坠的原则啊,接受孤电坠的原则啊,这是关于这一块啊,比如安系啊,当中呢,谁接受了呢啊, 他是有固定对的啊,所以说这个地方是轻接受的,所以说应该指向这个啊,但是呢,对于这个安根来讲呢,他四个蛋清键呢,是一样的啊,看的是不一样的,但实际上是一样的啊,所以说他是四个空间键是完全相同的。好吧, 那么对于配合物来讲呢,对于这个来讲,它分为什么?内界外界是吧,然后呢我们把铜呢称为中心原子啊,然后呢安安安气啊,咱称为配体啊,然后呢弹原子被称为配为原子啊,呃,然后呢 这个四呢称为这个配备数啊,就是关于这一块。好吧,今天这一块内容呢就给大家讲那么多啊,这个有任何问题呢,欢迎大家随时与我沟通。
129飞哥聊化学 02:26查看AI文稿AI文稿
02:26查看AI文稿AI文稿哈喽,同学们大家好,今天呢,老师教大家一个巧用杂话方式判断分子的 vsepr 模型的方法。那废话不多说,大家看拜拜。 只需要大家记住这样的对应关系就就可以了啊,那我们还是 abn 型分子,只要中心圆子,他的杂号方式成 s p 三杂话的,那么他的 vs epr 模型一定是什么呢? 正四面体型或者叫四面体型都可以啊, 那如果是 sp 二咋画的呢?那他的 vs 一 pm 型一定是平面三角形啊, 那如果是 sp 咋换呢?那么他的 vsepm 型一定是什么直线型啊, 大家记住这个对应关系就就可以了啊。我们来看几个实力,你比如说我举几个 sp 三杂话的例子啊,你比如说贾文,安琪, 水分子图画清,他们的 vsepm 模型都是什么呀? 都是正四面体型,还不会砸我方式的。同学们啊,翻,翻一翻我前面的视频看一看啊。那么我们来举一个 sp 二砸画的, sp 二砸画的,我们常见的什么比心 一对吧,本,那么这两种杂号方式呢?找一找我之前有机物中太原子的杂号方式怎么来计算啊,这就为什么解释了 乙烯分子和本的分子他们处于同一平面,那么我们来找一个 sp 咋画的?你比如说乙缺分子,当时我们在学乙缺的时候,是不是学的乙缺,他是一个什么直线型啊, 他的杂号方式就决定了他的 vsepr 模型是不是非常简单呢。好,今天的课就上到这,朋友们再见。
102老张讲化学
猜你喜欢
- 18.0万教化学的小王
最新视频
- 18.0万教化学的小王

